测定冰的熔解热
【引言】
一定压强下的晶体开始熔解时的温度称为该晶体在此压强下的熔点,质量为1g的某种物质的晶体熔解为相同温度的液体所吸收的热量叫做该晶体的熔解热。
本实验采用混合量热测定冰的熔解热,其基本原理是:把待测系统和一个已知其热容的系统混合起来,并使它们形成一个与外界没有热量交换的孤立系统。于是,在此孤立系统中已知其热容的系统吸收(或放出)的热量也就是待测系统放出(或吸收)的热量。已知其热容的系统吸收(或放出)的热量可通过其温度的变化及其热容来求得,于是待测系统放出(或吸收)的热量也便可求得
由此可见,保持系统为孤立系统,是混合量热法所要求的基本实验条件,着要从一汽装置、测量方法以及实验操作等方面去保证。如果实验过程中玉外界的热交换不能忽略,就要做散热活吸热修正。
温度是热学的一个基本量,量热实验中必须测量温度。一个系统的温度,只有在平衡时才有意义,因此计温时必须使系统温度达到稳定而且均匀,永温度计的指示值代表系统温度,必须使系统与温度计之间达到平衡。
【方法介绍】
混合发是热学实验中的一种常用方法,其基本原理可用热平衡方程来描述,即在一个孤立系统中,一部分物体所吸收的热量等于该系统中其他物体所放出的热量。本实验用混合法测冰的熔解热,关键的必须保证系统为孤立系统。
【实验目的】
1.掌握用混合法测定冰的熔解热的方法。
2.学习散热修正的一种方法。
【实验器材】
量热器、物理天平、温度计、水、冰块、秒表、取冰夹子、量筒、玻璃皿、干抹布等。
【仪器介绍】
为了使实验系统(待测系统与已知其熔解热的系统二者合一)成为以一个孤立系统,我们采用量热器。
传递热量的方法有三种:传导、对流和辐射。以此,必须使实验系统与环境之间的传导、对流和辐射都尽量减少,量热器即能满足这样的要求。
量热器的种类很多,随测量的目的、要求、测量精度的不同而异。最简单的一种如图4-4-1所示,它是由热的良导体做成的内筒,放在一较大的外筒中组成。通常在内筒中放水、温度计及搅拌器,这些东西(内筒、温度计、搅拌器及水)连同放进的待测物体就构成了我们所考虑的(进行实验的)系统,内筒、水、温度计和搅拌器的热容可以测知。量热器的内筒置于一绝热架上,外筒用绝热盖盖住,因此其内的空气与外界对流很小。又因空气是不良导体,所以内、外筒间通过热传导传递的热量便可减至很少。同时由于内筒的外壁及外筒的内外壁都十分光亮,使得它们向外辐射热或吸收辐射热的本领变得很小,因而,我们进行实验的系统和环境之间因辐射而产生热量的传递也可减至很小。这样,量热器就可粗略地被看作一个孤立系统了。
外壁及外筒的内外壁都十分光亮,使得它们向外辐射热或吸收辐射热的本领变得很小,因而,我们进行实验的系统和环境之间因辐射而产生热量的传递也可减至很小。这样,量热器就可粗略地被看作一个孤立系统了。
【实验原理】
一、用混和法测定冰的熔解热
将质量为 、温度为
、温度为 (以
(以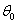 表示)的冰放入质量为
表示)的冰放入质量为 、温度为
、温度为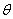 的温水中(温水盛在量热器的内筒里),通过搅拌待冰全部熔解后,其平衡温度为
的温水中(温水盛在量热器的内筒里),通过搅拌待冰全部熔解后,其平衡温度为 。在此交换过程中,冰先吸收热量
。在此交换过程中,冰先吸收热量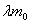 (
(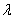 为冰的熔解热)而熔解为
为冰的熔解热)而熔解为 的水,再从
的水,再从 升温到
升温到 ,又吸收热量为
,又吸收热量为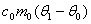 ,
,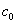 为水的比热容。量热器系统(内筒、搅拌器、温度计)与原来的温水放出的热量可表示为(
为水的比热容。量热器系统(内筒、搅拌器、温度计)与原来的温水放出的热量可表示为(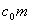 +
+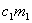 +
+ +
+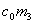 )
)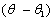 。其中
。其中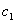 、
、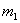 分别为铝的比热容和内筒的质量,
分别为铝的比热容和内筒的质量,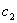 、
、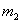 分别为铜的比热容和搅拌器的质量,
分别为铜的比热容和搅拌器的质量,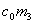 为温度计温度降
为温度计温度降 所放出的热量,它相当于质量为
所放出的热量,它相当于质量为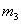 的水温度降
的水温度降 所放出的热量,
所放出的热量,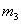 的值由实验室给出(习惯上
的值由实验室给出(习惯上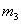 称为温度计的水当量)。根据平衡原理有
称为温度计的水当量)。根据平衡原理有
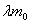 +
+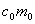
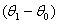 =(
=(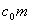 +
+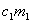 +
+ +
+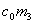 )
)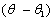 (4-4-1)
(4-4-1)
即
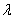 =
=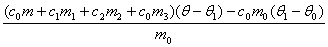 (4-4-2)
(4-4-2)
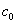 、
、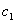 、
、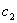 的值分别为
的值分别为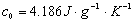 、、
、、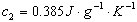 (它们随温度的变化可忽略不计)。
(它们随温度的变化可忽略不计)。
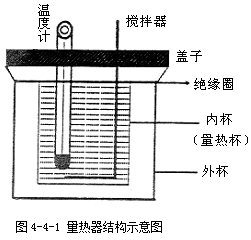 可以看出,本实验的关键是必须保持系统为孤立系统,即系统与外界环境没有热交换,热传递有三种方式:①热传导;②热对流;③热辐射。实验中考虑了整个“热学系统”的吸热与放热,“热学系统”主要由量热器的内筒、搅拌器、温度计以及水和冰块组成。量热器结构上有效地防止热传递。
可以看出,本实验的关键是必须保持系统为孤立系统,即系统与外界环境没有热交换,热传递有三种方式:①热传导;②热对流;③热辐射。实验中考虑了整个“热学系统”的吸热与放热,“热学系统”主要由量热器的内筒、搅拌器、温度计以及水和冰块组成。量热器结构上有效地防止热传递。
量热器的结构如图4-4-1所示,为防止热传递,内筒放在外筒内的绝热支架上可防止热传导,外筒用绝热盖盖住,因此可防止空气与外界对流,而且空气是热的不良导体,所以内、外筒间因对流传递的热量可减至很小。内筒的外壁及外筒的内壁都电镀得十分光亮,使得它们发射或吸收辐射热的本领变得很小,因此可以减小(本实验的热学系统和环境之间)因辐射而产生热量的传递。这样的量热器可以使实验的热学系统粗略地接近于一个绝热的孤立系统了。
二、散热修正
保持实验系统为孤立系统是混合法测定冰的熔解热的必要条件,但是,把冰块投入量热器的温水中,冰块不可能立即熔解,在整个实验过程中,系统必然要与外界交换热量。换言之,系统不是一个严格的孤立系统,这就破坏了式(4-4-2)的成立条件。所以按式(4-4-2)计算出来的熔解热必然存在相当大的误差,为此必须对热量损失进行修正。
根据“牛顿冷却定律”,在系统温度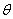 与室温
与室温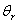 相差不大时,系统与环境之间的传热速率
相差不大时,系统与环境之间的传热速率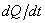 与温差(
与温差(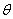 -
-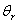 )成正比,即
)成正比,即
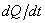 =
=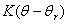 (4-4-3)
(4-4-3)

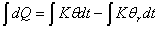 (4-4-4)
(4-4-4)
式中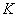 是常量,系统温度
是常量,系统温度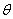 是时间
是时间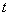 的函数,室温
的函数,室温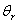 认为是基本不变的。如果我们以横轴代表时间
认为是基本不变的。如果我们以横轴代表时间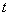 ,以纵轴代表温度
,以纵轴代表温度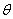 ,作出
,作出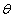 —
—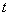 图,则
图,则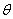 —
—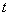 曲线与等温线
曲线与等温线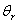 所包围的面积可代表传热量
所包围的面积可代表传热量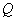 (相差一个比例常数
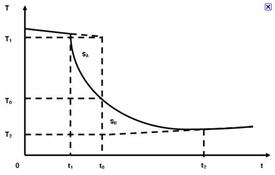
(相差一个比例常数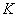 ),如图4-4-2所示。图中
),如图4-4-2所示。图中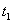 为投入冰块的时刻,
为投入冰块的时刻,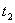 为温度最低的时刻。曲边三角形
为温度最低的时刻。曲边三角形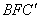 的面积可代表系统向外界散发的热量,曲边三角形
的面积可代表系统向外界散发的热量,曲边三角形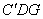 可代表系统从外界吸收的热量。
可代表系统从外界吸收的热量。
把水的初温预热到室温以上,而使冰熔解后系统的末温在室温以下。以室温为界,把整个过程分为放热和吸热两个阶段,这样,就能使在第一阶段和第二阶段不免要发生的热量交换得到一定的补偿。
一般说来,系统向外界散发的热量不会等于它从外界吸收的热量,因为这涉及到的因素很多,诸如水的初温,水的质量,冰块的质量等。为了获得更准确的测量结果,还必须进行散热修正。
图4-4-3表示系统温度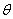 随时间
随时间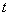 的变化曲线,图中
的变化曲线,图中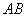 段是投入冰前温水的自然降温曲线(由于温度高于室温
段是投入冰前温水的自然降温曲线(由于温度高于室温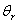 ,系统向外界散热,温度逐渐降低),在
,系统向外界散热,温度逐渐降低),在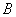 点(温度
点(温度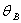 )将冰投入水中,
)将冰投入水中,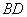 段是投冰后水的降温曲线,到
段是投冰后水的降温曲线,到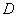 点冰全部熔解并升温至与量热器中水的温度相等,此时温度
点冰全部熔解并升温至与量热器中水的温度相等,此时温度 低于室温
低于室温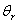 ,系统将从外界吸收热量而逐渐升温,如图中
,系统将从外界吸收热量而逐渐升温,如图中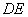 段所示。
段所示。
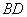 段水的温度由
段水的温度由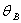 降至
降至 是由两个因素共同造成的,一个是系统与外界有热交换导致水温变化(其中系统向外界散发的热量可用面积
是由两个因素共同造成的,一个是系统与外界有热交换导致水温变化(其中系统向外界散发的热量可用面积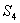 表示,从外界吸收的热量可用面积(
表示,从外界吸收的热量可用面积(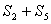 )表示,系统从外界吸收的净热量表示为(
)表示,系统从外界吸收的净热量表示为(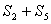 -
-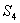 ),图中
),图中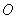 是
是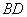 与
与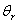 等温线的交点)。另一个是冰的吸热引起水温下降。因此,只是因为冰的吸热引起的水温下降并不等于(
等温线的交点)。另一个是冰的吸热引起水温下降。因此,只是因为冰的吸热引起的水温下降并不等于(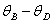 ),用
),用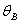 和
和 分别代替式(4-4-2)中的
分别代替式(4-4-2)中的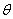 和
和 显然是不妥当的。
显然是不妥当的。
下面我们设计一个与实际过程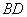 等价的过程,即图4-4-3中的
等价的过程,即图4-4-3中的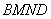 过程(
过程(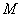 点为理想投冰点),来将上述两个因素分开,将系统与外界的热交换引起的温度变化限制在
点为理想投冰点),来将上述两个因素分开,将系统与外界的热交换引起的温度变化限制在 段和
段和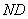 段,所交换热量与
段,所交换热量与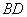 段系统与外界实际交换的热量相等。为此,我们在曲线
段系统与外界实际交换的热量相等。为此,我们在曲线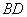 上找一点
上找一点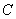 ,过
,过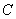 点做时间
点做时间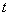 轴的垂线,交
轴的垂线,交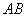 的延长线与
的延长线与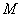 ,交
,交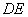 的反向延长线于
的反向延长线于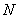 ,使曲边三角形
,使曲边三角形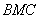 的面积(
的面积(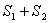 )与曲边三角形
)与曲边三角形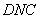 的面积
的面积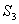 相等,即
相等,即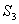 -
-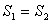 ,那么,过程
,那么,过程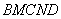 从外界吸收的净热量为
从外界吸收的净热量为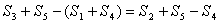 ,这与实际过程从外界吸收的净热量相等。
,这与实际过程从外界吸收的净热量相等。
在过程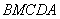 中,设想冰从
中,设想冰从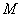 点投入,在
点投入,在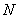 点全部熔解且升温至系统温度最低点,
点全部熔解且升温至系统温度最低点,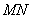 是瞬间进行的“冰的吸热”过程,没有与外界进行热量交换,这样,过程
是瞬间进行的“冰的吸热”过程,没有与外界进行热量交换,这样,过程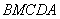 就把上述两个因素分别用过程
就把上述两个因素分别用过程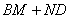 和过程
和过程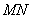 表示了。因此,投冰时水的初温是
表示了。因此,投冰时水的初温是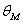 ,末温是
,末温是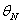 。(
。(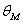 -
-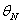 )单纯由于冰吸收热量引起,用它们分别代替(4-4-2)中的
)单纯由于冰吸收热量引起,用它们分别代替(4-4-2)中的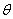 和
和 即可得到较为准确的测量结果,即式(4-4-2)可写为
即可得到较为准确的测量结果,即式(4-4-2)可写为
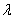 =
=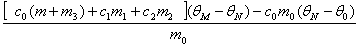 (4-4-5)
(4-4-5)
【实验内容】
1. 测出量热器内筒的质量和搅拌器的质量。
2. 测出室温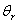 。
。
3. 配制温水,水温高于室温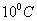 左右。
左右。
4. 测出温水的质量,其水位约为内筒高度的三分之二。
5. 当水温高于室温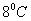 左右时测自然降温曲线(
左右时测自然降温曲线(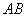 )段
)段 , 每
, 每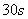 记录一次温度值。
记录一次温度值。
6. 尽快投冰,用搅拌器不断轻轻搅拌,每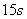 记录一次温度值,直到温度不再下降。
记录一次温度值,直到温度不再下降。
7. 测自然升温曲线(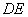 段)
段) , 每
, 每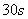 记录一次温度值。
记录一次温度值。
8. 测出冰块的质量。
9. 自己拟定数据记录表格,记录测量数据。
10. 用坐标纸作图,用查小方格个数的方法确定面积,求出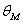 、
、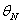 ,求出冰的熔解热
,求出冰的熔解热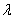 ,并与标准值
,并与标准值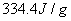 比较,求出相对误差,并进行误差分析。
比较,求出相对误差,并进行误差分析。
【数据记录】
(已知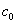 、
、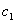 、
、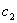 的值分别为
的值分别为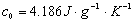 、、
、、 (它们随温度的变化可忽略不计)。搅拌器的质量为m2=6.24g 冰的熔解热参考值 L=3.335*10^J/kg)
(它们随温度的变化可忽略不计)。搅拌器的质量为m2=6.24g 冰的熔解热参考值 L=3.335*10^J/kg)
数据1
表1 实验表格
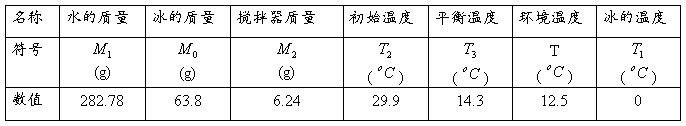
表2 温度随时间变化的实验表格(时间间隔15s)

数据2
表1 实验表格
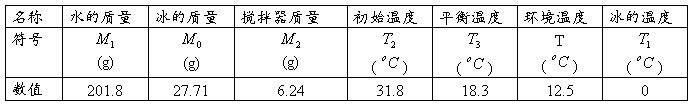
表2 温度随时间变化的实验表格(时间间隔15s)
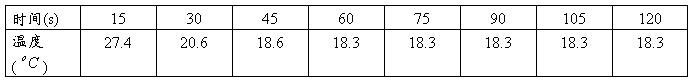
数据3
表1 实验表格

表2 温度随时间变化的实验表格(时间间隔15s)

【数据处理】


L=(201.8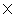 4.186+6.24
4.186+6.24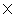 0.38)(31.8-18.3)/27.71-18.3=394.40(J/g) L=(282.7
0.38)(31.8-18.3)/27.71-18.3=394.40(J/g) L=(282.7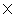 4.186+6.24
4.186+6.24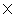 0.38)(29.9-14.3)/63.8-14.3=275.75(J/g)
0.38)(29.9-14.3)/63.8-14.3=275.75(J/g)
L=(246.97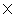 4.186+6.24
4.186+6.24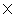 0.38)(29.8-14.9)/42.58-14.9=347.69(J/g)
0.38)(29.8-14.9)/42.58-14.9=347.69(J/g)
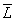 =(275.75+394.40+347.69)/3=339.28(J/g)
=(275.75+394.40+347.69)/3=339.28(J/g)
测定结果的相对误差
U(λ)=  *100%=1.587%
*100%=1.587%
实验图示
【实验结论】
由以上测量结果可见,用混合法测量冰的熔解热为λ=339.28(J/g),其相对误差为1.587%,在大学物理实验要求的误差允许范围内,所以本次实验成功.
【误差分析】
1.实验所取水的体积大于量热筒的2/3。
2.投冰前未将冰拭干或者用手触摸冰造成操作误差。
3.将水倒入量热器后未及时测量水的温度。
4.倒入冰前所测量的水温未达到稳定值。
5.倒入冰后未及时读出温度值。
6.每个时间间隔内所读的温度值有人为的读数误差。
7.实验仪器的保温条件不够,造成的散热误差。
8.实验次数少所造成的偶然误差。
【注意事项】
1.整个测量过程盖子应盖好,还要不停地用搅拌器轻轻地搅拌内筒中的水,以保证热学系统的温度均匀,同时防止内筒中的水搅出内筒外和桌面上,以保持内筒中水的质量不减小。
2.冰的质量应在测出末温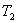 后再称量。
后再称量。
3.热学系统的末温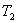 不能选得太低,以免内筒外壁出现凝结水而改变其散热系数。
不能选得太低,以免内筒外壁出现凝结水而改变其散热系数。
4. 时间连续计时,秒表不能停止。
5.室温应取实验前后平均值;水的初温可高于室温约10-15,配置温水时,又应略高于约1-2。
6.严守天平的操作规则。
7.投冰前应将其拭干,且不得直接用手触摸
8.注意维护温度计,玻璃液体(水银或酒精)温度计容易折断,水银泡更易破碎,水银溢出会造成严重污染。
9.先做一次实验,在分析器情况和结果的基础上,确定温度及冰的质量等值大体应以多少为宜,然后仔细的重复实验。
10.测定实验过程中系统温度随时间的变化
每隔一定时间(如15s)测量一下系统温度,做出T-t图,从而:
为了使系统散热、吸热大体抵消,适当选取初始温度和平衡温度。
【思考题】
1.根据本实验装置以及操作的具体情况,分析误差产生的主要因素有哪些?
2.冰块投入量热器内筒时,若冰块外面附有水,将对实验结果有何影响(只需定性说明)?
3.整个实验过程中为什么要不停地轻轻搅拌?分别说明投冰前后搅拌的作用。
4.试分析若系统从外界吸收的热量大于向外界散失的热量,将使结果偏大还是偏小?
5混合量热法所要求的基本实验条件是什么?本实验是如何得到满足的?
6.本实验中的“热力学系统”是由哪些组成的?量热器内筒、外筒、温度计、搅拌器等都属于该热力学 系统吗?
7冰块投入前量热器应该做好哪些准备工作?投冰室应注意什么?
8.试定性说明下述情况给测量结果带来的影响:
(1)测量初始温度是没有搅拌;
(2)测量初始温度后到投冰前相隔了一段时间;
(3)搅拌过程中有水溅出;
(4)冰未拭干就投入量热器;
9.哪些因素会影响测量的准确性?实验中应该怎样注意?
第二篇:测定冰的熔解热研究性报告
《测定冰的熔解热》研究性报告
一、 摘要
冰的溶解热实验以牛顿冷却定律为原理,采用了巧妙的散热修正的方法,减小实验误差。虽然电阻法测温度利用函数计算之后,得到精确度较高的数字,但在用面积法对初末温度进行修正的过程中,由于数格子这一过程较为繁琐,且缺乏较高的精确性,而影响了实验的最终结果。我们的报告利用EXCEL拟合已经精确积分计算的方法,完成电阻和温度较为精确计算,以及面积取等的过程,力求减小实验误差,得到更加的实验结果。
二、 实验目的
1. 学习用混合量热法测定冰的熔解热。
2. 应用有物态变化时的热交换定律来计算冰的溶解热。
3. 学习进行散热修正的方法。
4. 熟悉热学实验中基本仪器的使用。
三、 实验原理
1. 基本原理
本实验用混合量热法测定冰的熔解热。其基本做法如下:把待测系统A和一个已知热容的系统B混合起来,并设法使它们形成一个与外界没有热量交换的孤立系统C(C=A+B)。这样A或(B)所放出的热量,全部为B(或A)所吸收。因为已知热容的系统在实验过程中所传递的热量Q,是可以由其温度的改变△T和热容C计算出来,即Q = C△T,因此待测系统在实验过程中所传递的热量也就知道了。
实验时,量热器装有热水(约高于室温10℃,占内筒容积1/2),然后放入适量冰块,冰溶解后混合系统将达到热平衡。此过程中,原实验系统放热,设为Q放,冰吸热溶成水,继续吸热使系统达到热平衡温度,设吸收的总热量为Q吸。因为是孤立系统,则有:
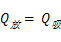
若有质量为M、温度为T1的冰(在实验室环境下其比热容为c1,熔点为T0)。与质量为m、温度为T2的水(比热容为c0)混合,冰全部熔解后系统的平衡温度为T3,设量热器内筒和搅拌器的质量分别为m1、m2(比热容分别为c1 c2),数字温度计浸入水中的部分放出的热量忽略不计。如果实验系统为孤立系统,则热平衡方程式为:
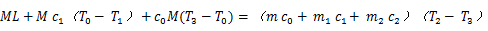
因在本实验条件下,冰的熔点可认为是0℃,所以冰的溶解热为:
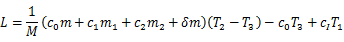
综上所述,保持实验系统为孤立系统是混合量热法所要求的基本实验条件。为此整个实验在量热器内进行,但由于实验系统不可能与环境温度始终一致,因此不满足绝热条件,可能会吸收或散失能量。所以当实验过程中系统与外界的热量交换不能忽略时,就必须作一定的散热修正。
由牛顿冷却定律可知,系统温度Ts 如果略高于环境温度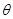 (如两者的温度差不超过10℃-15℃),系统热量的散热速率与温度差成正比,用数学形式表示为:
(如两者的温度差不超过10℃-15℃),系统热量的散热速率与温度差成正比,用数学形式表示为:
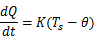
其中K为常数,与量热器表面积,表面情况和周围环境等因素有关。
2. 散热修正
通过作图用外推法可得到混合时刻的热水温度T2',和热平衡的温度T3'。
图中面积SA等于面积SB时,过t0作t轴的垂线,得对应的温度T2'、T3'。
四、 实验仪器
数字三用表、量热器、电子天平、电子温度计、加温器皿。
五、 实验内容与步骤
1. 将内筒擦干净,用天平称出搅拌器加内筒的质量的总和m1;
2. 筒中装入适量的水(约高于室温10-15℃,水质量160-200g),用天平称得内筒加搅拌器加水的质量m1+m;
3. 将内筒置于量热器中,盖好盖子,插好搅拌器和温度计,开始计时并轻轻上下搅动量热器中的水,观察热水的温度变化(如每隔1min记录一个数据),去三到五个点,能得到水温下降的趋势即可,并得到一个初始温度;
4. 初始温度记录后马上从冰箱中取出预先备好的冰块(三块),同时投入水中;
5. 用搅拌器轻轻上下搅动量热器中的水,记录温度随时间的变化,每15s读一次数,当系统出现最低温T3(℃)时,说明冰块完全溶解系统基本达到热平衡,再记录回升温度3-5个点(每1min 测一次),得到水温上升曲线,最末温度必须低于环境温度5-10度;
6. 将内筒拿出,用天平称出内筒(包括搅拌器)和水的质量m1+m+M;
7. 实验完毕,整理仪器,处理数据。
六、 数据记录与处理
1. 原始数据

2. 对应温度

3. 数据处理
通过excel计算线性回归方程:
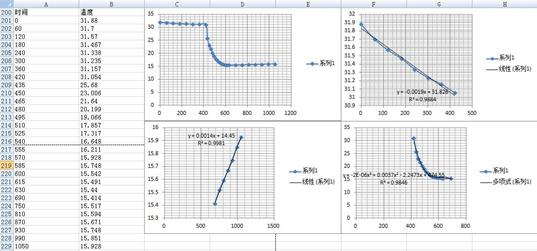
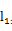 y=-0.0019x+31.826
y=-0.0019x+31.826
 :y=-2
:y=-2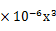 +0.0037
+0.0037 -2.2473x+474.55
-2.2473x+474.55
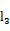 :y=0.0014x+14.45
:y=0.0014x+14.45
解方程:
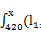 -
-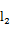 )dx=
)dx=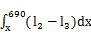
得出T2=30.871℃ T3=15.154℃
又m1+m2=162.52g m0=178.28g M=31.89g
c0 =4.18kJ·kg-1·K-1 cI=1.8kJ·kg-1·K-1 c2=0.389kJ·kg-1·K-1
T1=-21℃ T2=30.871℃ T3=15.154℃
由公式
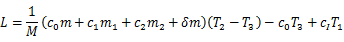
得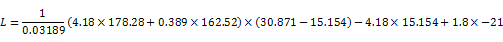
L=297.292kJ·kg-1
七、 误差分析
1. 实验过程中,可能存在系统传热不均的问题。 加热快或搅拌慢了,量热器内的水上热下凉,温度计测得的是高温层的水温,引起计算结果偏小,加热慢了或搅拌过快,搅拌器对水作的功和量热器散热引起计算结果偏大。
2. 实验过程中涉及的热容包括铝质内筒、镀锌铁丝搅拌器、铜杆接线柱、合金电阻丝、铜螺母和金属电阻感应器等,分别都测量热容比较困难,实际上又很多估计值。
3. 实验过程中操作不当,热量散失增大,使L值偏小。
4. 难以保证读数时的时间间隔完全相等,带来数据的误差,对作图有微小影响。
八、 思考题
1.如何求得系统的散热系数K?
K=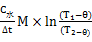 , 任取温度上升过程中的
, 任取温度上升过程中的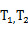 两点。
两点。
2.试定性说明下述情况给 的测量结果带来的影响。
(1) 测初温之前没有搅拌;
答:未搅拌导致T2偏大,由
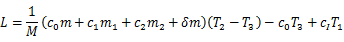
得L偏大。
(2) 测初温后到投冰之前相隔了一段时间;
答:相隔了一段时间导致T2偏大,由
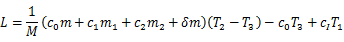
得L偏大
(3) 搅拌过程中有水溅出;
答:有水溅出导致最后系统所测得的平衡温度T3偏小,由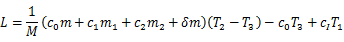
得L偏大。
(4) 冰含水或者未拭干就投入量热器;
答:冰含水或者未拭干使得M偏大,由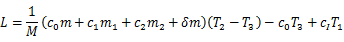
得L偏小。
(5)水蒸发,在量热器绝缘盖上形成露滴。
答:水蒸发带走了热量,使得T3偏小,由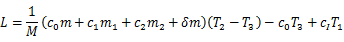
得L偏大。
九、 总结与反思
此次《测定冰的溶解热》实验,我们主要是学习了牛顿冷却定律,以及两种散热修正的方法,虽然实验过程并不复杂,但是这次实验以及数据处理的过程,都使我们有很大收获。
首先,对于实验提出的修正方法。第一种散热修正已经能够是散热和吸热比较好的相互抵消,但是第二种修正方法又进行了进一步的改进,将热量的修正改为了对初末温度的修正,减少了对水初末温度的限制,是实验能够更加精确。这启示我们,为提高实验的精度,首先要想到在原理上提出进一步的改进,对改进的方式不应该轻易满足 ,可以采用替代、转化,利用数学以及作图等多种方法来寻求更好的原理和方法。
第二方面,就是关于数据处理。我们在处理数据的过程中,认识到虽然用电阻值及相应函数,得到具有较高精度的温度值是可以实现的,但是,从实验操作到数据处理的每一个过程和细节都会直接影响到实验最终的精确度。因此我们想到了利用计算机技术,以及精确地函数计算来处理数据的方法。然而,我们也意识到数据处理水平的提高并不能完全地提高实验的精确度,实验方法和应用原理也是至关重要的。虽然这次实验没有想到更为完善的方法,但是,在今后的实验中,我们一定会更加注重理论理解,在实验过程中发现一些小漏洞,思考并寻求更好的解决方法,以保证实验整体的精度。
最后,是关于我们是实验素养方面的。这次实验操作过程并不难,但去需要敏捷的动作、足够的耐心和适当的技巧。比如在投入冰地过程中要迅速的计时,以保证初温的准确度。放入冰块时也要敏捷迅速,这样才不会改变冰块的温度,甚至引起冰块的融化,造成更大的误差。计数时要尽量保证时间间隔的一致,这时的准确读数也是要掌握一定技巧的。而且,更为重要的是,在预习实验的过程中 ,我们也要尽可能多的考虑到实验过程中可能遇到的情况,这样实际操作的时候才能正确迅速的处理,以免造成实验的误差。
