实验20 固相反应动力学
一、实验目的
验证固相反应理论,通过本实验达到进一步了解固相反应机理。通过测定BaCO3-SiO2系统中给定组成的固相反应速度常数,熟悉测定固相反应速度的仪器及方法。
二、实验内容
1.原理
固态物质中的质点(分子、原子或离子)是不断振动的(除绝对零度外),随着温度升高,振幅增大,当达到一定温度时(各种物质不同),由于存在热起伏,使某些质点具有了一定的能量,以至于可以跳离其原来的位置,而产生质点的迁移。这一过程对于单元系统来说就是烧结的开始。这一过程在无气相和液相时也能进行,这就是狭义的固相反应。从广义上讲,所谓固相反应就是有固体物质参加的反应。
固相反应全部过程可分为扩散过程、反应过程及晶核形成过程这三个部分。其中进行得最慢的一个过程控制着整个过程的进行。许多固相反应是由扩散过程控制的,在这种情况下,等温固相反应动力学有三种可能性:
1. 1. 新形成的反应产物层阻碍扩散作用:此时反应速度与产物层的厚度y成反比:
dy/dt=K/y (1)
2. 2. 新形成的反应产物层与扩散作用无关:
dy/dt=K (2)
3. . 新形成的反应产物层能促进扩散作用:
dy/dt=Ky (3)
实际上大部分固相反应属于第一种类型.由(1)式积分得:
y2=Kt (4)
由于实际测量反应产物层厚度比较困难,因此,通常用反应产物百分数x来表示反应程度.设颗粒为球形且反应物与产物的比重相等,则可推得如下方程:
[1-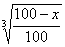 ]2=Kt
]2=Kt
对于BaCO3-SiO2系统,可以用测量反应时放出得气体体积或系统重量损失(重量法)来计算反应产物百分数。但因重量法灵敏度差,故常采用量气法。
量气法一般都在负压下(-40mmHg)进行,这样实验结果准确度高。本实验为便于控制和操作,在常压下进行。
2. 实验装置
实验装置如图20-1所示。
3. 实验步骤
(1) 在分析天平上称0.4~0.5克样品于白金小筒内,塌实,接上悬丝,然后置于炉内反应管中,挂于小钩上。
(2) 检查仪器密封情况,不漏气方可进行实验。采用提高(或降低)水准瓶,使之产生一个水位差(压力差)的方法来检查漏气情况。
(3) 检查线路后,接通电源,按10℃/min的升温速度升温至800℃,并保温10分钟,旋三通开关使反应管与量气筒接通(到指定温度前,反应管放空),记下量气筒的起始读数。
(4) 作好准备工作后,将悬丝脱开,使白金小量筒落到反应管中,同时按动秒表记录时间。第一分钟内每20秒记录一次量气管上的读数。注意读数时应将水准瓶与量气管中的液面保持在同一水平上(为什么?),一分钟以后,每分钟读一次,10分钟后二分钟读一次,20分钟后每5分钟读一次,至60分钟实验结束。
注意整个实验中应严格控制温度,波动范围为<5℃。
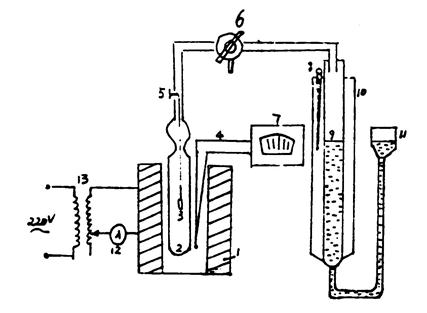
1. 高温炉;2. 反应管;3. 反应小筒;4. 热电偶;5. 挂筒钩;6. 三通开关;7. 温度控制器;8. 水银温度计;9. 量气筒;10. 水套管;11. 水准瓶;12. 电流表;13. 调压变压器
图20-1 量气法装置线路图
样品制备
将BaCO3和石英砂研细,过4900孔筛,SiO2在空气中加热至800℃,保温5小时,BaCO3在CO2气氛中加热到400℃,保温4小时,除去其颗粒表面的吸附水和其它气体,并消除研磨时表面产生的应力。把热处理后BaCO3和SiO2按分子比1:2配好混匀,防于干燥器内备用。
4. 实验结果与处理
(1) 根据实验时的气压及水温,将记录的气体体积换算成为标准状态下气体的体积。
(2) 按反应方程式计算反应的x和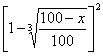
x的求法:
因BaCO3:SiO2=1:2, 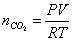 ,
, 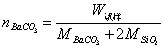
有: 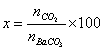
其中: nCO2、nBaCO3分别为CO2和BaCO3的摩尔数
M BaCO3、M SiO2分别为BaCO3和SiO2的分子量
W试样表示试样的重量。
(3) 以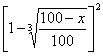 为纵坐标,时间t为横坐标作图。并由所作曲线的斜率计算在给定温度下反应速度常数K。
为纵坐标,时间t为横坐标作图。并由所作曲线的斜率计算在给定温度下反应速度常数K。
三、思考题
1. 把BaCO3与SiO2的分子比由1:2改为2:1对实验有何影响?
2. 影响本实验准确性的因素有哪些?在实验的后期数据为什么偏离直线?
3. 根据本实验可以获得固相反应动力学中哪些数据?如何获得?
第二篇:第四章气-固相催化反应宏观动力学
第四章 气-固相催化反应宏观动力学
在多孔催化剂进行的气-固相催化反应由下列几个步骤所组成:
① 反应物从气相主体扩散到催化剂颗粒的外表面。
② 反应物从外表面向催化剂的孔道内部扩散。
③ 在催化剂内部孔道所组成的那表面上进行催化反应。
④ 产物从那表面扩散到外表面。
⑤ 产物从外表面扩散到气流主体。
①、⑤称为外扩散;②、④称为内扩散;③为本征动力学所描述,存在传质、传热现象(传质系数、传热系数),
描述以上五个步骤的模型称为宏观动力学模型。
§4.1气-固相催化反应的宏观过程
一、气-固相催化反应过程中反应组分的浓度分布
以催化活性组分均匀分布的球形催化剂为例,说明催化反应过程中反应物的浓度分布。
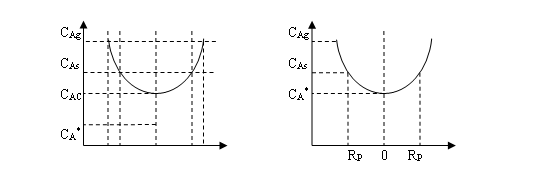
死区:可逆反应,催化剂颗粒中反应物可能的最小浓度是颗粒温度夏的平衡浓度C*A,如果在距中心半径Rd处反应物的浓度接近平衡浓度,此时,在半径Rd颗粒内催化反应速率接近于零,这部分区域称为“死区”。
二、 内扩散有效固子与总体速率
内扩散 内表面上的催化反应}同时进行,使催化剂内各部分的反映速率并不一致,越接近于外表面,反应物浓度↗,产物浓度↘,颗粒处于等温时,越接近于外表面,单位内表面上催化反应速率↗,内扩散有效因子(或内表面利用率)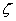 :
:
等温催化剂单位时间颗粒中实际反应量与按外表面组分浓度及颗粒内表面积计算的反应量之比。
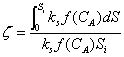
KS为按单位内表面积计算的催化反应速率常数。
Si为单位体积催化床中催化剂的内表面积。
定态下,单位时间内催化剂颗粒外表面由扩散作用进入催化剂内部的反应组分量与单位时间内整个催化剂颗粒中实际反应的组分量相等,所以

即单位时间内从气流主体扩散到催化剂外表面的反应组分量也必等于颗粒内实际反应量,即: 
Se-单位体积催化床中颗粒得外表面积
KG-外扩散传质系数
 -将内、外传递过程影响考虑在内的催化反应总体速率,
-将内、外传递过程影响考虑在内的催化反应总体速率,
若催化反应式一级可逆反应,则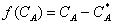
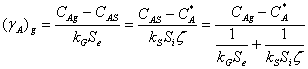
§4.2催化剂颗粒内气体的扩散
一、多孔介质中气体扩散的形式
分子扩散: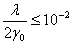
纽特逊扩散(Knudsen) 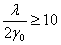
构型扩散 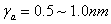 与分子大小相当,扩散系数与分子构型有关
与分子大小相当,扩散系数与分子构型有关
表面扩散(重点了解分子扩散与纽特逊扩散,简要提及构型扩散与表面扩散)
二、分子扩散
Fick定律 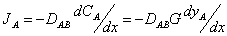
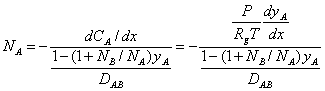
三、纽特逊扩散
直圆孔中Knudsen扩散系数DK可按下式估算:
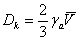 cm2/s
cm2/s
式中 为孔半径cm,
为孔半径cm,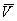 为平均分子运动速度cm/s
为平均分子运动速度cm/s
又 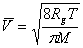
∴ 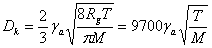 cm2/s
cm2/s
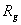 =8.314 KJ/kmol﹒K,M为扩散组分的相对分子量Kg/kmol
=8.314 KJ/kmol﹒K,M为扩散组分的相对分子量Kg/kmol
气体分子的平均自由程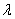 可用下式估算
可用下式估算
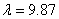 ×10-11/P cm
×10-11/P cm
式中压力P的单位为Pa
一、催化剂孔内组分的综合扩散系数

一般工业催化剂只考虑分子扩散和Knudsen扩散,Ni(D)由两者串联而成,Ni(V)为滞流流动通量,是由催化剂两端存在着相当大的压力差而引起的组分通过多孔粗话机的滞流流动所形成,一般工业催化剂不予考虑可忽略。
孔道内为等摩尔相互扩散时(双组分)

二、有效扩散系数

θ为孔隙率,σ为曲折因子。
§4.3内扩散有效因子
内扩散过程实际为扩散与反应耦合过程,是催化反应宏观动力学的主要研究内容。早在1939年,梯尔(Thiele)就提出球形催化剂内进行一级不可逆反应时反应一扩散方程及其解析解。
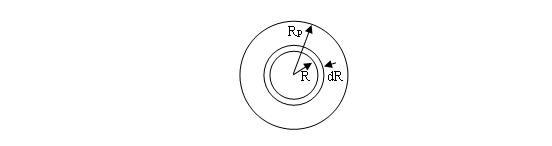
一、球形催化剂颗粒内反应-扩散方程
1、 浓度分布微分方程
取半径为R,厚度dR的微元壳体,定态时,
输入: 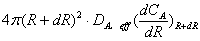
输出: 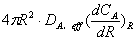
反应量: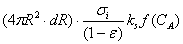 ε为床层空隙率。
ε为床层空隙率。
由输入-输出=反应量(消耗)得:
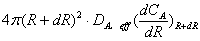 -
-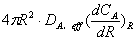 =
=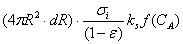
化简得: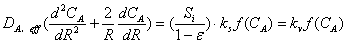
或 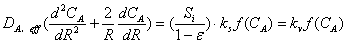
边界条件:
1无“死区”{ 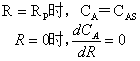
2有“死区”{ 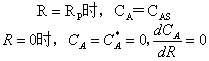
2、 温度分布微分方程
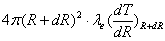 -
-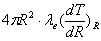 =
=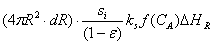
 为反应热,放热反应其值为负,吸热反应,其值范围正,化简
为反应热,放热反应其值为负,吸热反应,其值范围正,化简
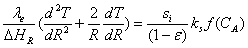
边界条件:{ 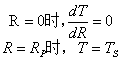
联立以上两微分方程: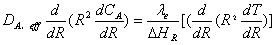
积分得: 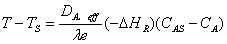
此式与动力学方程形式无关,可由浓度分布推出温度分布颗粒中心处反应物浓度为0时, 取极值:
取极值:

二、等温催化剂一级不可逆反应内扩散有效因子的解析解

令梯尔模数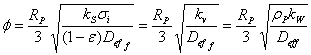 ,则
,则

解之得: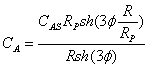
求导: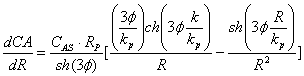
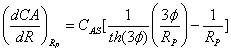
∴ 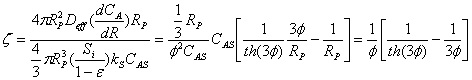

非均相催化过程(反应条件和定时产率的规范值以及反应器类型)