BZ振荡反应实验
一、实验目的
1.了解BZ振荡反应的基本原理;体会自催化过程是产生振荡反应的必要条件。
2.掌握在硫酸介质中以金属铈离子作催化剂时,丙二酸被溴酸氧化体系的基本原理。
3.了解化学振荡反应的表观活化能计算方法。
二、实验原理
BZ振荡反应系统是有机物在酸性介质中被催化溴氧化的一类反应,如丙二酸在Ce4+的催化作用下,自酸性介质中溴氧化的反应。BZ振荡反应是用首先发现这类反应的前苏联科学家Belousov及Zhabotinsky的名字而命名的,其化学反应方程式为:
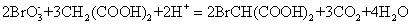 (1)
(1)
真实反应过程是比较复杂的,该反应系统中HBrO2中间物是至关重要的,它导致反应系统自催化过程发生,从而引起反应振荡。为简洁的解释反应中有关现象,对反应过程适当简化如下:
当Br-浓度不高时,产生的HBrO2中间物能自催化下列过程:
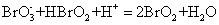 (2)
(2)
 (3)
(3)
在反应(3)中快速积累的Ce4+又加速了下列氧化反应:
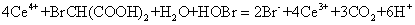 (4)
(4)
通过反应(4),当达到临界浓度值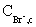 后,反应系统中下列反应成为主导反应:
后,反应系统中下列反应成为主导反应:
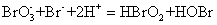 (5)
(5)
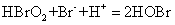 (6)
(6)
反应(6)与反应(2)对HBrO2竞争,使得反应(2)、(3)几乎不发生。Br-不断消耗,当Br-消耗到临界值以下,则反应(2)、(3)为主导作用,而反应(5)、(6)几乎不发生。由此可见,反应系统中Br-浓度的变化相当于一个“启动”开关,当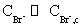 时,反应(2)、(3)起主导作用,通过反应(4)不断使Br-积累;当
时,反应(2)、(3)起主导作用,通过反应(4)不断使Br-积累;当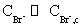 时,反应(5)、(6)起主导作用,Br-又被消耗。由于反应(2)、(3)中存在自催化过程,使动力学方程式中出现非线性关系,导致反应系统出现振荡现象。Br-在(5)、(6)中消耗,又在反应(4)中产生;Ce3+、Ce4+分别在(3)、(4)中消耗和产生,所以Br-、Ce3+、Ce4+在反应过程中浓度会出现周期性变化,而
时,反应(5)、(6)起主导作用,Br-又被消耗。由于反应(2)、(3)中存在自催化过程,使动力学方程式中出现非线性关系,导致反应系统出现振荡现象。Br-在(5)、(6)中消耗,又在反应(4)中产生;Ce3+、Ce4+分别在(3)、(4)中消耗和产生,所以Br-、Ce3+、Ce4+在反应过程中浓度会出现周期性变化,而 和
和 反应物,在反应过程中不断消耗,不会再生,因此,它们不会出现振荡现象。
反应物,在反应过程中不断消耗,不会再生,因此,它们不会出现振荡现象。
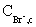 值又反应(2)、(6)可求得
值又反应(2)、(6)可求得
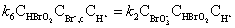
所以 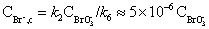
本实采用离子选择性电极上的电势(U)随时间(t)变化的U—t曲线来观察B—Z反应的振荡现象,同时测定不同温度对振荡反应的影响。根据U—t曲线,得到诱导期(T诱)。
设反应的速率方程是:-dc/dt=kcn
在温度T1时速率常数为k1,诱导期为t1,那么
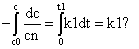
在温度T1时速率常数为k2,诱导期为t2,那么
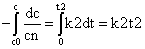
由于起始浓度相同,反应程度相同,所以两式左边的积分值应相同,则有
k1t1= k2t2
即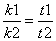
根据阿仑尼乌斯公式:
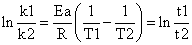
可由诱导期推算表观活化能E诱。
三、仪器试剂
仪器:NDM-1电压测量仪;SYC-15B超级恒温水浴;磁力搅拌器; 反应器100ml;217型甘汞电极;213型铂电极;数据采集接口装置;计算机;
试剂:溴酸钾(GR);硝酸铈铵(AR);丙二酸(AR);浓硫酸(AR)。
四、实验步骤
1.用1.00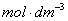 硫酸作217型甘汞电极液接;
硫酸作217型甘汞电极液接;
2.按图连接好仪器,打开超级恒温水浴,将温度调节至25.0±0.1℃;
3.配制0.45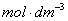 丙二酸250ml、0.25
丙二酸250ml、0.25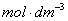 溴化钾250ml、3.00
溴化钾250ml、3.00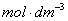 硫酸250ml;在0.20
硫酸250ml;在0.20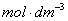 硫酸介质中配制
硫酸介质中配制 的硫酸铈铵250ml。
的硫酸铈铵250ml。
4.在反应器中加入已配好的丙二酸溶液、溴酸钾溶液、硫酸溶液各15ml;
5.打开磁力搅拌器,调节合适速度;
6.将精密数字电压测量仪置于分辨率为0.1mV档(即电压测量仪的2V档),且为“手动”状态,甘汞电极接负极,铂电极接正极;
7.恒温5min后,加入硫酸铈铵溶液15ml,观察溶液颜色的变化,同时开始计时并记录相应的变化电势;
8.电势变化首次到最低时,记下时间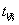 ;
;
9.用上述方法将温度设置为30℃、35℃、40℃、45℃重复实验,并记下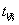 ;
;
10.根据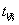 与温度数据
与温度数据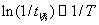 作图。
作图。
五、数据记录及处理
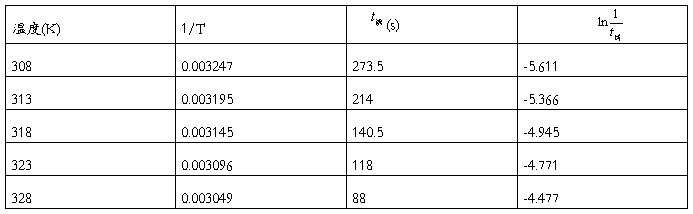
根据实验数据作出 图如下:
图如下:

根据上图可得出直线斜率为k=-5785.64,则表观活化能
E诱=-kR=5785.64*8.314=48850J=48.85kJ
六、注意事项
1.实验中溴酸钾试剂要求纯度高,为GR级;其余为AR级。
2.配制硫酸铈铵溶液时,一定要在0.2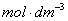 硫酸介质中配制,防止发生水解呈浑浊。
硫酸介质中配制,防止发生水解呈浑浊。
3.反应器应清洁干净,转子位置和速度都必须加以控制。
4.电压测量仪一定要置于0.1mV分辨率的手动状态下。
5.跟电脑连接时,要用专用通讯线将电压测量仪的串行口与电脑串行口相接,在相应软件下工作。
七、思考题
1.试述影响诱导期的主要因素。
答:中间体的生成速率。
2.初步说明BZ振荡反应的特征及本质。
答:BZ振荡反应的特征如下:(1)反应必须是敞开系统,且远离平衡态;(2)反应历程中应包含自催化的步骤;(3)系统具有双稳定性。
BZ振荡反应的本质是必然是耗散结构,化学振荡的动力学具有非线形的微分速率公式。
3.说明实验中测得的电势的含义。
答:说明离子的浓度随时间的周期性变化情况从而导致电势周期性的发生变化。
第二篇:BZ振荡反应实验报告
验九 BZ振荡反应

一、实验目的
1.了解BZ振荡反应的基本原理;体会自催化过程是产生振荡反应的必要条件。
2.初步理解耗散结构系统远离平衡的非线性动力学机制。
3.掌握测定反应系统中电势变化的方法;了解溶液配制要求及反应物投放顺序。
二、实验原理
自然界存在大量远离平衡的敞开系统,它们的变化规律不同于通常研究的平衡或近平衡的封闭系统,与之相反,它们是趋于更加有秩序、更加有组织。由于这类系统在其变化过程中与外部环境进行了物质和能量的交换,并且采用了适当的有序结构来耗散环境传来的物质和能量,这样的过程称为耗散过程。受非线性动力学控制,系统变化显示了时间、空间的周期性规律。
目前研究的较多、较清楚的典型耗散结构系统为BZ振荡反应系统,即有机物在酸性介质中被催化溴氧化的一类反应,如丙二酸在Ce4+的催化作用下,自酸性介质中溴氧化的反应。BZ振荡反应是用首先发现这类反应的前苏联科学家Belousov及Zhabotinsky的名字而命名的,其化学反应方程式为:
 (1)
(1)
真实反应过程是比较复杂的,该反应系统中HBrO2中间物是至关重要的,它导致反应系统自催化过程发生,从而引起反应振荡。为简洁的解释反应中有关现象,对反应过程适当简化如下:
当Br-浓度不高时,产生的HBrO2中间物能自催化下列过程:
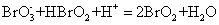 (2)
(2)
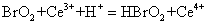 (3)
(3)
在反应(3)中快速积累的Ce4+又加速了下列氧化反应:
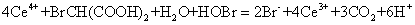 (4)
(4)
通过反应(4),当达到临界浓度值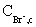 后,反应系统中下列反应成为主导反应:
后,反应系统中下列反应成为主导反应:
 (5)
(5)
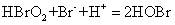 (6)
(6)
反应(6)与反应(2)对HBrO2竞争,使得反应(2)、(3)几乎不发生。Br-不断消耗,当Br-消耗到临界值以下,则反应(2)、(3)为主导作用,而反应(5)、(6)几乎不发生。由此可见,反应系统中Br-浓度的变化相当于一个“启动”开关,当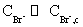 时,反应(2)、(3)起主导作用,通过反应(4)不断使Br-积累;当
时,反应(2)、(3)起主导作用,通过反应(4)不断使Br-积累;当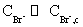 时,反应(5)、(6)起主导作用,Br-又被消耗。由于反应(2)、(3)中存在自催化过程,使动力学方程式中出现非线性关系,导致反应系统出现振荡现象。Br-在(5)、(6)中消耗,又在反应(4)中产生;Ce3+、Ce4+分别在(3)、(4)中消耗和产生,所以Br-、Ce3+、Ce4+在反应过程中浓度会出现周期性变化,而
时,反应(5)、(6)起主导作用,Br-又被消耗。由于反应(2)、(3)中存在自催化过程,使动力学方程式中出现非线性关系,导致反应系统出现振荡现象。Br-在(5)、(6)中消耗,又在反应(4)中产生;Ce3+、Ce4+分别在(3)、(4)中消耗和产生,所以Br-、Ce3+、Ce4+在反应过程中浓度会出现周期性变化,而 和
和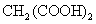 反应物,在反应过程中不断消耗,不会再生,因此,它们不会出现振荡现象。
反应物,在反应过程中不断消耗,不会再生,因此,它们不会出现振荡现象。
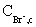 值又反应(2)、(6)可求得
值又反应(2)、(6)可求得
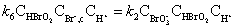
所以 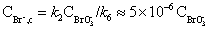
三、仪器与试剂:
NDM-1电压测量仪; SYC-15B超级恒温水浴;
磁力搅拌器; 反应器100ml;
217型甘汞电极; 213型铂电极;
数据采集接口装置; 计算机;
溴酸钾(GR); 硝酸铈铵(AR);
丙二酸(AR); 浓硫酸(AR)。
四、实验步骤:
1.用1.00 硫酸作217型甘汞电极液接;
硫酸作217型甘汞电极液接;
2.按图连接好仪器,打开超级恒温水浴,将温度调节至25.0±0.1℃;
3.配制0.45 丙二酸250ml、0.25
丙二酸250ml、0.25 溴化钾250ml、3.00
溴化钾250ml、3.00 硫酸250ml;在0.20
硫酸250ml;在0.20 硫酸介质中配制
硫酸介质中配制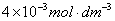 的硫酸铈铵250ml。
的硫酸铈铵250ml。
4.在反应器中加入已配好的丙二酸溶液、溴酸钾溶液、硫酸溶液各15ml;
5.打开磁力搅拌器,调节合适速度;
6.将精密数字电压测量仪置于分辨率为0.1mV档(即电压测量仪的2V档),且为“手动”状态,甘汞电极接负极,铂电极接正极;
7.恒温5min后,加入硫酸铈铵溶液15ml,观察溶液颜色的变化,同时开始计时并记录相应的变化电势;
8.电势变化首次到最低时,记下时间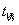 ;
;
9.用上述方法将温度设置为30℃、35℃、40℃、45℃重复实验,并记下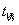 ;
;
10.根据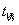 与温度数据
与温度数据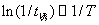 作图。
作图。
五、注意事项
1.实验中溴酸钾试剂要求纯度高,为GR级;其余为AR级。
2.配制硫酸铈铵溶液时,一定要在0.2 硫酸介质中配制,防止发生水解呈浑浊。
硫酸介质中配制,防止发生水解呈浑浊。
3.反应器应清洁干净,转子位置和速度都必须加以控制。
4.电压测量仪一定要置于0.1mV分辨率的手动状态下。
5.跟电脑连接时,要用专用通讯线将电压测量仪的串行口与电脑串行口相接,在相应软件下工作。
六、实验数据及数据处理
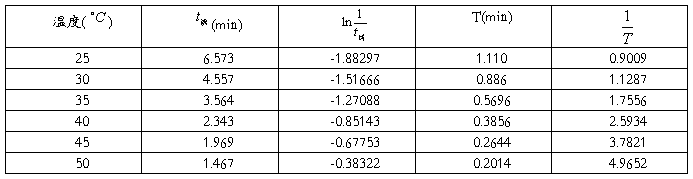
根据实验数据作出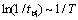 图如下:
图如下:
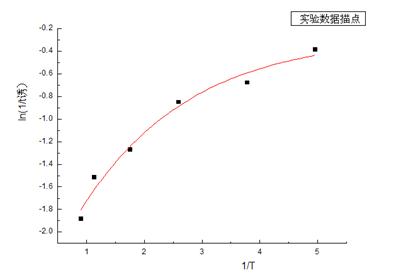
依据上图就可求出任何温度下的诱导期和振荡周期。
七、思考题
1.试述影响诱导期的主要因素。
答:中间体的生成速率。
2.初步说明BZ振荡反应的特征及本质。
答:BZ振荡反应的特征如下:(1)反应必须是敞开系统,且远离平衡态;(2)反应历程中应包含自催化的步骤;(3)系统具有双稳定性。
BZ振荡反应的本质是必然是耗散结构,化学振荡的动力学具有非线形的微分速率公式。
3.说明实验中测得的电势的含义。
答:说明离子的浓度随时间的周期性变化情况从而导致电势周期性的发生变化。
