反应精馏实验装置操作说明
(化工原理、石油化工、化工工艺、医药化工等教学实验用)
一、 前言
精馏是化工工艺过程中重要的单元操作,是化工生产中不可缺少的手段,其基本原理是利用组分的汽液平衡关系与混合物之间相对挥发度的差异,将液体升温汽化并与回流的液体接触,使易挥发组分(轻组分)逐级向上提高浓度;而不易挥发组分(重组分)则逐级向下提高浓度。若采用填料塔形式,对二元组分来说,则可在塔顶得到含量较高的轻组分产物,塔底得到含量较高的重组分产物。
本装置是化学工程与化工工艺、化工研究实验室专用设备,可供有机化工、石油化工、精细化工、生物制药化工等专业部门的科研、教学、产品开发方面使用。用于有机物质的精制分离时,具有操作稳定、塔效率高、数据重现性好等优点。此外,它还可装填不同规格、尺寸的填料测定塔效率,也能用于小批量生产或中间模拟试验。当填装小尺寸的三角型填料或θ网环填料时,可进行精密精馏。装置结构紧凑,外形美观,控制仪表采用先进的智能化形式。
对一般教学用的常减压精馏、反应精馏、萃取精馏玻璃塔来说只有一节塔体,它们在塔壁不同位置开有侧口,可供改变加料位置或作取样口用。而对科研或特殊要求的装置来说,塔体可由不同尺寸的塔节组成,它能方便地组合优化塔高和进料位置。塔体全部由玻璃制成,塔外壁采用新保温技术制成透明导电膜,使用中通电加热保温以抵消热损失。在塔的外部还罩有玻璃套管,既能绝热又能观察到塔内气液流动情况。装置配有玻璃塔釜、塔头及其温度控制、温度显示、回流控制部件构成整体设备。反应精馏的塔体视反应物料的反应性能和催化剂情况而定,对催化剂可溶于原料的条件下,塔体填料只起到提供反应和分离的界面,反应和分离同时进行,两个反应物进料位置可距离远些,而催化剂为颗粒状时,进料位置应在催化剂上方和下方。本实验如果将反应物在釜内进行,塔体就只提供分离的作用,此时也可称为间歇法。对本实验不以颗粒状催化剂为反应条件,采用前者。
二、 图片

三、 技术指标
玻璃塔体内径: 20mm.; 填料高度: 1.4mm ;
填料: φ2×2 mm不绣钢 θ网环;
保温套管直径 : 60—80mm ;
釜容积 : 500ml, 加热功率 : 300w ;
保温段加热功率(上、下):各300w ;
塔的侧口位置:
侧口 : 五个 ; 每口间距 : 250mm, 距塔底和塔顶各200mm。
四、装置结构
控制柜的仪表盘板面布置如图1所示。
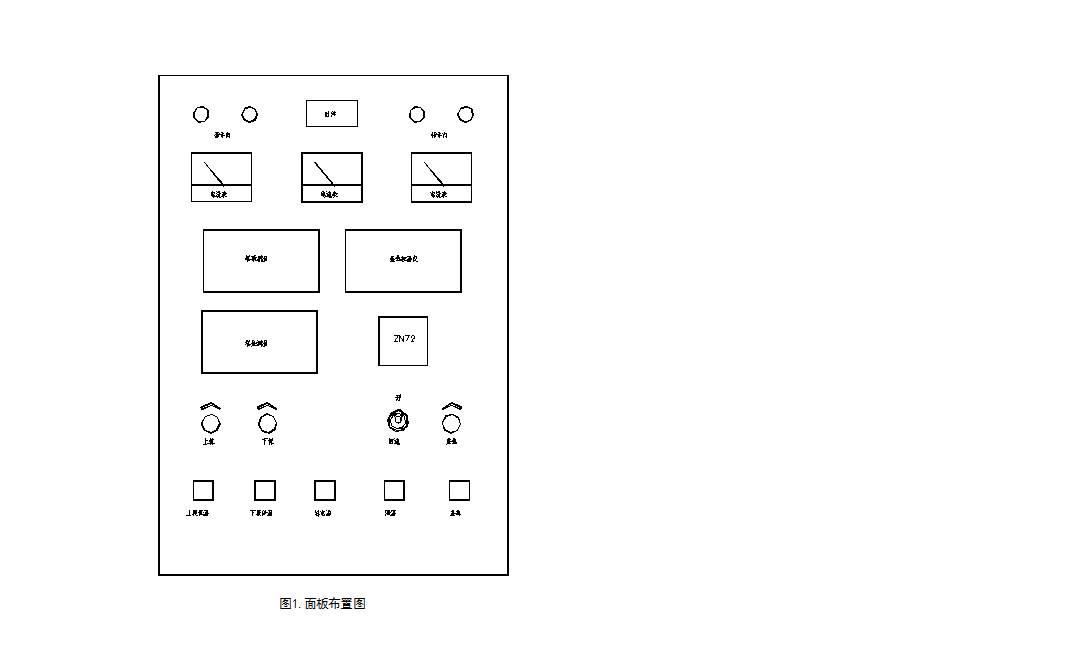
四、操作方法
1、装塔
在塔的各个接口处,凡是有磨口的地方都要涂以活塞油脂(真空油脂),并小心地安装在一起,另外,若用带有翻边法兰的接口时,要将各塔节连接处放好垫片,轻轻对正,小心地拧紧带螺纹的压帽(不要用力过猛以防损坏)这时要上好支撑卡子螺丝,调整塔体使整体垂直,此后调节升降台距离,使加热包与塔釜接触良好(注意,不能让塔釜受压),以后再连接好塔头(注意,不要固定过紧使它们相互受力)最后接好塔头冷却水出入口胶管。(!操作时先通水)
2、将各部分的控温、测温热电偶放入相应位置的孔内。
3、电路检查
(1)插好操作台板面各电路接头,检查各接线端子标记与线上标记是否吻合。
(2)检查仪表柜内接线有无脱落。电源的相、零、地线位置是否正确,无误后进行升温操作。
4、加料
进行间歇的反应精馏时,要打开釜的加料口或取样口,加入被反应的样品,同时加入几粒陶瓷环,以防暴沸。做连续反应精馏时初次操作还要在釜内加入一些被精馏的物质或釜残液。
5、升温
(1)开启总电源开关,开启测温开关,温度显示仪表有数值出现
(2)开启釜热控温开关,仪表有显示。顺时间针方向调节电流给定旋钮,使电流表有显示后,温度控制的数值给定要按仪表的∧、∨键,在仪表的下窗口显示出设定值。需调整参数时,继续按参数键,出现参数符号,并可通过增减键给其所需值。详细操作可见控温仪表操作说明(AI人工智能工业调节器说明书)的温度给定参数设置方法。当给定值和参数值都给定后控制效果不佳时,可将控温仪表参数CTRL改为2再次进行自整定。自整定须要一定时间,温度经过上升、下降、再上升、下降、类似位式调节,很快就达到稳定值。
升温操作注意事项:(1)釜热控温仪表的给定温度大致要高于沸点温度50—80 ℃,使加热有足够的温差以进行传热。其值可根据实验要求而取舍,边升温边调整,当很长时间还没有蒸汽上升到塔头内时,说明加热温度不够高,还须提高。此温度过低蒸发量少,没有馏出物;温度过高蒸发量大,易造成液泛。(2)还要再次检查是否给塔头通入冷却水,此操作必须在升温前进行,不能在塔顶有蒸汽出现时再通水,这样会造成塔头炸裂。
当釜已经开始沸腾时,打开上下段保温电源,顺时针方向调节保温电流给定旋钮,使电流维持在0.2—0.3A之处。(注意:不能过大,过大会造成过热,使加热膜受到损坏,另外,还会造成因塔壁过热而变成加热器,回流液体不能与上升蒸气进行气液相平衡的物质传递,反而会降低塔分离效率)。
(3)升温后观察塔釜和塔顶温度变化,当塔顶出现气体并在塔头内冷凝时,进行全回流一段时间后可开始出料。
(4)有回流比操作时,应开启回流比控制器给定比例(通电时间与停电时间的比值,通常是以秒计,此比例即采出量与回流量之比。
(5)连续精馏时,在一定的回流比和一定的加料速度下,当塔底和塔顶的温度不再变化时,认为已达到稳定。可取样分析,并收集之。
6、停止操作
停止操作时,关闭各部分开关,无蒸汽上升时停止通冷却水。
五、 故障处理
1、开启电源开关指示灯不亮,并且没有交流接触器吸合声,则保险坏或电源线没有接好。
2、开启仪表等各开关时指示灯不亮,并且没有继电器吸合声,则分保险坏,或接线有脱落的地方。
3、控温仪表、显示仪表出现四位数字,则告知热电偶有断路现象。
4、仪表正常但电流表没有指示,可能保险坏或固态变压器,固态继电器坏或加热包电热丝断路。
六、实验指导
(一) 精馏方法选择
1、分离物系的确定:要选择的物系是属于理想溶液还是非理想溶液,如果是前者分离为较纯的物质,相反的只能分离为共沸组成的物质 。为得到较好的数据应选择前者,仅仅为测定塔理论板数的话,最好选正庚烷—甲基环己烷、苯—四氯化碳、苯—二氯乙烷等二元标准体系。
2、普通精馏塔可间歇操作亦可连续操作,不管哪种操作都需要一定的稳定时间,尤其是连续操作更是如此。
3、通常,在不同的二元混合溶液精馏过程中,可定性的看出塔的效率如何。主要是在全回流条件下取塔顶产物分析,纯度越高则效率越高,对共沸物来说,越接近共沸组成则效率越高.
4、做为精馏实验教学训练,选取沸点相差较大的二元混合物系为好,例如:苯—甲苯、苯—二甲苯、甲醇—乙醇、乙醇—丙醇、乙醇—丁醇、正己烷—正庚烷等。以醇类同系物为好,适于做连续精馏。
5、反应精馏、萃取精馏、共沸(恒沸)精馏等特殊精馏,具体操作、分类讲述。
(二) 反应精馏实验指导摘要
反应精馏是将反应与分离过程结合在一起于一个装置内完成的操作过程。当反应处在非均相催化状态下时,即为催化精馏过程,两者都是反应精馏。反应精馏的特点是:
(1)简化了流程;
(2)对放热反应可有效的利用能量;
(3)对可逆反应因能即时分离产物而增加了平衡转化;
(4)对某些体系可因即时分离产物而抑制了副反应;
(5)可采用低浓度原料;
(6)因反应物存在可改变系统组分的相对挥发度,能实现沸点相近或具有共沸组成的混合物之间完全分离。
反应精馏的应用:
主要用于酯化、醚化、皂化、水解、异构体分离等,如:
异丁烯 + 甲醇——→甲基叔丁醚 或其逆反应
丙烯酸酯类+甲醇——→丙基醇+碳酸二甲酯
醋酸 + 醇类——→醋酸酯类
异丁烯 + 水——→叔丁醇
氯乙醇、氯丙醇(皂化)——→环氧乙烷、环氧氯丙烷等
环氧乙烷 + 醇——→聚氧乙烯醚
过程选择:
何种过程才能选用反应精馏?尚未有准确的规定,但从反应物和产物之间挥发度关系去分析考虑还是可行的。把四种物质挥发度大小依次写成A1,A2,A3,A4时, (A)当A 2+ A3 == A1 + A4,则反应物挥发度均介于生成物挥发度之间,选用反应精馏肯定有利。可使转化率超过平衡转化率,甚至达到完全转化。最有利的是能实现产物之间的分离,在塔顶或塔底得到纯品。 (B)当A1 + A2 == A3 + A4(A2 + A3 == A1)或A3 + A4 == A1 + A2(A1 + A2 == A3),产物挥发度全部大于或小于反应物挥发度,则采用催化精馏才有利。 (C)当A1 + A4 == A2 + A3,则所有产物挥发度均介于反应物挥发度之间,不太适于反应精馏。(D)当A1 + A3==A2 + A4 或A2 + A4 == A1 + A3,则反应物和产物挥发度相同也不太适于反应精馏。(E)当A1+A2→A3→A4或A1 + A3→A4,产物与反应物挥发度不同,串联反应适于反应精馏,因产物能不断地被分离可抑制副反应,提高选择性。
反应精馏存在许多复杂因素,要求温度比较缓和,要维持在塔内的个各塔板上有液体即泡点温度,靠调节压力来维持。操作条件相互影响:如进料位置、塔板数、停留时间、催化剂、原料配比、塔内结构,填料形式等都有影响。
实验
《 1.》 间歇式反应精馏
(1) 用量筒取100 ml乙醇 倒入蒸馏釜内.
(2) 取100 ml用已配制好的含硫酸 0.3% (重量百分数) 的冰醋酸,将它倒入釜内.
(3) 按操作程序升温。
(4) 蒸汽上升到塔顶时,全回流二十分钟后启动回流,控制回流比为4:1,并开始收集出料,分析.
(5) 当全回流时,从侧口向上取样分析直至釜顶.
(6) 停止试验,等不再有液体流回塔釜时,取塔顶流出物和塔釜内残留物称重,并分析其值.
(7) 计算出转化率和收率.列出各分析数据,并画出塔填料高度与塔内组成的关系曲线.
《2.》 连续反应精馏
(1) 将釜内填加150 ml已知组成的釜残液。
(2) 开始升温直至塔顶有蒸汽并有回流液体出现。
(3) 从塔的上部侧口以40ml/h的速度加入已配制好的含0.3%硫酸的冰醋酸原料。
(4) 从塔的下部侧口以40ml/h的速度加入无水乙醇原料。
(5) 经15分钟全回流后,开启回流操作,以回流比为4:1维持出料,并稳定1小时后分析塔顶馏出物的重量和组成。
(6) 最后停止操作后,取样分析计算转化率和收率。
(7) 操作中可从侧口取样分析,做出填料高度与组成变化曲线.
分析:
用带有热导池鉴定器的气相色谱仪去分析原料和产物,色谱操作条件:
H2为载体,桥流100mA,柱直径 3 mm ,长1 m。内装填60~80目GD×102 载癸二酸20%,柱前压力0.1Mpa,柱温度120℃,气化室温度130℃,检测器温度120℃。
相对校正因子:水0.74 、乙醇 1.0 、乙酸乙酯1.15、醋酸 1.27。
用面积归一法计算。
分析谱图如下:
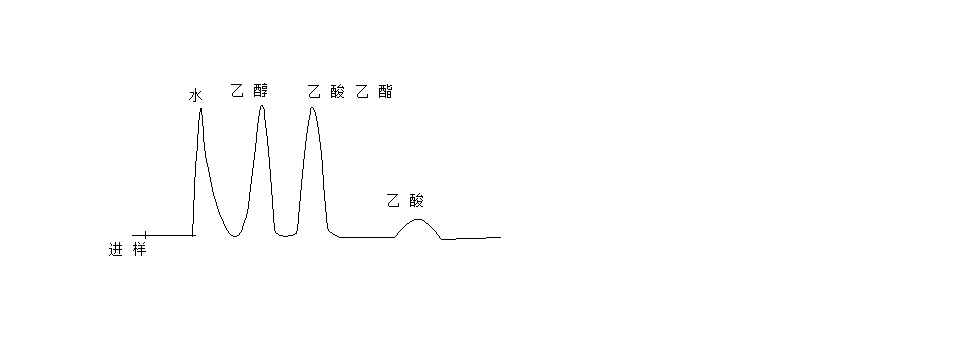
回流器使用说明:
1. 显示器:正常工作时,上边四位LED数码显示延时值,下边四位LED数码显示设定值。
2. 位选键(?):设定时,用于选择某位数码,选中的数码呈闪烁状态。
3. 增加键(▲):设定时按过位选键(?)后,按此键,可改变闪烁位的数值,此数值单向增加。
4.  复位键( ):正常工作时,按下复位键,延时器恢复初始状态;抬起复位键,延时器重新开始延时。
复位键( ):正常工作时,按下复位键,延时器恢复初始状态;抬起复位键,延时器重新开始延时。
5.  暂停键( ):正常工作时,按下暂停键,延时停止,抬起暂停键,延时继续。此功能可作累时器。
暂停键( ):正常工作时,按下暂停键,延时停止,抬起暂停键,延时继续。此功能可作累时器。
6. 延时值设定:在显示范围内利用增加键和位选键即可任意设定继电器的延时值。第一次按位选键(?),POW指示灯亮,下边第一位数码管闪烁,按增加键(▲),设定第一位数值;再按位选键(?),下边第二位数码管闪烁,按增加键(▲),设定第二位数值;依次类推,可设定第三位、第四位数值,此时,数码管仍在闪烁,过8秒钟,闪烁停止,设定值便自动存入机内。利用复位键或复复位端子或重新上电,都可使延时器开始延时,待延时完成后,继电器按其工作方式动作。
注意:在整个设定过程中,应连续进行,每两步骤之间不超过8秒钟。
第二篇:反应精馏实验
实验二 反应精馏
反应精馏是精馏技术中的一个特殊领域。在操作过程中,化学反应与分离同时进行,
故能显著提高总体转化率,降低能耗。此法在酯化、醚化、酯交换、水解等化工生产中得
到应用,而且越来越显示其优越性。
一、实验目的:
1. 了解反应精馏是既服从质量作用定律又服从相平衡规律的复杂过程。
2. 掌握反应精馏的操作。
3. 能进行全塔物料衡算和塔操作的过程分析。
4. 了解反应精馏与常规精馏的区别。
5. 学会分析塔内物料组成。
二、实验原理:
反应精馏过程不同于一般精溜,它既有精馏的物理相变之传递现象,又有物质变性的
化学反应现象。两者同时存在,相互影响,使过程更加复杂。因此.反应精馏对下列两种
情况特别适用: (1)可逆平衡反应。一般情况下,反应受平衡影响,转化率只能维持在
平衡转化的水平;但是,若生成物中有低沸点或高沸点物质存在,则精馏过程可使其连续
地从系统中排出,结果超过平衡转化率,大大提高了效率。 (2)异构体混合物分离。通
常因它们的沸点接近,靠精馏方法不易分离提纯,若异构体中某组分能发生化学反应并能
生成沸点不同的物质,这时可在过程中得以分离。
对醇酸酯化反应来说,适于第一种情况。但该反应若无催化剂存在,单独采用反应精馏操作也达不到高效分离的目的,这是因为反应速度非常缓馒,故一般都用催化反应方式。酸是有效的催化剂,常用硫酸。反应随酸浓度增高而加快,浓度在0.2一1.0%(WT)。此外,还可用离子交换树脂,重金属盐类和丝光沸石分子筛等固体催化剂。反应精馏的催化剂用硫酸,是由于其催化作用不受塔内温度限制,在全塔内都能进行催化反应,而应用固体催化剂则由于存在一个最适宜的温度,精馏塔本身难以达到此条件,故很难实现最佳化操作。
本实验是以醋酸和乙醇为原料,在酸催化剂作用下生成醋敢乙酯的可逆反应。
反应的化学方程式为:
CH3COOH + C2H5OH → CH3COOC2H5 + H2O
实验的进料有两种方式:一是直接从塔釜进料;另一种是在塔的某处进料。前者有间
歇和连续式操作;后者只有连续式。本实验用后一种方式进料,即在塔上部某处加带有酸
催化剂的醋酸,塔下部某处加乙醇。釜沸腾状态下塔内轻组分逐渐向上移动,重组分向下
移动。具体地说,醋酸从上段向下段移动,与向塔上段移动的乙醇接触,在不同填料高度
上均发生反应,生成酯和水。塔内此时有4组元。由于醋酸在气相中有缔合作用,除醋酸
外,其它三个组分形成三元或二元共沸物。水—酯,水—醇共沸物沸点较低,醇和酯能不
断地从塔顶排出。若控制反应原料比例,可使某组分全部转化。因此,可认为反应精馏的
分离塔也是反应器。全过程可用物料衡算式和热量衡算式描述。
1.物料平衡方程
全塔物料总平衡如图1所示。
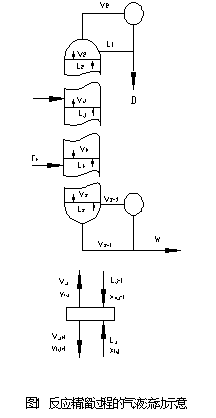
对第j块理论板上的i组进行物料衡算如下:
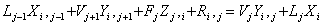 (1)
(1)
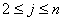 ,
, 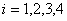
2.气液平衡方程
对平衡级上某组分i有如下平衡关系:
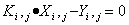 (2)
(2)
每块板上组成的总和应符合下式:
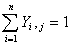 ;
; 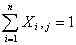 (3)
(3)
3.反应速率方程
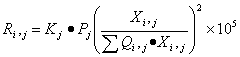 (4)
(4)
式(4)指原料中各组分的浓度相等条件下才成立,否则予以修正。
4.热量衡算方程
对平衡级上进行热量衡算,最终得到下式:
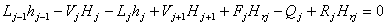
三、实验装置:
实验装置如图2所示。
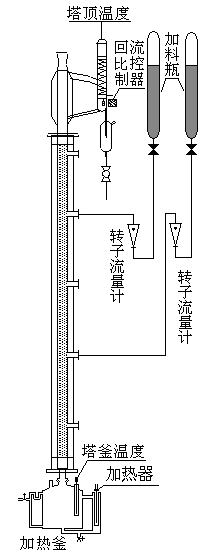
图2 反应精馏实验装置流程图
反应精馏塔用玻璃制成。直径29mm,塔高1400 mm,塔内填装φ3x 3 mm不锈钢θ环型填料;塔釜玻璃双循环自动出料塔釜,容积500m1,塔外壁镀有金属保温膜,通电使塔身加热保温。塔釜用500W电加热棒进行加热,采用电压控制器控制釜温。塔顶冷凝液体的回流采用摆动式回流比控制器操作。此控制系统由塔头上摆锤、电磁铁线圈、回流比计数器等仪表组成。进料采用高位槽经转子流量计进入塔内,可选择不同的进料口。
四、实验步骤:
操作前在釜内加入200克接近稳定操作组成的釜液,并分析其组成。检查进料系统各
管线是否连接正常。无误后将醋酸、乙醇注入原料量管内(醋酸内含0.3%硫酸),打开进料流量计阀门,向釜内加料。
打开加热开关,注意不要使电流过大,以免设备突然受热而损坏。待釜液沸腾,开启塔身保温电路,调节保温电流(注意:不能过大),开塔头冷却水。当塔头有液体出现,待全回流10—15分钟后开始进料,实验按规定条件进行。一般可把回流比给定在3:1。酸醇分子比定在1:1.3,进料科速度为0.5mo1(乙醇)/h。进料后仔细观察塔底和塔顶温度。调节塔顶与塔釜出料速度。记录所有数据,及时调节进出料,使处于平衡状态。稳定操作2小时,其中每隔30分钟用小样品瓶取塔顶与塔釜流出液,称重并分析组成。在稳定操作下用微量注射器在塔身不同高度取样口内取液样,直接注入色谱仪内,取得塔内组分浓变分布曲线。
如果时间允许,可改变回流比或改变加料分子比,重复操作,取样分析,并进行对比。
实验完成旨关闭加料,停止加热,让持液全部流至塔釜,取出釜液称重,停止通冷却水。
五、实验数据处理:
自行设计实验数据记录表格。根据实验测得数据,按下列要求写出实验报告:
1、 实验目的与实验流程步骤;
2、 实验数据与数据处理;
3、 实验结果与讨论及改进实验的建议。
可根据下式计算反应转化率和收率。
转化率=[(醋酸加料量+原釜内醋酸量)—(馏出物醋酸量+釜残液醋酸量)]
/(醋酸加料量+原釜内醋酸量)
进行醋酸和乙醇的全塔物料衡,计算塔内浓度分布、反应收率、转化率等。
实验数据记录及处理
组分 质量校正因子f
水 0.549
乙醇 1
乙酸乙酯 1.109
乙酸 1.225
进样量:0.5μl
Wi%=fiAi%/∑fiAi%
乙酸质量:80.04g 乙醇质量:80.02g
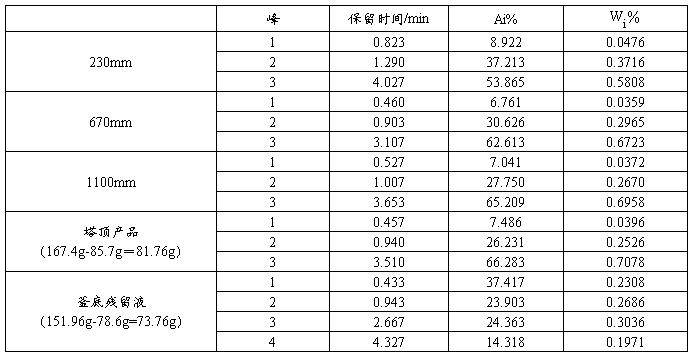
数据处理举例:
1、 各组分质量分数
水: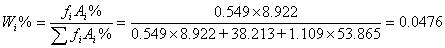
乙醇: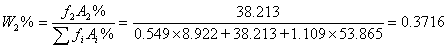
乙酸乙酯: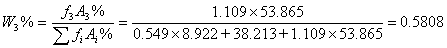
2、 转化率
XA=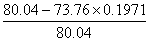 =0.8184
=0.8184
3、 收率
Y=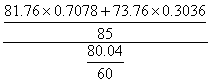 =
=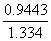 =0.708
=0.708
4、 物料衡算
塔顶产品中,水:81.76×0.0396=3.24g
乙醇:81.76×0.2526=20.65g
乙酸乙酯:81.76×0.7078=57.87g
塔釜残液中,水:73.76×0.2308=17.02g
乙醇:73.76×0.2686=19.81g
乙酸乙酯:73.76×0.3036=22.39g
乙酸:73.76×0.1971=19.54g
反应共生成乙酸乙酯57.87+22.39=80.26g,反应消耗乙酸: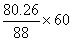 =54.72g,
=54.72g,
由物料衡算反应消耗乙酸为:80.04-19.54=60.5g,两者基本相等,符合物料衡算。
六、思考与讨论
1、 怎样提高酯化收率?
 答:对于酯化反应CH3COOH+C2H5OH CH3COOC2H5+H2O,为可逆平衡反应,一般情况下,反应受平衡的影响,转化率受平衡影响只能维持在平衡转化的附近;但是可以通过减小一种反应生成物的浓度,使平衡向有利于提高转化率的方向进行。反应精馏可以使生成物中高沸点或者低沸点物质从系统中连续的排出,使结果超过平衡转化率,大大提高效率。
答:对于酯化反应CH3COOH+C2H5OH CH3COOC2H5+H2O,为可逆平衡反应,一般情况下,反应受平衡的影响,转化率受平衡影响只能维持在平衡转化的附近;但是可以通过减小一种反应生成物的浓度,使平衡向有利于提高转化率的方向进行。反应精馏可以使生成物中高沸点或者低沸点物质从系统中连续的排出,使结果超过平衡转化率,大大提高效率。
2、 不同回流比对产物分布有何影响?
答:当回流比增大时,乙酸乙酯的浓度比回流比小时要大,但当回流比过大时,传质推动力减小,理论塔板数增大,需要的投资增加。
3、 加料摩尔比应保持多少为最佳?
答:此反应原料反应摩尔比为1:1,为加大反应的转化率通常使某种组分过量,因此在此反应中使乙醇过量,而且乙醇的沸点较低,容易随产物被蒸出,所以加入乙醇的摩尔数应该大于乙酸的摩尔数,比例约为2:1。
七、符号说明:
Fj ---- j板进料流量
hj ---- j板上液体焓值
Hj ---- j板上气体焓值
Hf,j ----- j板上原料焓值
Hr,j ----- j板上反应热焓值
Lj ----- j板下降液体量
Ki,j ----- i组分的汽液平衡常数
Pj ----- j板上液体混合物体积(持液量)
Ri,j ----- 单位时间j板上单位液体体积内i组分反应量
Vj ----- j板上升蒸汽量
Xi,,j ---- j板上组分i的液乡摩尔分数
Yi,,j ---- j板上组分i的气相摩尔分数
Zi,j ----- j板上i组分的原料组成
θi,j ----- 反应混合物i组分在j板上的体积
Qj ----- j板上冷却或加热的热量
