山东大学齐鲁医院医学伦理委员会
临床项目审批件
( )伦审第( )号
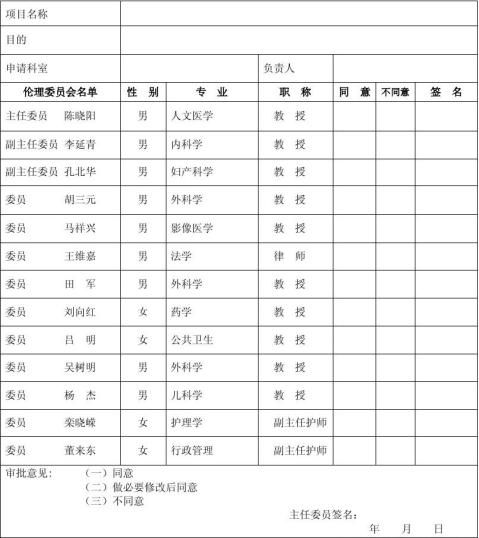
第二篇:新技术应用通过医院医学伦理委员会审核
新技术应用
通过医学伦理道德委员会讨论审核
第一条 为规范医务科技行为,保护受试者研究者及应用者的合法权益,强化法制意识和医德观念,特成立大通乡卫生院医院医学伦理委员会(医伦会)。
第二条 医伦会以医学国际组织理事会及世界卫生组织的有关文献为指导原则,并受中国有关法律法规、制度政策及道德规范的约束。
第三条 医伦会人员应不少于3人,设主任委员1名、副主任2名、秘书2人;委员会的成员须专业化,在民族、文化、经历等方面各不相同。委员会的组成应有从事非医药相关专业的工作者、法律专家及来自其他单位的委员;应有不同性别的委员。
第四条 医伦会的主要职责是负责医药卫生行业科技发展中伦理问题的咨询和审查,主要工作将涵盖整个人类医学领域,包括药品临床试验、器官移植、医疗辅助生育、安乐死、克隆技术与基因工程等方面——
1、审核以人为研究对象的药品临床试验等科研项目/方案。
2、审查涉及人生命健康或组织器官的医疗新技术、新仪器设备、器官移植等新技术和方法的临床应用。
3、审核除上述情况外的其他科研、教学、医疗过程或其成果的医学伦理道德问题。
4、定期审查和监视上述的科研项目、方案、技术、方法的临床试验。
5、审查上述情况/条件下所出现的的严重不良事件。
6、通知没有预见的安全问题,并监督缺陷的整改。
7、进行有关医德国际原则、政策法规、道德规范的咨询,或组织专题培训班或研讨会。
第五条 医伦会成员的职责
1
(一)主任委员的职责
1、贯彻执行医药卫生法规和临床研究道德规范。
2、制定年度工作计划和预算方案。
3、负责向医院汇报工作情况和重大问题。
4、批准全体会议、临时会议等会务安排。
5、主持召开伦理审批会议或专题会议。
6、审定、签发审批件、通知书。
7、批准医疗安全调查报告。
8、批准方案或不良事件的整改意见。
(二)副主任委员的职责
1、贯彻执行医药卫生法规和临床研究道德规范。
2、协助制定年度工作计划和预算方案。
3、安排专家对SAE等进行调查、取证、核实。
4、受委托主持召开全体会议、临时会议。
5、主持审批件、通知书的修改。
6、主持专题业务培训班或研讨会。
(三)秘书长的职责
1、贯彻执行医药卫生法规和临床研究道德规范。
2
2、主持秘书处的日常工作,协助正副主任委员指导委员会的业务开展。
3、主持起草计划、总结、审批件等文书。
4、组织实施会议决议、督办各种事项的落实情况。
(四)委员的职责
1、贯彻执行医药卫生法规和临床研究道德规范。
2、积极参与本会的各种会议,充分发挥自身的专业优势,主动开展业务性工作。
3、监督本会各种决议的执行情况。
(五)秘书的职责
1、负责委员会的会议资料及场地准备,按照主任委员的安排通知开会时间;
2、作会议记录及起草委员会各种决议和文件;
3、负责医院上报材料的整理、归档和保存。
第六条 医伦会的组织和工作应是独立的,不受任何参与试验的申办者(一般是药厂商)、研究者(一般是临床试验单位)的影响。医伦会和知情同意书是保障受试者的主要措施。
第七条 医伦会应建立工作制度和审批工作程序。
1、首先,研究者和申办者向医伦会提出申请并提供必要的资料:卫生制药部门或药品监督管理局的有关的批件;技术质量检查或药品检查报告;该药品、技术、方法临床前和临床有关资料的概述,知情同意书样本,试验研究方案,病例报告表。
2、医伦会应在接到申请后定期召开会议,审阅讨论。每次会议参会人数不应少于总人数的2/3。对试验方案的审查意见应在讨论后,以投票方式做出决定。必要时,可邀请非委员专家出席会议,但非委员专家不投票。
3
3、在审议后,主任委员签发书面意见,并附上出席会议人员的名单、其专业情况及签名。伦理委员会的意见可以是:Ⅰ.同意。Ⅱ.作必要修改后同意。Ⅲ.不同意。Ⅳ.终止或暂停先前批准的试验。
第八条 医伦会对临床试验方案的审查,主要是看否符合《赫尔辛基宣言》等伦理道德标准。其内容是主要包括:
1、研究者的资格、经验是否符合要求,是否有充分时间参加审议中的临床试验,人员配备及设备条件是否符合要求。目的是为了保证受试者在安全、有效的前提下接受临床试验,并使临床试验不致于因为设计不当和技术条件而失败。
2、试验方案是否适当。受试对象的选择要合理,并且使受试者在试验中可能获得的治疗利益大于承受的风险。方案中应事先确定在什么条件下必须终止试验,以保护受试者不受严重损害。试验设计前应充分掌握情报资料;了解药物、技术、仪器、设备等的安全性和有效性,并力求提高疗效,减少不良反应。
3、受试者入选的方法和向受试者或其家属或监护人或法定代理人提供有关的信息资料是否完整、易懂,获取知情同意书的方法是否适当。
4、受试者因参加临床试验而受到损害,甚至发生死亡时如何给予治疗或补偿,以及相应的保险措施。
5、临床试验的最后结果要对病人有利。试验全过程,自始至终要充分考虑受试者获得的利益应大于承受的风险。
6、对试验方案提出的修正意见是否可接受。
7、审查受试者所承受风险的程度。
第九条 任何受试者在参加试验前必须获得知情同意书,经仔细阅读、充分考虑后做出自愿参加试验的决定,并签署姓名和日期。知情同意书应告知受试者以下内容:
1、试验目的。评价一项试验的目的就在于考察其安全性和有效性。同时应强调一项试验,其性质本身就是一种研究,只有在安全性和有效性得到确定保障后,才能允许试验药品上市,或技术、方法、仪器、设备正式应用于临床。
4
2、试验内容和过程。包括试验步骤及所需时间、试验中观察有利和无利的项目及检查的频度、留取血标本的总量等。使受试者知晓本次试验本人需付出什么,也使其在理解试验过程后能更好地配合试验。
3、试验的益处和风险。预测参加试验会缓解或治愈原有疾病的可能性和可能出现的不良反应及其程度,使受试者事先可权衡参加试验的利弊、做好充分的思想准备。
4、目前此种疾病的其他诊治方法及每种方法可能的受益和风险。使受试者对所患疾病的诊治方法有更全面的了解,能更实事求是地决定是否参加试验。
5、试验分组。随机对照试验时受试者有可能被随机分入试验组和对照组,因此还需告诉其对照试验益处和风险。如选用安慰剂对照,需告之有可能分至阴性对照组,且可能在一定程度上影响病情及带来的风险。
6、参加试验的自愿原则。受试者了解上述情况后,必须自愿做出决定是否参加试验。通常应在入选数天前向受试者提供知情同意书,使其有充分的时间考虑,或和家属商量是否决定参加试验。可在试验过程中无须任何理由任何时候退出试验。
7、受试者个人试验资料的保密。明确受试者参加试验及个人试验资料为个人隐私,受试者的全名不会出现在所有记录及文件中(只以姓的拼音及入选编号代表)。只有申办者、研究者、监查员、伦理委员会、药政管理部门有权查阅受试者所有的试验记录资料,而其他人均无权接触个人试验资料。
8、受试者补偿。如发生与试验相关的非正常损害时,受试者可获得及时适当的治疗,以及保险赔付等补偿。以健康人为试验对象进行Ⅰ期临床试验或生物等效性研究时,则应付给相应的报酬。
第十条 医伦会所有会议及其决议均应书面纪录。记录保存及申报审核资料应保存到试验结束后5年。秘书处负责会务安排、资料整理、会议记录、文件起草及档案保存等工作。
第十一条 临床试验方案的执行。
1、方案须经医伦会同意并签发书面意见后方能进行。
5
2、在试验期间中,对所有试验方案或其中知情同意书的任何修改应向医伦会报告,经批准后方能执行。如发现涉及试验用药品的临床研究的技术方法等重要新资料则必须将知情同意书作书面修改送医伦员会批准后,再次取得受试者同意后方可继续进行。
3、在实验中发生任何严重不良事件,均应向医伦会报告。提前终止或暂停一次临床试验,也应向医伦会报告。
4、多中心试验方案及其附件由各中心的主要研究者共同讨论后制定,经申办者同意,伦理委员会批准后执行。
第十二条 医伦会的经费管理,按照国家有关法律法规管理制度执行。依照国际惯例及国内外同行的收费标准收取项目评审费。日常财务管理由主任委员指派专人负责,由秘书长主持编制年度预算及财务分析报表。自觉接受审计和监督。
第十三条 本条例自公布之日起实行,由医院管理处负责解释。
6
