 高一化学期中考试试题(B)
高一化学期中考试试题(B)
可能用到的相对原子质量:H 1 N 14 Cl 35.5 Zn 65
一、单项选择题
1、下列关于钠的叙述错误的是( )
A.实验后剩余的钠粒可放回原试剂瓶中
B.用一般的化学还原法不能制取金属钠
C.自然界中无游离态的钠存在
D.钠着火后可用煤油扑灭。
2、取一小块钠放在燃烧匙里加热,下列实验现象描述正确的是( )
① 钠先熔化 ②燃烧放出黄色火花 ③燃烧后得到白色固体
④燃烧时火焰为黄色 ⑤燃烧后得到浅黄色固体
A.①② B.①②③ C.①④⑤ D.①③④
3、金属钠投入到下列溶液中,既有气体放出,又有白色沉淀生成的是( )
A.盐酸 B.氯化钠溶液 C.氯化铜溶液 D.氯化镁溶液
4、下列物质间发生化学反应,在不同条件下可制得不同产物的是( )
A.Na和O2 B.Na和Cl2 C.Mg和O2 D.Na和H2O
5、当不慎有大量Cl2逸出污染周围空气时,可以用浸有某种物质的一定浓度的水溶液的毛巾捂住鼻子,该物质适宜采用的是 ( )
A.NaOH B.NaCl C.Ca(OH)2 D.Na2CO3
6、含有6.02×1023个O的H2SO4的物质的量是( )
A.1.00 mol B.0.50 mol C.0.25 mol D.0.125 mol
7、a mol H2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为( )
A. mol-1 B. mol-1 C. mol-1 D.mol-1
8、下列说法正确的是(NA表示阿伏加德罗常数的值)( )
A.在常温常压下,11.2 L氯气含有的分子数为0.5NA
B.在常温常压下,1 mol He含有的原子数为2NA
C.32 g氧气所含原子数目为2NA
D.在同温同压时,相同体积的任何气体单质所含的原子数目相同
9、在0.8克某物质中含有3.01×1022个分子,则该物质的相对分子质量约为( )
A.8 B.16 C.64 D.160
10、在标况下,2.24L NOx气体的质量为3.0g则x值为( )
A.4 B.3 C.2 D.1
11、将某溶液逐滴加入Fe(OH)3溶胶内,开始时产生沉淀,继续滴加时沉淀又溶解,则该溶液是( )
A.2 mol/L的NaCl溶液 B.2 mol/L的HCI溶液
C.2 mol/L的蔗糖溶液 D.硅酸溶胶
12、下列溶液中,阴离子浓度最大的是( )
A.0.5 mol·L-1 H2SO4溶液50Ml
B.0.6 mol·L-1 Al2(SO4)3溶液35mL
C.0.8 mol·L-1 NaCl溶液70mL
D.0.7 mol·L-1 Al (NO3)3溶液60mL
13、在无色、酸性溶液中,能大量共存的是( )
A. Ba2+、Cl-、NO3-、Na+ B. K+、Cu2+、SO42-、Cl-
C. Na+、K+、CO32-、SO42- D. Mg2+、SO42-、OH-、NO3-
14、下列离子方程式中正确的是( )
A. 稀硫酸滴在铜片上:Cu + 2H+= Cu2+ +H2↑
B. 硫酸钠与氯化钡溶液混和:SO42-+ Ba2+= BaSO4↓
C. 盐酸滴在石灰石上:Ca2++ 2H+= Ca2+ + H2O + CO2↑
D. 氧化铜与硫酸混和: Cu2++ SO42-= CuSO4
15.下列反应属于非氧化还原反应的是( )
A.Fe2O3+3CO 2Fe+3CO2 B.NH4NO3
2Fe+3CO2 B.NH4NO3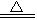 N2O↑十2H2O
N2O↑十2H2O
C.2NaHCO3 Na2CO3+CO2↑十H2O D.2FeCl3+Cu=2FeCl2+CuCl2
Na2CO3+CO2↑十H2O D.2FeCl3+Cu=2FeCl2+CuCl2
16.下列反应中,水作还原剂的是( )
A.2Na+2H2O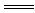 2NaOH+H2↑ B.Cl2+H2O
2NaOH+H2↑ B.Cl2+H2O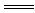 HCl+HClO
HCl+HClO
C.2F2+2H2O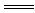 4HF+O2 D.SO2+H2O
4HF+O2 D.SO2+H2O H2SO3
H2SO3
17.下列变化需要加入还原剂才能实现的是( )
A.MnO42- Mn2+ B.HCl
Mn2+ B.HCl Cl2 C.Fe
Cl2 C.Fe Fe3+ D.KClO3
Fe3+ D.KClO3 O2
O2
18、下列含氯化合物中,不能由金属单质和氯气直接反应得到的是( )
A.FeCl2 B.CuCl2 C.AlCl3 D.AgCl
19、下列关于Fe2+、Fe3+ 的叙述中,正确的是( )
A.Fe2+的溶液为浅黄色 B.Fe3+ 的溶液为浅绿色
C.Fe2+既有氧化性又有还原性 D.Fe3+溶液加入KSCN,立即出现红色沉淀
20.将下列四种铁的化合物溶于稀盐酸,滴加KSCN溶液没有颜色变化,再加入氯水即呈红色的是( )
A. FeO B. Fe2O3 C. FeCl3 D. Fe2(SO4)3
21.已知反应3Cl2+6NaOH===5NaCl+NaClO3+3H2O下列说法不正确的是( )
A.Cl2既是氧化剂也是还原剂
B.被氧化的氯原子数是被还原的氯原子数的5倍
C.氧化剂和还原剂的质量比是5: 1
D.NaCl是还原产物,NaClO3氧化产物
22、矿泉水目前已成为人们常用的饮料,市场上有些不法商贩为牟取暴利,用自来水冒充矿泉水出售,为辨别真假,可用下列的一种化学试剂来鉴别,该试剂是( )
A.酚酞试液 B.氯化钡溶液 C.氢氧化钠溶液 D.硝酸银溶液
 二、推断题
二、推断题
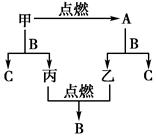
1、 A、B、C是三种常见的化合物,A为淡黄色固体。它们之间的转化关系如图所示:完成下列空白:
(1)A的化学式__________,B的化学式____________。
(2)写出甲+B―→C+丙的化学方程式____________________________
(3)写出A的一种重要用途________________。
2、室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可以按如图所示进行反应。又知E溶液是无色的,F溶液是浅绿色的。

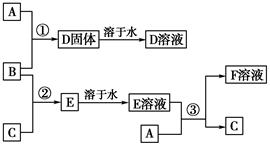
请回答:
(1)试写出下列物质的化学式:A________,B________,C________。
(2)反应①的化学方程式:_______________________________。
(3)反应③的化学方程式: _______________________________。
(4)反应③的离子方程式: _______________________________。
(5)反应④的离子方程式: _______________________________。
三、计算题
1.根据反应8NH3+3Cl2=6NH4Cl+N2回答下列问题。
(1)氧化剂_______,还原剂________;
(2)用双线桥标出反应中电子转移的方向和数目:
__________________________________________
(3)氧化剂与氧化产物的物质的质量之比________
(4)当生成28gN2时,被氧化的物质的质量是__________g。
2.(1)标准状况下,22.4 L HCl气体溶于水,制成250 mL盐酸,所得溶液中氯化氢的物质的量浓度为__________;将该盐酸稀释成1 L溶液A,则其氯化氢的物质的量浓度为____________。
(2)从溶液A中取出250 mL盐酸与足量Zn反应,标准状况下可生成多少体积氢气?(根据化学方程式计算)
高一化学期中考试试题答案(B)
一、1-5:DCDAD 6-10:CBCBD 11-15:BDABC 16-22:CAACABD
二、1、(1)Na2O2 H2O(2)2Na+2H2O 2NaOH+H2↑(3)呼吸面具和潜艇的供氧剂。
2NaOH+H2↑(3)呼吸面具和潜艇的供氧剂。
2、(1)Fe Cl2 H2 (2)3Cl2+2Fe== 2FeCl3
(3)2HCl+Fe== FeCl2 + H2↑ (4)2H++Fe == Fe2++ H2↑
(5)Fe+2Fe3+ == 3Fe2+
三、1、(1)Cl2、NH3 (2) 8NH3+3Cl2=6NH4Cl+N2
(3)3:1 (4)34
2、解析: (1)c=4 mol·L-1,将盐酸稀释成1 L,溶质的物质的量不变,c=1 mol·L-1。
(2)设可生成标准状况下氢气体积为V
Zn + 2HCl === ZnCl2 + H2↑
2 mol 22.4 L
1 mol·L-1×0.25 L V
V=2.8 L。
答案:(1)4 mol·L-1 1 mol·L-1 (2)2.8 L
第二篇:20xx年高一化学下学期期中考试试题及答案
20##年春高一期中考试化学试题
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32
Cl 35.5 Zn 65 Cu 63.5 Ag 108
说明:本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题),共100分,考试时间90分钟。请将第Ⅰ的答案涂在答题卡上;第II卷的答案填在答题纸的相应位置上。
第Ⅰ卷(选择题 共45分)
本题包括15小题。每小题3分,共45分。每小题只有一个选项符合题意。
1.据20##年12月的《参考消息》报道,有科学家提出硅是“21世纪的能源”、“未来的石油”。下列有关说法正确的是
A.地球上有丰富的晶体硅
B.高纯硅可以用石英与C在高温下制取
C.硅是一种良好的半导体材料,所以可以作光导纤维的材料
D.硅便于运输、贮存,从安全角度考虑,硅是有开发价值的燃料
2.下列有关厨房铝制品的使用中,你认为合理的是
A.盛放食醋 B.烧煮开水
C.用金属丝擦洗表面的污垢 D.用碱水洗涤
3.下列说法正确的是
A.3 2He原子核外有3个电子 B.3 2He和4 2He是两种不同的核素
C.O2和O3互为同位素 D.O2和O3的相互转化不是化学变化
4.下列元素中原子半径最大的是
A.F B.O C.Mg D.Al
5.下列说法不正确的是
A.铜在潮湿的空气里会被锈蚀
B.纯铁的抗蚀力很强
C.常温下,金属铝不被空气里的氧气氧化,因而能做导线
D.普通玻璃没有一定的熔点
6. 下列强碱碱性介于KOH和Mg(OH)2之间的是
A. NaOH B.Al(OH)3 C. LiOH D.RbOH
7.下列关于元素周期表的说法正确的是
A.能生成碱的金属元素都在ⅠA族
B.原子序数为14的元素位于元素周期表的第3周期ⅣA族
C.稀有气体元素原子的最外层电子数均为8
D.第二周期ⅣA族元素的原子核电荷数和中子数一定为6
8.将过量的CO2分别通入:①CaCl2溶液,②Na2SiO3溶液,③Ca(ClO)2溶液,④饱和Na2CO3溶液,最终有沉淀析出的是
A.①②③④ B.②④ C.①②③ D.②③
9.取四等份铝,分别加入足量的下列溶液中,充分反应后,放出氢气最多的是
A.3 mol·L-1氨水 B.4 mol·L-1 HNO3 C.8 mol·L-1 NaOH D.18 mol·L-1 H2SO4
10.下列各组离子,能在强酸性条件下大量共存的是
A.Fe3+、Ba2+、Cl-、NO3- B.NH4+、SiO32-、NO3-、Na+
C.NO3-、K+、[Al(OH)4]-、OH- D.Na+、Ba2+、Mg2+、HCO3-
11.原子序数大于4的主族元素X、Y的离子X埘Xm+、Yn-电子层结构相同,则X、Y的下列叙述正确的是:
①原子序数X>Y ②X和Y在同一周期 ③Y与X族序数之差是8—(m+n) ④X、Y核电荷数差为(m—n)
A.①③ B.②④ C.①② D.①②③
12.下列反应的离子方程式正确的是
A.大理石与盐酸反应: CO32- + 2H+ = H2O+CO2↑
B.在氯化铝溶液中滴加过量的氨水:Al3++4 OH-=[Al (OH)4]-
C.在氢氧化钠溶液中通入过量的CO2:2OH-+CO2=CO32-+H2O
D.二氧化硅与苛性钠溶液反应:SiO2+2OH- = SiO32- + H2O
13.已知元素X的原子序数小于元素Y的原子序数,X、Y间形成的常见化合物的分子式可表示为:Y2X 、Y2X2. 则这两种元素的原子序数之和等于
A.16 B .17 C. 18 D. 19
14.某溶液中有:①Cu2+、②NH4+、③Fe2+、④Al3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再向其中加入过量盐酸,溶液中大量减少的阳离子是
A.①② B.②③ C.③④ D.①④
15.X、Y、Z是3种短周期元素,其中X、Y位于同一主族,Y、Z处于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法正确的是
A.元素非金属性由弱到强的顺序为Z<Y<X
B.Y元素最高价氧化物对应水化物的化学式可表示为H3YO4
C.3种元素的气态氢化物中,Z的气态氢化物最稳定
D.原子半径由大到小的顺序为Z<Y<X
第Ⅱ卷(非选择题,共55分)
16.(8分)
(1)比较原子半径的大小(填“>”或“<”,下同):O F;K+ Ca2+。
(2)比较酸性强弱: H3PO4 H2SiO3(3)稳定性:NH3 ________ PH3
17.(12分)除去下列物质中的杂质,根据要求填空:
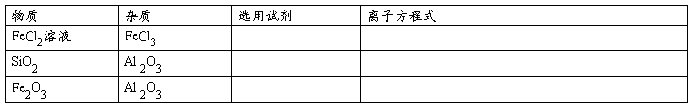
18.(14分)A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A为 ,B为 ,C为 。D的最高价氧化物的水化物是 。
(2)写出A、B的化合物与E反应的化学方程式:
。
(3)A、B两元素形成化合物属 (填“离子”或“共价”)化合物。
(4)写出D的最高价氧化物的水化物和A反应的化学方程式:
。
19.(12分)某混合物A含有KAl (SO4)2、Al2O3和Fe2O3,在一定条件下可实现下列物质之间的变化:
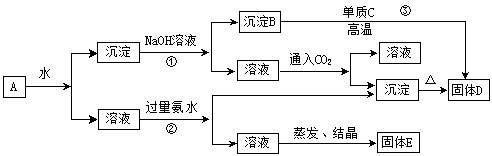
据此判断:
(1)固体E所含物质的化学式为 。
(2)反应③的化学方程式为 。
(3)反应①的离子方程式为 。
(4)反应②的离子方程式为 。
20. (5分)铝镁合金已成为飞机制造、化工生产等行业的重要材料。研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列实验方案进行探究。填写下列空白。
〖实验方案〗准确称取质量的铝镁合金,与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃,1.01 105Pa)的体积,再转换成标准状况下的体积,通过计算得知镁的质量分数。
105Pa)的体积,再转换成标准状况下的体积,通过计算得知镁的质量分数。
同学们拟选用下列实验装置完成实验:
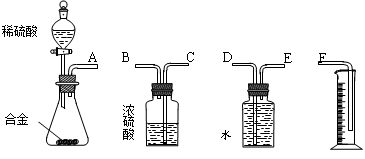
(1)你认为最简易的装置其连接顺序是: (用接口字母表示)
(2)实验结束时,在读取测量实验中生成氢气的体积时,你认为合理的是 。
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.视线与凹液面的最低点水平,读取量筒中水的体积
21.(4分)有一根粗铝条含铁和硅两种杂质。取等质量的样品分别投入足量的稀盐酸和足量的稀氢氧化钠溶液中,放出等量的H2(提示:硅能与强碱反应生产硅酸盐和氢气),求该粗铝中铁和硅的质量比 。
化学试题参考答案及评分标准
第Ⅰ卷(选择题 共45分)
选择题(本题包括15小题,每题3分,共45分。每小题只有一个选项符合题意)
1.D 2.B 3 .B 4.C 5.C 6.A 7.B 8.B 9.C 10.A
11.A 12.D 13.B 14.B 15.A
第Ⅱ卷(非选择题 共55分)
16. (8分 每空2分) (1) > > (2) > <
17.(12分 每空2分)铁粉 : Fe +2 Fe3+ =3Fe2+;盐酸 :Al 2O3+ 6H+ = 2Al3+ + 3 H2O ;
NaOH溶液: Al 2O3+2OH- +3 H2O=2 [Ai(OH)4]-
18.(14分 每空2分)
(1)C(碳),O(氧),Na(钠),H2SO4 (硫酸)
(2)2Na2O2+CO2=2Na2CO3+O2
(3)共价
(4)C+2H2SO4(浓)  CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
19.(12分 每空2分)(1)K2SO4(2分)、(NH4)2SO4 (1分)
(2)2Al+Fe2O3 2Fe+Al2O3 (3)Al2O3+2OH-+3H2O=2[Al(OH)4]-
2Fe+Al2O3 (3)Al2O3+2OH-+3H2O=2[Al(OH)4]-
(4)Al3++3NH3·H2O=Al(OH)3↓+3NH4+
20(5分)(1)A、ED、F (2分)(2)A、B、C
21(4分)4∶1
