硫酸铜的制备及产品质量分析
一、实验目的
1.了解硫酸铜的制备原理和用重结晶法提纯物质的基本原理。
2.掌握加热、溶解、蒸发浓缩、结晶、常压过滤、减压过滤等基本操作技术。
3.掌握天平、电炉和研钵的操作。
二、实验原理
(一)硫酸铜的制备
铜是不活泼金属,不能直接和稀硫酸发生反应制备硫酸铜,必须加入氧化剂。在浓硝酸和稀硫酸的混合液中,浓硝酸将铜氧化成Cu2+,Cu2+与SO42-结合得到硫酸铜 :
Cu + 2HNO3 + H2SO4 == == CuSO4 + 2NO2 + 2H2O
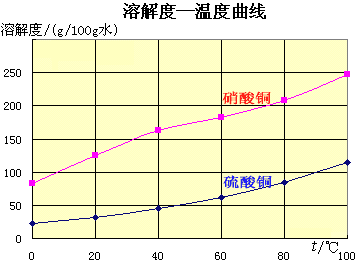
未反应的铜屑(不溶性杂质)用倾滗法除去。利用硝酸铜的溶解度在0~100℃范围内均大于硫酸铜溶解度的性质,溶液经蒸发浓缩析出硫酸铜,经过滤与可溶性杂质硝酸铜分离,得到粗产品。
硫酸铜的溶解度随温度升高而增大,可用重结晶法提纯。在粗产品硫酸铜中,加适量水,加热成饱和溶液,趁热过滤除去不溶性杂质。滤液冷却,析出硫酸铜,过滤,与可溶性杂质分离,得到纯的硫酸铜。

(二)硫酸铜的提纯
硫酸铜为可溶性晶体物质。根据物质的溶解度的不同,可溶性晶体物质中的杂质包括难溶于水的杂质和易溶于水的杂质。一般可先用溶解、过滤的方法,除去可溶性晶体物质中所含的难溶于水的杂质;然后再用重结晶法使可溶性晶体物质中的易溶于水的杂质分离。
重结晶的原理是由于晶体物质的溶解度一般随温度的降低而减小,当热的饱和溶液冷却时,待提纯的物质首先结晶析出而少量杂质由于尚未达到饱和,仍留在母液中。
粗硫酸铜晶体中的杂质通常以硫酸亚铁(FeSO4)、硫酸铁[Fe2(SO4) 3]为最多。当蒸发浓缩硫酸铜溶液时,亚铁盐易氧化为铁盐,而铁盐易水解,有可能生成Fe(OH) 3 沉淀,混杂于析出的硫酸铜晶体中,所以在蒸发浓缩的过程中,溶液应保持酸性。
若亚铁盐或铁盐含量较多,可先用过氧化氢(H2O2)将 Fe2+氧化为 Fe3+,再调节溶液的pH值约至4,使Fe3+水解为Fe(OH) 3沉淀过滤而除去。
pH≈4
2Fe2+ + H2O2 + 2H+ = 2Fe3+ + 2H2O Fe3+ + 3H2O = Fe(OH)3 + 3H+
三、仪器和试剂
1.仪器 天平(公用)、烧杯(50rnL)1只、烧杯(100rnL)1只、10mL量筒1只、石棉网1个、玻棒、电炉1个、漏斗1个、漏斗架1个、表面皿1只、蒸发皿1只、泥三角1只、塑料洗瓶1只、布氏漏斗1只、抽滤装置1套、滴管3支、硫酸铜回收瓶。
2. 试剂及材料 铜屑3g、H2SO4(3 rnol·L-1)20mL、浓HNO310mL、H2O2(3%)10mL、NaOH(0.5 mol·L-1)10mL、pH试纸、6mol/L氨水10mL、去离子水500mL、2mol/L KCNS 2mL、滤纸3张、CuSO4·5H2O标样(分析纯、化学纯各1g)。
四、实验步骤
(一)硫酸铜的制备
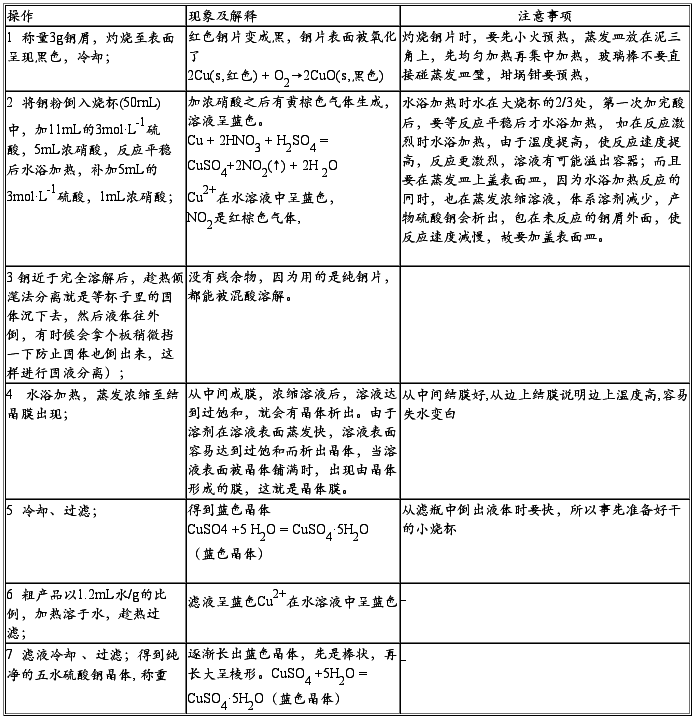
(二)称量和溶解
用台秤称取粗硫酸铜4g,放入洁净的100mL烧杯中,加入纯水20mL。然后将烧杯置于石棉网上加热,并用玻棒搅拌。当硫酸铜完全溶解时,立即停止加热。大块的硫酸铜晶体应先在研钵中研细。每次研磨的量不宜过多。研磨时,不得用研棒敲击,应慢慢转动研棒,轻压晶体成细粉末。
(三)沉淀
往溶液中加入3%H2O2溶液10滴,加热,逐滴加入 0.5mol·L-1NaOH溶液直到 pH=4(用pH试纸检验),再加热片刻,放置,使红棕色 Fe(OH) 3沉降。用pH试纸(或石蕊试纸)检验溶液的酸碱性时,应将小块试纸放入干燥清洁的表面皿上,然后用玻璃棒蘸取待检验溶液点在试纸上,切忌将试纸投入溶液中检验。
(四)过滤
将折好的滤纸放入漏斗中,用洗瓶挤出少量水润湿滤纸,使之紧贴在漏斗壁上。将漏斗放在漏斗架上,趁热过滤硫酸铜溶液,滤液承受在清洁的蒸发皿中。从洗瓶中挤出少量水洗涤烧杯及玻璃棒,洗涤水也应全部滤入蒸发皿中。过滤后的滤纸及残渣投入废液缸中。
(五)蒸发和结晶
在滤液中滴入2滴1mol·L-1H2SO4溶液,使溶液酸化,然后放在石棉网上加热,蒸发浓缩(切勿加热过猛以免液体溅失)。当溶液表面刚出现一层极薄的晶膜时,停止加热。静置冷却至室温,使CuSO4·5H2O充分结晶析出。
(六)减压过滤
将蒸发皿中CuSO4·5H2O晶体用玻棒全部转移到布氏漏斗中,抽气减压过滤,尽量抽干,并用干净的玻棒轻轻挤压布氏漏斗上的晶体,尽可能除去晶体间夹的母液。停止抽气过滤,将晶体转到已备好的干净滤纸上,再用滤纸尽量吸干母液,然后将晶体用台秤称量,计算产率。晶体倒入硫酸铜回收瓶中。
(七)产品纯度检定
(1)称取1g提纯后的CuSO4·5H2O晶体放入100ml小烧杯中,用100ml去离子水溶解。加入1mL稀硫酸酸化,再加入3%的H2O2 2mL 煮沸片刻使Fe2+氧化成 Fe3+ 。
(2)将溶液冷却后在搅拌下逐滴加入6mol/L氨水(约8mL),直到最初生成的沉淀完全溶解且溶液呈深蓝色为止。此时Fe3+转化为Fe(OH)3沉淀。而 Cu2+ 转化为[Cu(NH3)4]2+;
Fe3++3NH3+3H2O → Fe(OH)3 ↓ +3NH4+
2CuSO4+2NH3+2H2O → Cu2(OH)2SO4 ↓(蓝) + (NH4)2SO4
Cu2(OH)2SO4 +(NH4)2SO4 + 6NH3 → 2[Cu(NH3)4]SO4 +2H2O
(3)用普通漏斗过滤,并用滴管将 2mol/L 氨水滴到滤纸上,直到蓝色洗去为止,弃去滤液,此时Fe(OH)3棕黄色沉淀留在滤纸上。
(4)有滴管把3mL热的 2mol/L HNO3 (或盐酸)滴到滤纸上以溶解 Fe(OH)3 沉淀。如果一次不能完全溶解,可将滤液加热,再滴到滤纸上,滤液可流入25mL 比色管中。
(5)在滤液中滴入2mol/L KCNS,观察血红色溶液产生。
Fe3+ + nCNS- → [Fe(CNS)n]3-n
Fe3+越多,血红色越深,因此可以根据血红色的深浅,比较Fe3+ 的多少,将血红色溶液与标准系列溶液比较,确定产品相当试剂几级(一般化学试剂的品级:一级试剂、二级试剂、三级试剂、四级试剂。国内标准名称:优级纯(保证试剂)、分析纯、化学纯 、实验试剂。)。
五、结果记录
产品色泽外观:
理论产量: g
提纯后的实际产量: g
产率:
纯度检验结果:
六、思考题
1.用重结晶法提纯硫酸铜,在蒸发滤液时,为什么加热不可过猛?为什么不可将滤液蒸干?
2.为了提高提纯精制硫酸铜的产率,实验过程中应注意哪些问题?
第二篇:硫酸铜的制备
一、 实验目的
1. 练习托盘天平的使用,蒸发浓缩,减压过滤,重结晶等基本操作。
2. 了解由金属制备它的某些盐的方法,弄清重结晶提纯物质的原理。
实验原理
纯铜属不活泼金属,不能溶于非氧化性的酸中,但其氧化物在酸中却溶解,因此在工业上制备胆矾(硫酸铜)时,先把铜烧成氧化铜。然后与适当浓度的硫酸反应而生成硫酸铜,本实验采用的浓硝酸作氧化剂,以废铜屑与硫酸、浓硝酸反应来制备硫酸铜,反应式为:
Cu +2HNO3 +H2SO4=CuSO4 + 2NO2 + 2H2O
产物中除硫酸铜外,还含有一定量的硝酸铜和一些可溶性或不溶性的杂质,不溶性杂质可过滤除去,而硝酸铜则利用它和硫酸铜在水中溶解度的不同,通过结晶的方法将其除去(留在母液中)。
表6-1硫酸铜和硝酸铜在水中的溶解度(g/100 g水)
CuSO4·5H2O
Cu(NO3)·6H2O
Cu(NO3)·3H2O 0 ℃ 23.3 81.8 20 ℃ 32.3 125.1 40 ℃ 46.2 ~160 60 ℃ 61.1 ~178.5 80 ℃ 83.8 ~208 由表6-1中数据可知,硝酸铜在水中的溶解度不论在高温或低温下都比硫酸铜大得多,在本实验所得的产物中它的量又小,因此,当热的溶液冷却到一定温度时硫酸铜首先达到过饱和而硝酸铜却远远没有达到饱和,随着温度的继续下降,硫酸铜不断从溶液中析出,硝酸铜则绝大部分的留在溶液中,有小部分作为杂质伴随硫酸铜出来的硝酸铜可以和其它一些可溶性杂质一起,通过重结晶的方法除去,最后达到制得纯硫酸铜的目的。
主要用品
仪器:蒸发皿(烧杯100 mL),布氏漏斗,吸滤瓶,量筒(100 mL,10 mL);
药品:H2SO4(3 mol·L-1),浓HNO3,废铜屑。
实验部分
1. 称取2.5 g剪细的铜屑,将它置于干燥的蒸发皿中,用酒精喷灯强热灼热,至不再产生白烟为止(目的在于除去附着在铜屑上的油污),放冷。
2. 往上述盛有铜屑的蒸发皿中加入8 mL,3 mol·L-1H2SO4,然后缓慢的分次加入3.5 mL浓硝酸(反应过程产生大量有毒的二氧化氮气体,操作应在通风橱中进行),待反应缓和后,
-1盖上表面皿,放在水浴上加热,加热过程需要补加4 mL,3 mol·LH2SO4和1 mL浓HNO3
(由于反应情况不同,补加的酸量要根据具体反应情况而定,在保持反应继续顺利进行的情况下,尽量少加硝酸)待铜屑近于全部溶解,趁热用倾析法将溶液转入一个小烧杯(或直接转入另一瓷蒸发皿中,如果仍有一些不溶性残渣,可用少量3 mol·L-1H2SO4洗涤后弃去,洗涤液合并与小烧杯中,随后再将硫酸铜溶液转入洗净的蒸发皿中,在水浴上加热浓缩至表面有晶膜出现为止,取下蒸发皿,置于冷水上冷却,即有蓝色粗的五水硫酸铜晶体析出,冷却至室温抽滤,称重,计算产率。
3. 将粗产品以每克加1.2 mL水的比,溶于蒸馏水中加热使其完全溶解并趁热过滤,滤液收集在一个小烧杯中,让其慢慢冷却,即有晶体析出(如无晶体析出,可在水溶液上再加热蒸发,稍微浓缩)冷却后,用抽滤法除去母液,晶体干燥后,再放在二层滤纸间进一步挤压吸干,然后将产品放在表面皿上称重,计算收率,母液回收。
问题讨论
1. 在托盘天平上称量时必须注意哪几点?什么叫零点和停点。
2. 什么情况下可使用倾析法?什么情况下使用常压过滤或者滤压过滤?
3. 在减压过滤操作中如果(1)未开自来水开关之前把沉淀转入布氏漏斗内,(2)结束时先关上自来水开关,各会产生何种影响?
蒸发浓缩CuSO4的水溶液时,为什么要水浴加热?
