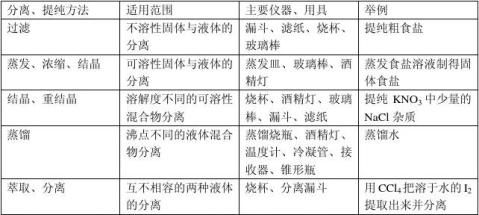
混合物分离与提纯
物质的分离是把混合物中各物质经过物理(化学)变化,将其彼此分开的过程,分开后各物
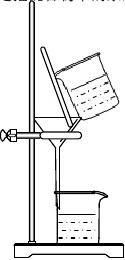
1、 过滤
过滤操作注意事项:“一贴、二低、三接触”,如图 ①“一贴”:折叠后的滤纸放入漏斗后,用食指按住,加入少量蒸馏水润湿,使之紧贴在漏斗内壁,赶走纸和壁之间的气泡。 ②“二低”:滤纸边缘应略低于漏斗边缘;加入漏斗中液体的液面应略低于滤纸的边缘(略低约1cm),防止未过滤的液体溢出。
③“三接触”漏斗颈末端与接滤液的烧杯内壁接触,使滤液沿烧杯内壁流下;向漏斗中倾倒液体时,玻璃棒一端要与三层滤纸的部分接触;盛放待过滤液体烧杯嘴和玻璃棒接触,使待过滤的液体在玻璃棒的引流下流入漏斗。
④其他:滤液浑浊应重新过滤; 滤液对滤纸有腐蚀性,可用石棉或玻璃丝代替滤纸;如果过滤的目的是要得到洁净的沉淀物,要对沉淀物进行洗涤,具体操作(向漏斗里加入适量蒸馏水,水面浸没沉淀物,待水滤去后,再加水洗涤,连续几次,直至沉淀物洗净为止。取滤液用检验离子的方法可知道是否洗净。) 2、 蒸馏
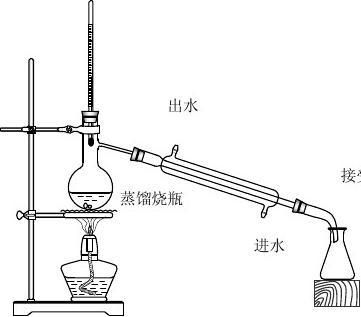
蒸馏操作注意事项:如图
①蒸馏烧瓶中液体不能超过容积的2/3,也不能少于1/3;
②温度计水银球下端要与烧瓶支口下端相奇;
③冷凝管中冷凝水,下口进,上口出;
④蒸馏瓶中要加入少量碎瓷片,防止暴沸;
⑤蒸馏瓶、冷凝管、牛角管接口处用橡皮塞穿过,防止溜出液混入杂质;
⑥加热温度不能超过混合物中沸点最高物质的沸点。
3、 蒸发
注意事项:蒸发皿的溶液不能超过其容积的三分之二;加热过程中要不断搅拌,以免局部温度过高溶液溅出;如果蒸干,当析出大量晶体时就应熄灭酒精灯,利用余热蒸干。
【蒸馏与蒸发的区别】
加热是为了获得溶液的残留物(浓缩后的溶液或蒸干后的固体物质)时,要用蒸发;为了收集蒸气的冷凝液体时,就用蒸馏。
4、萃取
萃取操作方法:
①用普通漏斗把待萃取液注入分液漏斗,再注入足量萃取液;
②用右手压住上口玻璃塞,左手握住活塞,反复倒转漏斗并用力振荡,
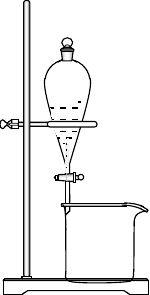
是溶质充分转移到萃
取剂中。振荡过程中并在活塞处放气。
③将分液漏斗置于铁架台的铁环上静置,待分层后分液;
④蒸发萃取剂就可得到纯净的溶质。为把溶质分离干净,一般需多次萃取。
分液操作方法:
①用普通漏斗把待分离液注入分液漏斗,盖好玻璃塞,让玻璃塞上的凹槽与瓶口上的小孔对齐(内外大气压一致,利于分层)。
②将分液漏斗置于铁架台的铁圈上,静置,分层。
③打开活塞,使下层液体慢慢流出,放入烧杯,待下层液体流完立即关闭活塞,注意不可使上层液体流出;
④从漏斗上端口倒出上层液体。
总结:化学方法提纯和分离物质的“四原则”和“三必须”
“四原则”一不增(提纯过程中不增加新物质);二不减(不减少欲被提纯的物质);三易分离(被提纯物与杂志易分离);四易复原(被提纯物质易复原)。
“三必须”除杂试剂必须过量;过量试剂必须除尽;除杂途径必须最佳。
第二篇:混合物的分离提纯及物质的鉴别方法总结
混合物的分离提纯及物质的鉴别方法总结
(一)、复习目标
⒈掌握将混合物分开并恢复至原状态的方法。
⒉掌握任选试剂或不用外加试剂鉴别物质的 方法。
(二)、方法指导:
A 混合物的分离提纯
⒈固体与固体混和物,若杂质易分解,易升华时用加热法;若一种易溶,另一种难溶,可用溶解过滤法;若二
者均易溶,但其溶解度受温度的影响不同,用重结晶法。
⒉液体与液体混和物,若沸点相差较大时,用分馏法;若互不混溶时,用分液法;若在溶剂中的溶解度不
同时,用萃取法。
⒊气体与气体混和物:一般可用洗气法。
⒋若不具备上述条件的混和物,可先选用化学方法处理,待符合上述条件时,再选用适当的方法。
该类题目的主要特点有三个:一是选取适当的试剂及分离的方法除去被提纯物中指定含有的杂质;二
是确定除去被提纯物质中多种杂质时所需加入试剂的先后顺序。三是将分离提纯与物质的制备,混和物成
分的确定等内容融为一体,形成综合实验题。
B 物质的鉴别
⒈不用任何外加试剂鉴别多种物质主要有如下四种形式:
⑴顺序型:通过观察,加热焰色反应或两两混合等方法,先确定某种物质,再用这种物质作为试剂,
依次鉴别本组内各物质。
⑵一次型:用某种方法鉴别出一种物质后,这种物质能与其它几种物质分别反应呈现不同的现象,一
次性地鉴别本组物质。
⑶分组型:用某方法将原物质组分成若干组(如现象不同),再对各小组内物质进行鉴别。
⑷综合型:以上几种类型的组合。
⒉任选试剂鉴别多种物质的题目往往以简答题的形式出现,回答时要掌握以下要领:
⑴选取试剂要最佳:选取的试剂对待检物质组中的各物质反应现象要有明显差异。
⑵不许原瓶操作。
⑶不许“指名道姓”:结论的得出来自实验现象,在加入试剂之前,该物质是未知的,叙述时不可出
现取某某物质加入某某试剂……的字样,一般简答顺序为:各取少许→溶解→加入试剂→描述现象→得出
结论。
