第一章 化学反应与能量
《绪言 》总结与练习
班级 姓名 编写:黄蒲生
[要点总结]
1、 有效碰撞模型:
(1)反应物之间如果发生反应,反应物分子之间必须碰撞。(必要条件)
(2)但每次碰撞并不一定都发生反应。
(3)有效碰撞:碰撞并发生了反应。
2、活化分子与活化能:
(1)活化分子:
(2)活化能:
3、提高活化分子含量的方法:
(1)
(2)
4、已知:2H2 (g)+ O2 (g) = 2H2O(g),反应过程中能量变化如图所示,请回答下列问题。
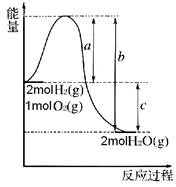
(1)(1)a、b、c分别代表什么意义?
a: ;
b: ;
c: 。
(2)该反应是________________反应(填“放热”或“吸热”)
[补充练习]
1、(2011上海)据报道,科学家开发出了利用太阳能分解水的新型催化剂。下列有关水分解过程的能量变化示意图正确的是 ( )
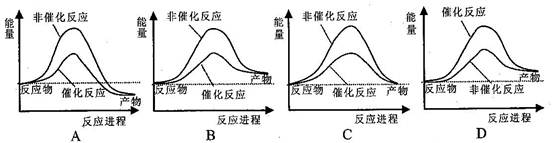
2、下列说法正确的是 ( )
A.需要加热才能发生的反应一定是吸热反应
B.化学反应中的能量变化都表现为热量变化
C.任何放热反应在常温下一定能发生反应
D.反应物和生成物所具有的总能量决定了反应是放热还是吸热
3、氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏1 mol氢气中的化学键消耗的能量为Q1 kJ,破坏1 mol氯气中的化学键消耗的能量为Q2 kJ,形成1 mol氯化氢中的化学键释放的能量为Q3 kJ。下列关系式中,正确的是 ( )
A.Q1+Q2>Q3 B.Q1+Q2>2Q3 C.Q1+Q2<Q3 D.Q1+Q2<2Q3
4、下列过程一定释放出能量的是 ( )
A.化合反应 B.分解反应 C.分子拆成原子 D.原子组成分子
5、下列说法正确的是 ( )
A.电解熔融的Al2O3可以制得金属铝和氧气,该反应是一个放出能量的反应
B.水分解产生氢气和氧气时放出能量
C.相同状况下,己知反应2SO2+O2=2SO3是一个放热反应,则反应2SO3=2SO2+O2是一个吸热反应
D.氯化氢分解成氢气和氯气时会放出能量
6、下列反应属于吸热反应的是 ( )
A.稀硫酸和氢氧化钾溶液反应 B.碳与水气高温下反应制水煤气
C.锌与稀硫酸的反应 D.生石灰变成熟石灰的反应
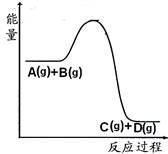 7、反应A(g)+B(g)
7、反应A(g)+B(g) C(g) +D(g)过程中的能量变化
C(g) +D(g)过程中的能量变化
如图所示,下列说法正确是 ( )
A.该反应是吸热反应
B.当反应达到平衡时,升高温度,A的转化率减小
C.反应体系中加入催化剂对反应热有影响
D.在反应体系中加入催化剂,反应速率增大,A的转化也增大
8、根据化学反应的实质是旧键断裂新键形成这一事实,下列变化属于化学变化的(双选) ( )
A.氧气转化成臭氧(O3) B.石墨在高温下转化为金刚石
C.液态水变为水蒸气 D.干冰熔化
9、下列物质加入水中显著放热的是 (双选) ( )
A.固体NaOH B.生石灰 C.无水乙醇 D.固体NH4NO3
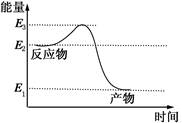 10、某反应过程中的能量变化如图所示,该反应的活化能为 ( )
10、某反应过程中的能量变化如图所示,该反应的活化能为 ( )
A.E2 B.E2-E1
C.E3-E2 D.E3
第二篇:化学选修4第一章第一节练习
第一节 化学反应与能量测试题(基础)
1.物质之间发生化学反应时,一定发生变化的是( )
A.颜色 B.状态 C.化学键 D.原子核
2.下列过程一定释放出能量的是 ( )
A.化合反应 B.分解反应
C.分子拆成原子 D.原子组成分子
3.我们把拆开1 mol 共价键所吸收的能量或生成1 mol共价键所放出的能量叫键能,
-1已知Cl—Cl键的键能为247 kJ·mol。下列有关键能的叙述正确的是 ( )
A.要拆开1 mol Cl—Cl键需吸收247 kJ能量
B.要形成1 mol Cl—Cl键需吸收247 kJ能量
C.要拆开1 mol Cl—Cl键需放出247 kJ能量
D.要形成1 mol Cl—Cl键需放出247 kJ能量
4

.“摇摇冰”是一种即用即冷的饮料。吸食时,将饮料罐隔离层中的化学物质和水混
6.石墨和金刚石都是碳元素的单质,石墨在一定条件下可转化为金刚石。已知12 g石墨完全转化成金刚石时,要吸收E kJ的能量,下列说法正确的是( )
A.石墨不如金刚石稳定
B.金刚石不如石墨稳定
C.等质量的石墨与金刚石完全燃烧,金刚石放出的能量多
D.等质量的石墨与金刚石完全燃烧,石墨放出的能量多
7.在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,下列热化学方程式正确的是( )
A. CH3OH(l)+3-1O2(g) →CO2(g)+2H2O(l) ;ΔH=+725.8 kJ·mol 2
-1B. 2CH3OH(l)+3O2(g) →2CO2(g)+4H2O(l) ;ΔH=-1 452 kJ·mol
-1C. 2CH3OH(l)+3O2(g) →2CO2(g)+4H2O(l) ;ΔH=-725.8 kJ·mol
-1D. 2CH3OH(l)+3O2(g) →2CO2(g)+4H2O(l) ; ΔH=+1 452 kJ·mol
8、下列说法正确的是 ( )
A.需要加热方能发生的反应一定是吸热反应
B.放热的反应在常温下一定很易发生
C.反应是放热的还是吸热的必须看反应物和生成物所具有的总能量的相对大小
D.吸热反应在一定的条件下也能发生
9、已知在25 ℃、101 kPa下,1 g C8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40 kJ的热量。表示上述反应的热化学方程式正确的是( )
25-1O2(g) →8CO2(g)+9H2O(g) ;ΔH=-48.40 kJ·mol 2
25-1B. C8H18(l)+O2(g) →8CO2(g)+9H2O(l) ;ΔH=-5 518 kJ·mol 2
25-1C. C8H18(l)+ O2(g) →8CO2(g)+9H2O ;ΔH=+5 518 kJ·mol 2
25-1D. C8H18(l)+ O2(g) →8CO2(g)+9H2O(l) ;ΔH=-48.40 kJ·mol 2A. C8H18(l)+
10、在同温同压下,下列各组热化学方程式中,ΔH1>ΔH2的是( )
A.2H2(g)+O2(g)===2H2O(g) ;ΔH1
2H2(g)+O2(g)===2H2O(l) ;ΔH2
B. S(g)+O2(g)===SO2(g) ;ΔH1
S(s)+O2(g)===SO2(g) ;ΔH2
C. C(s)+1O2(g)===CO(g) ;ΔH1 2
C(s)+O2(g)=== CO2(g) ;ΔH2
D. H2(g)+Cl2(g)===2HCl(g) ;ΔH1
11H2(g)+Cl2(g)===HCl(g) ;ΔH2 22
11.以NA代表阿伏加德罗常数,则关于热化学方程式C2H2(g)+
-15O2(g) →22CO2(g)+H2O(l) ;ΔH=-1 300 kJ·mol的说法中,正确的是 ( )
A.当10NA个电子转移时,该反应放出1 300 kJ的能量
B.当1NA个水分子生成且为液体时,吸收1 300 kJ的能量
C.当2NA个碳氧共用电子对生成时,放出1 300 kJ的能量
D.当8NA个碳氧共用电子对生成时,放出1 300 kJ的能量
12.一些盐的结晶水合物,在温度不太高时就有熔化现象,即熔溶于自身的结晶水中,又同时吸收热量。它们在塑料袋中经日晒就熔化,又在日落后缓慢凝结而释放热量。故可用于调节室内温度,或用作夏日防暑的枕垫或坐垫,这些物质可称之为热材料。现有几种盐的
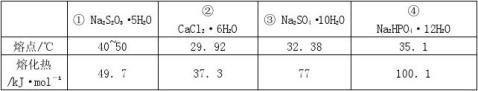
根据上述数据和实用性考虑,实际应用时常采用的物质应该是
A.① B.② C.③ D.④
13、1 g炭与适量水蒸气反应生成一氧化碳和氢气,需吸收10.94 kJ的热量,相应的热化学方程式为 ( )
A.C+H2O=CO+H2 ΔH=+10.9 kJ/ mol
B.C(s)+H2O(g)=CO(g)+H2(g) ΔH=+10.94 kJ/ mol
C.C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.28 kJ/ mol
D.1/2C(s)+ 1/2H2O(g)= 1/2CO(g)+ 1/2H2(g ) ΔH=+65.64 kJ/ mol
14.已知1mol白磷转化成1mol红磷,放出18.39 kJ热量,又知:P4(白,s)+5O2 = 2P2O5(s)
ΔH1,4P(红,s)+5O2 = 2P2O5 (s)ΔH2
则ΔH1和ΔH2的关系正确的是( )
A.ΔH1>ΔH2 B.ΔH1<ΔH2
C.ΔH1=ΔH2 D.无法确定
15、 今有如下三个热化学方程式:
H2(g)+1/2O2(g)=H2O(g) ΔH=a kJ/ mol
H2(g)+1/2O2(g)=H2O(l) ΔH=b kJ/ mol
2H2(g)+ O2(g)=2H2O(l) ΔH=c kJ/ mol
关于它们的下列表述正确的是 ( )
A.它们都是吸热反应 B.a、b和c均为正值
C.a=b D.2b=c
16.298 K、101 kPa时,合成氨反应的热化学方程式为N2(g)+3H2(g)2NH3(g);
-1ΔH=-92.38 kJ·mol。在该温度下,取1 mol N2(g)和3 mol H2(g)放在一密闭容器中,
在催化剂存在情况下进行反应,测得反应放出的热量总是少于92.38 kJ,其原因是什么?
17.家用液化气中的主要成分之一是丁烷,当10 kg丁烷完全燃烧并生成二氧化碳和液
5态水时,放出热量为5×10kJ,试写出丁烷燃烧反应的热化学方程式_______________。
已知1 mol液态水汽化时需要吸收44 kJ的热量,则1 mol丁烷完全燃烧并生成气态水时放出的热量为______kJ。
答案:1、C 2、D 3、AD 4、B 5、D 6、BC 7、B
8、C 9、B 10、AD 11、AD 12、D 13、CD 14、 A 15、D
16、该反应是可逆反应,在密闭容器中进行该反应将达到平衡状态, 1 mol N2(g)和3 mol H2(g)不能完全反应生成2 mol NH3(g),因而放出的热量总小于92.38kJ
17、2C4H10(g)+13O2(g)===8CO2(g)+10H2O(l)+5800 kJ[或C4H10(g)+ O2(g)===4CO2(g)+5H2O(l)+2900 kJ] 2680
