�ڶ�����ĩ��ҵ
�ڶ�����ĩ��ҵ
�༶ ���� ��д:������
1����ѧ������������ɳ�����չ������ء����д�ʩ�����ڽ��ܼ��š������������ǣ� ��
�ټӿ컯ʯȼ�ϵĿ�����ʹ�ã� ���з����������ũҩ����Ӧ�ø�Ч�ྻ����Դת���������������սոѣ����ƹ�ʹ�ý��ܻ������ϡ�
A���٢ۢ� B���ڢۢ� C���٢ڢ� D���ڢܢ�
2������˵����ȷ���� �� ��
A.��Ҫ���ȵĻ�ѧ��Ӧ�������ȷ�Ӧ B.�кͷ�Ӧ���Ƿ��ȷ�Ӧ
C.ԭ����ǽ�����ת��Ϊ��ѧ�ܵ�һ��װ�� D.ˮ�������ǽ���ѧ��ת��Ϊ���ܵĹ���
3�������뻯ѧ��Ӧ�����仯��ص���������ȷ���� �� ��
A����֪CH4(g)��2O2(g)=CO2(g)��2H2O(g) ��H��-802 kJ/mol�������ȼ����Ϊ802 kJ/mol
B������H2��O2����ȫȼ�գ�����H2O(g)������H2O(l)�ų���������
C��ͬ��ͬѹ�£�H2(g)��Cl2(g)=2HCl(g)�ڹ��պ͵�ȼ�����µĦ�H��ͬ
D����ʯī�Ƚ��ʯ�ȶ���֪��C(���ʯ, s)=C(ʯī, s) ��H<0
4������˵����ȷ���� �� ��
A��ij��Ӧ������������ʴ��ڷ�Ӧ�������ʱ����Ӧ���ȣ���H��0
B����ѧ��Ӧ�����У��������ʱ仯��ͬʱ��һ�����������仯
C��SO2������ˮ��������Һ�ܵ��磬����SO2�ǵ����
D������ij��Ӧ�ķ�Ӧ�ȿ���������ļ����ܺͼ�ȥ��Ӧ��ļ����ܺ�
5�������й��Ȼ�ѧ����ʽ�������У���ȷ���� ( )
A����20.0 g NaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7 kJ�����������ʾ�÷�Ӧ�к��ȵ���
��ѧ����ʽΪ NaOH(aq)��HCl(aq) = NaCl(aq)��H2O(l) ��H����57.4 kJ/mol
B����֪C(ʯī��s) = C(���ʯ��s) ��H��0������ʯ��ʯī�ȶ�
C����֪2H2(g)��O2(g) =2H2O(g) ��H����483.6 kJ/mol����H2ȼ����Ϊ241.8 kJ/mol
D����֪2C(s)��2O2(g) ==2CO2(g) ��H1,��2C(s)��O2(g) = 2CO(g) ��H2����H1����H2
6��֪��2CO��g��+O2(g)=2CO2(g) ��H = ��566 kJ/mol
Na2O2(s)+CO2(g) = Na2CO3(s)+1/2 O2(g) ��H=��226 kJ/mol
���������Ȼ�ѧ����ʽ�жϣ�����˵����ȷ���� �� ��
A.CO��ȼ����Ϊ283 kJ
B.��ͼ�ɱ�ʾ��CO����CO2�ķ�Ӧ���̺�������ϵ
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) H��-452 kJ/mol
D.CO(g)��Na2O2��s����Ӧ�ų�509 kJ����ʱ������ת����Ϊ6.02��1023
7����֪��Ӧ����101kPaʱ��2C(s) +O2(g)==2CO(g)����H=��221 kJ/mol
��ϡ��Һ�У�H+(aq)+OH��(aq)==H2O(l)����H=��57.3 kJ/mol�����н�����ȷ���� �� ��
A��̼��ȼ����С��110.5 kJ/mol
B���ٵķ�Ӧ��Ϊ221 kJ/mol
��1ҳ
�ڶ�����ĩ��ҵ
C��ϡ������ϡNaOH��Һ��Ӧ���к���Ϊ-57.3 kJ/mol
D��ϡ������ϡNaOH��Һ��Ӧ����1 molˮ���ų�������С��57.3 kJ
8����֪��Ӧ���� 2C(s)��O2(g)��2CO(g) ��H����221 kJ��mol
�� ϡ��Һ�У�H(aq)��OH(aq)��H2O(l) ��H����57.3 kJ��mol
���н�����ȷ����


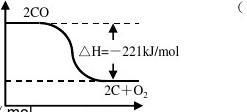
��
����
A��̼��ȼ���ȴ���110.5 kJ��mol
B����ͼ�ɱ�ʾ�ٵķ�Ӧ���̺�������ϵ
C��ϡ������ϡNaOH��Һ��Ӧ���к���Ϊ57.3 kJD��ϡ������ϡNaOH��Һ��Ӧ����1 molˮ���ų�57.3 kJ ������
9���״������͵���������ȼ�ϡ���ҵ�Ͽ�ͨ��H2��CO�����Ʊ��״����÷�Ӧ���Ȼ�ѧ����ʽΪ�� 2H2(g)��CO(g)CH3OH(g) ? 1??116kJ?mol?1H
1?1��1����֪��CO(g)?O2(g)?CO2(g) ?H2??283kJ?mol 2
H2(g)?1O2(g)?H2O(g) ?H3??242kJ?mo1?1 2
1 mol�״�ȼ������CO2��ˮ�����ų� kJ��������
10����ҵ�Ͽ����������ַ�Ӧ�Ʊ��״���
CO(g) + 2H2(g)
CO2(g) �� 3H2(g) CH3OH(g) ��H1 CH3OH(g) + H2O(g) ��H2
��֪��2H2(g)+ O2(g) �� 2H2O(g) ��H3 ��
��2CO(g)��O2(g) �� 2CO2(g) �ķ�Ӧ��
��H����H1����H2����H3��ʾ����
11���ָ�������3���Ȼ�ѧ��Ӧ����ʽ��
Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) ��H1�� �D24.8kJ��mol 3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) ��H2�� �D47.2kJ��mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ��H3�� +640.5kJ��mol
д��CO���廹ԭFeO����õ�Fe�����CO2������Ȼ�ѧ��Ӧ����ʽ��
12��NO2��CO��Ӧ����CO2��NO�����������仯ʾ��ͼ��
��д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ��
��
�ڷ�Ӧ��ϵ�м��������E1��E2�ı仯�ǣ�
E1_________��E2________�����������С�����䡱����
�Է�Ӧ���Ƿ���Ӱ��?_______________��
��2ҳ
�ڶ�ƪ���˽̰滯ѧѡ��4�κ�ǿ����ҵ-3-3-2
������ ������ �ڶ���ʱ

һ��ѡ����(ÿС����1����2��ѡ���������)
������
1����0.1 mol��L1Na2CO3��Һ�У���ʹCO2L1����Ӧ����Һ3��Ũ�Ⱦ����ӽ�0.1 mol���м�
( )
A��HCl B��Na2CO3 C��NaCl D��KOH
��������
�������� ��Na2CO3��Һ�д���ˮ�⣺CO2HCO3��OH��HCO3��3��H2
O
����2��
H2OH2CO3��OH������Һ�м���KOH��������CO23��ˮ�⣬ʹCO3��Ũ�Ⱦ�����
��
��0.1 mol��L1
���𰸡� D
��
2��Ϊ�˳�ȥMgCl2������Һ�е�Fe3�����ڼ��Ƚ���������¼���һ���Լ������˺��ټ���������HCl�������Լ���
( )
A��NH3��H2O B��NaOH C��Na2CO3 D��MgCO3
�������� ���ʳ��ӵ�ԭ���ǣ������ӵ����ʾ�����Ҫ���٣����������µ����ʣ�����
����
���ڷ��븴ԭ������NH3��H2O��NaOH��Na2CO3ʱ������������������NH4��Na����
������
�������⡣��Ϊԭ��Һ��Fe3ˮ�⣺Fe3��3H2OFe(OH)3��3H��������MgCO3����
������
MgCO3��3H��Mg2��CO2����H2O��Ӧ��������H��ʹƽ�������ƶ������ɵ�Fe(OH)3
��
�ڼ��Ƚ��������·����۳������ɽ�Fe3��ȥ������MgO��Mg(OH)2��MgSҲ�ܴﵽͬ����Ч����
���𰸡� D
3����CH3COONa��Һ�и����ӵ�Ũ���ɴ�С����˳����ȷ����
( )
��������
A��c(Na)>c(CH3COO)>c(OH)>c(H)
��������
B��c(CH3COO)>c(Na)>c(OH)>c(H)
��������
C��c(Na)>c(CH3COO)>c(H)>c(OH)
��������
D��c(Na)>c(OH)>c(CH3COO)>c(H)
������
�������� ��CH3COONa��Һ������CH3COO��ˮ�⣬ʹ��c(Na)>c(CH3COO)��
����
��������ˮ�⣬ʹ��Һ�Լ��ԣ���c(OH)>c(H)�������ε�ˮ��̶ȱȽ�С������c(CH3COO����
)>c(OH)����A����ȷ�� ���𰸡� A
������
4����FeCl3��Fe2(SO4)3�Ļ����Һ�У�������Fe3��ˮ�⣬����Һ��c(Fe3)��c(SO24)ʱ�������ж���ȷ����
( )
��3��
A��c(Fe)>c(CI)
����
B��c(SO24)>c(Cl)
����
C��c(SO24)<c(Cl)
D��FeCl3��Fe2(SO4)3�����ʵ������
������3��
�������� ������Һ�е���غ�ɵã�3c(Fe3)��2c(SO24)��c(Cl)������c(Fe)��������2��3��2��
c(SO24)�������c(SO4)��c(Fe)��c(Cl)����A��B��C���������c(SO4)��c(Cl)���ɵ�FeCl3��Fe2(SO4)3�����ʵ�����ȣ���D����ȷ��
���𰸡� D
����
5����0.02 mol��L1CH3COOH��Һ��0.01 mol��L1NaOH��Һ�������ϣ�����Һ��
��Ũ�ȹ�ϵ��ȷ����
( )
A��c(CH3COO)>c(Na)
��B��c(CH3COOH)>c(CH3COO)
����C��2c(H)��c(CH3COO)��c(CH3COOH)
����D��c(CH3COOH)��c(CH3COO)��0.01 mol��L1
�������� CH3COOH��Һ��NaOH��Һ��Ϻ�����Ӧ��CH3COOH��NaOH��CH3COONa��H2O���������ɵ�CH3COONa��ʣ���CH3COOHŨ����ȡ���������
������CH3COOH�ĵ����CH3COO��ˮ�⣬��c(CH3COOH)��c(Na)��c(CH3COO)��������
������CH3COOH�ĵ���̶ȴ���CH3COO��ˮ��̶ȣ�����c(CH3COO)>c(Na)>c(CH3COOH)��
��A����ȷ������̼ԭ���غ㣬��֪D����ȷ��
���𰸡� AD
��6�������Ƕ�Ԫ���ᣬ���������Һ�����ԡ���0.1 mol��L1KHC2O4��Һ�У����й�ϵ
��ȷ����
( )
��������2��A��c(K)��c(H)��c(HC2O4)��c(OH)��c(C2O4)
������B��c(HC2O4)��c(C2O2L1 4)��0.1 mol��
��C��c(C2O24)>c(H2C2O4)
������D��c(K)��c(H2C2O4)��c(HC2O4)��c(C2O24)
���������������� ��KHC2O4��Һ�д�������ƽ�⣺HC2O4H��C2O2HC2O44(����ƽ��)��
������������H2O���H2C2O4��OH(ˮ��ƽ��)������غ��ϵʽΪc(K)��c(H)��c(HC2O4)��c(OH)
����������2c(C2O2���A���������غ��ϵʽΪc(K)��c(H2C2O4)��c(HC2O4)��c(C2O24)��4)��0.1 ��mol��L1�����B����D��ȷ����Һ������˵������̶ȱ�ˮ��̶ȴ����C��ȷ��
���𰸡� CD
7��Ҫ�����ʵ��֤����ij���ε�ˮ�������ȵġ�����λͬѧ�ֱ�������·��������в���ȷ����
( )
A����ͬѧ��������茶�������ˮ����ˮ���½���˵�������ˮ�������ȵ�
����B����ͬѧ���ü��ȵķ����ɳ�ȥKNO3��Һ�л��е�Fe3��˵����Fe3����ˮ������
�ȵ�
C����ͬѧ��ͨ��ʵ�鷢��ͬŨ�ȵ��ȵĴ�����Һ����Ĵ�����Һȥ����Ч���ã�˵��̼����ˮ�������ȵ�
D����ͬѧ���ڴ�������Һ�е����̪��Һ������(������ˮ����)������ɫ���˵��������ˮ�������ȵ�
�������� ���⿼�����ʵ����������֤����ˮ�������ȵģ���������ˮ��ƽ���ƶ�ԭ���������ܸ�������Һ������жϡ�A����������ˮ���¶��½���˵����Ӧ�������ͣ����������ߣ�������֤�������ˮ�������Ȼ���ȡ�B�����ز�ˮ�⣬������ˮ�⣬��
��������ת��������������Fe3��3H2OFe(OH)3��3HCl�������ܳ�ȥ��˵������ˮ��ƽ��
���������������ķ����ƶ�������ƽ���ƶ�ԭ������֤������ˮ�������Ӧ�����ȵġ�C�
����2�������ڼ����ܽ�ת���ɿ��������ȥ������ԽǿԽ�׳�ȥ��CO3��H2OHCO3��OH��
�ȴ�����Һ����ǿЩ��˵����������Һ����ˮ��̶ȴ�֤��ˮ�������Ӧ�����ȷ�Ӧ��D�����Һ�м����̪��Һ����Һ��ɫ��dz��˵����Һ����ǿ������������Һ�мӷ�̪��Һ��CH3COONa��H2OCH3COOH��NaOH��������Һ��ɫ���˵��������ǿ��֤����ƽ���������������Ʒ����ƶ���ˮ������Ӧ�����ȵġ�
���𰸡� A
����8��ij��ʽ��NaHY��ˮ��Һc(OH)>c(H)������������ȷ����
( )
��2��A��H2Y�ĵ��뷽��ʽ��H2Y2H��Y
��������B��HY��ˮ�ⷽ��ʽ��HY��H2OH3O��Y2
��������C������ʽ����Һ������Ũ�ȹ�ϵ��c(Na)>c(HY)>c(OH)>c(H)
����������D������ʽ����Һ������Ũ�ȹ�ϵ��c(Na)>c(Y2)>c(HY)>c(OH)>c(H) ����
�������� H2Y�����ᣬ�ֲ����룬����A��һ�������Ǵ���ģ������⣬������ʽ
������������Һ�ʼ��ԣ�˵��HY��ˮ��Ϊ����HY��H2OH2Y��OH��B���ȷ����Һ��
�����������������ڣ�NaHY��Na��HY��HY��H2OH2Y��OH��c(Na)>c(HY)>c(OH)>c(H2Y)>c(H
������)��C����ȷ��D�����HYˮ��̶ȴ��ڵ���̶ȣ�����Ũ�ȴ�С�У�c(Na)>c(HY����)>c(H2Y)>c(Y2)��
���𰸡� C
9������С�մ�ˮ��Һ�ı�����ȷ����
( )
����2��A��c(Na)��c(HCO3)��c(CO3)��c(H2CO3)
����������B��c(Na)��c(H)��c(HCO3)��c(CO23)��c(OH)
����C��HCO3�ĵ���̶ȴ���HCO3��ˮ��̶�
��������������D�����ڵĵ����У�NaHCO3��Na��HCO3��HCO3H��CO2H��OH 3��H2O
�������� С�մ�NaHCO3������Һ�и����Ӵ��������¼��ֹ�ϵ��
�����������ٵ���غ㣺c(Na)��c(H)��c(OH)��c(HCO3)��2c(CO23)��
�������������غ㣺c(Na)��c(H2CO3)��c(HCO3)��c(CO23)��
����������������ʽ�����ĵ���ʽ��c(H)��c(CO23)��c(H2CO3)��c(OH)������A��ȷ��B
��������Һ�Լ���֪��ˮ����ڵ��룬C����D��ȷ��
���𰸡� AD
����10����һ��Ũ�ȵ�FeCl3��Һ�У���������ˮ��ƽ�⣺Fe3��3H2OFe(OH)3��3H��
�ڴ���Һ�е��뱥�͵�FeCl3��Һ�������ĸ��仯��˵����ȷ
( )
A��ˮ��ƽ��������Ӧ�����ƶ�
B��ˮ��ƽ�����淴Ӧ�����ƶ�
��C����Һ��HŨ������
��D��Fe3��ˮ��̶�����
���������� ���뱥�͵�FeCl3��Һ������Һ��c(Fe3)������ʹƽ�������ƶ�����Һ��
n(FeCl����ˮ��)��c(H)����FeCl3������FeCl3����n(FeCl3����)
�࣬ʹˮ��̶ȼ�С��
���𰸡� AC
11����ͬ�¶��£������ʵ���Ũ�ȵ�������Һ��a.(NH4)2SO4��b.(NH4)2CO3��
��c.(NH4)2Fe(SO4)2��c(NH4)��С�ж���ȷ����
( )
A��a��b��c B��a>b>c
C��a>c>b D��c>a>b
�������� ���⿼�����ˮ��ƽ��ԭ���ж�����Ũ�ȴ�С��������Һ�д��ڹ�ͬ���ӣ�������������NH4��ˮ�⣺NH4��H2ONH3��H2O��H��c(NH4)��ȣ�CO2CO2HCO33ˮ�⣺3��H2O
������������OH��Fe2ˮ�⣺Fe2��2H2OFe(OH)2��2H�����ԣ�c����������ˮ��������NH4ˮ
���������⣬��b��CO23ˮ�����OH���к�H�ٽ�NH4ˮ�⡣
���𰸡� D
12��(2008��ȫ���߿����)��֪����(HA)�����Աȼ���(HB)���������ʵ���Ũ�Ⱦ�Ϊ0.1 ��1mol��L��NaA��NaB�����Һ�У�����������ȷ����
( )
����A��c(OH)>c(HA)>c(HB)>c(H)
��������B��c(OH)>c(A)>c(B)>c(H)
��������C��c(OH)>c(B)>c(A)>c(H)
����D��c(OH)>c(HB)>c(HA)>c(H)
�������� ���ݡ�Խ��Խˮ�⡱��ԭ��NaA��ˮ���NaBˮ��̶ȴ�������Һ��
����������c(HA)>c(HB)��c(A)<c(B)���ٸ��ݡ�˭ǿ��˭�ԡ���֪��Һ�е�c(OH)>c(H)������
��������Һ�����ӵ�ˮ��Ͼ������ģ�����c(OH)<c(A)��c(B)��
���𰸡� A
13����25 mL 0.1 mol��L1NaOH��Һ����μ���0.2 mol��L
�й�����Ũ�ȹ�ϵ�Ƚ���ȷ���� ����1������Һ����������ͼ��ʾ��
(
)
������A����A��B����һ�㣬��Һ��һ������c(Na)>c(CH3COO)>c(OH)>c(H)
��������B����B�㣬a>12.5������c(Na)��c(CH3COO)��c(OH)��c(H)
��������C����C�㣬c(CH3COO)>c(Na)>c(H)>c(OH)
����D����D�㣬c(CH3COO)��c(CH3COOH)��2C(Na)
�������� ����ѡ��A����һ������㣬��NaOH��Һ��ֻ������������ʱ����ԶԶ
����������������Һ��ֻ��������CH3COONa������й�ϵʽc(Na)>c(OH)>c(CH3COO)>c(H)��
��ѡ��A��������ѡ��B����B��ʱ����Һ��pHǡ��Ϊ7������ݵ���غ�Ӧ�У�c(Na)��
������c(CH3COO)>c(OH)��c(H)��ѡ��BҲ����
���𰸡� CD
14��Ϊ��ͬʱ��ijũ����ʩ�÷ֱ���N��P��K����Ԫ�صĻ��ʣ����ڸ����Ļ��ʣ���K2CO3����KCl����Ca(H2PO4)2����(NH4)2SO4���ݰ�ˮ�����ʺϵ������
( )
A���٢ۢ� B���ڢۢ�
C���٢ۢ� D���ڢۢ�
���������������� K2CO3ˮ��ʼ��ԣ�CO2HCO3��OH���̬�����е�NH4��3��H2O
����������OH�ݳ�NH3ʹ��Ԫ����ʧ����ɷ�Ч���ͣ�NH4��OH��NH3����H2O��OH��H2PO4��
����2�������ɵ�PO34��Ca��Ӧ����Ca3(PO4)2���������ܱ��������գ���ˮ�������OHҲ��
����������Ӧ���ɲ�����Ca3(PO4)2��
���𰸡� B
15�����������£���CH3COONaϡ��Һ�зֱ���������������ʣ��ٹ���NaOH����
������KOH���۹���NaHSO4���ܹ���CH3COONa���ݱ����ᡣ����һ����ʹc(CH3COO)/c(Na
��)��ֵ�������
( )
A���٢� B���ڢ� C���٢� D���ڢܢ�
���𰸡� B
16���Т�Na2CO3��Һ����CH3COONa��Һ����NaOH��Һ��25 mL�����ʵ���Ũ�Ⱦ�
��Ϊ0.1 mol��L1������˵����ȷ����
( )
A��3����ҺpH�Ĵ�С˳���Ǣ�>��>��
B������3����Һϡ����ͬ������pH�仯�����Ǣ�
��C�����ֱ����25 mL 0.1 mol��L1�����pH�����Ǣ�
D����3����Һ��pH��Ϊ9�������ʵ���Ũ�ȵĴ�С˳���Ǣ�>��>��
���𰸡� C
����17��(2008��ԥ����У�߶����)��ʹ����ƽ��H2OH��OH�����ƶ�����ʹ��Һ��
���Ե���
( )
A����ˮ�м��������������ƹ���
B����ˮ�м�����������������
C����ˮ�м�������̼���ƹ���
D����ˮ���ȵ�100�棬ʹˮ��pH��6
���𰸡� B
18��(2008��Ϋ���߶����)������θҺ��pH��0.3��1.2֮�䣬θ��(һ���������ʾ)�࣫
����Ҫ���ơ�ijЩ��������θ������ҩ���к�MgCO3��NaHCO3��Ҳ���þ�ʯ���������Ƶġ���˵��
( )
A��̼�ᡢ��ʯ�ᶼ����ǿ��
B�����˶��ԣ���ʯ����Ӫ��Ʒ
C��MgCO3��NaHCO3��θ�����ò���CO2���ڷ�ҩ���к���ˮ�������
D����ʯ����ˮ��������
���𰸡� A
19�����й���FeCl3ˮ���˵���������
( )
A��ˮ��ﵽƽ��ʱ(������)�����Ȼ����ﱥ����Һ����Һ�����Ի���ǿ
��B��Ũ��Ϊ5 mol/L��0.5 mol/L������FeCl3��Һ������������ͬʱ��Fe3��ˮ��̶�
ǰ�߱Ⱥ���С
��C����50���20���ͬŨ�ȵ�����FeCl3ϡ��Һ������������ͬʱ��Fe3��ˮ��̶�ǰ
�߱Ⱥ���С
��D��Ϊ����Fe3��ˮ�⣬�Ϻõر���FeCl3��Һ��Ӧ����������
���𰸡� C
��20�������ʵ���Ũ�ȶ���0.1 mol��L1��ij����HX��Һ��NaX��Һ�������ϣ�����
˵���������
( )
������A������Ϻ���Һ��c(Na)>c(X)��˵��HX�ĵ���̶�����X��ˮ��̶�
��������B���������Һ�����ԣ���c(X)>c(Na)>c(HX)>c(H)>c(OH)
����C�������Һ��c(HX)��c(X)��0.2 mol��L1
������D�������Һ��c(HX)��c(H)��c(Na)��c(OH)
���������������� A���������Һ��c(Na)>c(X)���ɵ���غ�֪c(H)<c(OH)������HX
��������̶�����X��ˮ��̶ȣ�B���������Һ�����ԣ�˵��HX����̶ȴ���Xˮ��̶ȣ�
��������������c(X)>c(Na)>c(HX)����Һ������c(H)>c(OH)��HX����̶���Xˮ��̶ȶ�������������������c(H)��c(OH)����С��C���������Һ����ı仯��c(HX)��c(X)��0.1 mol��L1��D
�������������ɵ���غ��ϵʽ��c(H)��c(Na)��c(OH)��c(X)�������غ��ϵʽc(HX)��c(X)��
��2c(Na)�Ƴ�D����ȷ��
���𰸡� C
������ѡ����
21��(2009�������߶����)����������Һ����20 mL 0.1 mol/LH2SO4��Һ����40 mL 0.1 mol/L CH3COOH��Һ����40 mL 0.1 mol/L HCl��Һ����40 mL 0.1 mol/L NaOH��Һ����20 mL 0.1 mol/L Ba(OH)2��Һ�����У�
��(1)c(H)������__________________��
(2)��ȡ2����Һ��ϣ������Һ��pHΪ7(��ӽ�7)����__________��ȡ����
(3)�ڢܻ�Ϻ���Һ��pH__________7(����ڡ�����С�ڡ����ڡ�)��
(4)��Ϻ���ְ�ɫ������������Һ��__________��
���𰸡� (1)�� (2)4 (3)���� (4)�٢�
22��pH��2��ij��HnA(AΪ���)��pH��12��ij��B(OH)m�������ϣ����Һ��pH��Ϊ6��
(1)д�����ɵ����εķ���ʽ��__________��
(2)�����д�����һ��ˮ������ӣ������ӵ�ˮ�ⷽ��ʽΪ____________��
(3)�����û��Һ�����Ե�ԭ��__________________��
��������
����(1)���μ����е�H����е�OH��ȫ��Ӧ���ɵ��Σ�A�ԣ�n�ۣ�B�ԣ�m�ۣ�����
����ΪBnAm��
(2)��Ϊǿ��ǿ�����ǡ�÷�Ӧ���ɵ��β�ˮ�⣬��Һ�����ԣ������ϣ���Ϊ����ǿ�ᣬ���������ʱ��������϶࣬���ҺӦ�ʼ��ԣ������ϣ�����ӦΪ����ǿ���ϣ�����Anˮ�⣬ע��An�ֲ�ˮ�⣬��ֻд��һ����
An��H2OHA(n��1)��OH��
��(3)��������������H
���𰸡� (1)BnAm
������(2)An��H2OHA(n��1)��OH
��(3)�����������һ�������H
23��(2009��ԥ����У�߶����)(1)�����£���A��B��C��D������ɫ��Һ�����Ƿֱ���CH3COONa��Һ��NH4Cl��Һ�������NaNO3��Һ�е�һ�֡���֪A��B��ˮ��Һ��ˮ�ĵ���̶���ͬ��A��C��Һ��pHֵ��ͬ��
��B��__________��Һ��C��__________��
�����ڳ�������B��Һ��c(OH)��C��Һ�е�c(H)��ͬ��B��Һ��pH��PHb��ʾ��C��
Һ��pH��pHc��ʾ����pHb��pHc��__________(��ij����)��
��������(2)��֪ij��Һ��ֻ����OH��H��NH4��Cl�������ӣ�ijͬѧ�Ʋ�������Ũ�ȴ�С
˳�������¼���
����������c(Cl)>c(NH4)>c(H)>c(OH)
����������c(Cl)>c(NH4)>c(OH)>c(H)
����������c(NH4)>c(Cl)>c(OH)>c(H)
����������c(Cl)>c(H)>c(NH4)>c(OH)
��
(��)������ϵһ������ȷ����__________(�����)��
(��)����Һ��ֻ��һ�����ʣ������Һ������Ũ�ȵĴ�С��ϵΪ__________________(�����)��
����(��)����������Ũ�ȹ�ϵ��c(NH4)��c(Cl)�������Һ��__________(����ԡ�������
�ԡ������ԡ�)��
�������� (1)CH3COONa��Һ��ˮ�ĵ����ܵ��ٽ�����Һ�Լ��ԣ�NH4Cl��Һ��ˮ�ĵ����ܵ��ٽ�����Һ�����ԣ�������ˮ�ĵ����ܵ����ƣ���Һ�����ԣ�NaNO3��Һ��ˮ�ĵ��벻��Ӱ�죬��Һ�����ԡ�����A��B��C��D�ֱ�ΪNH4Cl��CH3COONa�����ᡢNaNO3��
��������������CH3COONa��Һ��c(OH)��������Һ�е�c(H)��ͬ������pHb��14��logc(H)��
��C��ҺpHc��logc(H)����pHb��pHc��14��
����������������(2)��Һ��ֻ����OH��H��NH4��Cl��������ʱ��c(Cl)>c(NH4)>c(OH)>c(H)һ��
�����ڣ���Ϊ��ʱ��Һ��������ɵ���������ȣ�����Һ��ֻ��һ�����ʣ���ΪNH4Cl��
��������Һ������Һ������Ũ�ȵĴ�С��ϵΪc(Cl)>c(NH4)>c(H)>c(OH)������������Ũ�ȹ�ϵ��
��������c(NH4)��c(Cl)��������Һ�ĵ�����ԭ������c(OH)��c(H)�������Һ�����ԡ�
���𰸡� (1)��CH3COONa ���� ��14
(2)(��)�� (��)�� (��)����
������24��ij��Ԫ��(��ѧʽ��H2A��ʾ)��ˮ�еĵ��뷽��ʽ�ǣ�H2A��H��HA HAH
��2����A
������������⣺
(1)Na2A��Һ��__________(����ԡ��������ԡ����ԡ�)��
������__________________(�����ӷ���ʽ��ʾ)��
��(2)��0.1 mol��L1��Na2A��Һ�У���������Ũ�ȹ�ϵ����ȷ����__________��
������A��c(A2)��c(HA)��0.1 mol��L1
������B��c(H)��c(OH)��c(HA)
����������C��c(Na)��c(H)��c(OH)��c(HA)��c(A2)
������D��c(Na)��2c(A2)��2c(HA)
����(3)��֪0.1 mol��L1 NaHA��Һ��pH��2����0.1 mol��L1 H2A��Һ�������ӵ����ʵ���
��Ũ�ȿ�����__________________0.11 mol��1(�<������>������)��������
__________________��
��(4)0.1 mol��L1 NaHA��Һ�и�������Ũ���ɴ�С��˳����__________________��
���𰸡� (1)����
������A2��H2OHA��OH
(2)B��C ������
(3)< H2A��һ���������H������HA�ĵ���
����������(4)c(Na)>c(HA)>c(H)>c(A2)>c(OH)
����
