产品持续稳定性观察管理规程
1目的:在有效期内监控已上市药品的质量,以发现药品与生产相关的稳定性问题(如杂质含量等的变化),并确定药品能够在标示的贮存条件下,符合质量标准的各项要求。
2范围:适用于公司产品、新产品的持续稳定性考察、由其他原因引起公司产品需要进行的稳定性考察。
3职责:质量部相关人员对其实施负责。
4内容:
4.1质量部设专人负责产品持续稳定性考察,对公司生产的每个品种的每个批号药品,按规定数量留样,填写“留样登记台账”(即留样样品观察记录),并及时做好“持续稳定性考察记录”。
4.2产品持续稳定性考察的分类:
4.2.1为公司新产品确定有效期与贮存运输条件提供科学数据所进行的稳定性考察;
4.2.2为监控公司产品在有效期内质量所进行的持续稳定性考察;
4.2.3由其他原因引起公司产品需要进行的稳定性考察。
4.2.3.1重大变更或生产和包装有重大偏差的药品;
4.2.3.2任何采用非常规工艺重新加工、返工、或有回收操作的批次;
4.2.3.3改变主要物料供应商时所作验证的批次。
4.3产品稳定性考察样品批次的规定:
4.3.1为公司新产品确定有效期与贮存运输条件提供科学数据所进行的稳定性考察,这种情况的稳定性考察需要连续试制的三批样品;
4.3.2公司新产品正常批量生产的最初三批产品应列入持续稳定性考察计划,以进一步确认有效期。
4.3.3为监控公司产品在有效期内质量所进行的持续稳定性考察批次按产品不同品种、不同规格、不同内包装形式每年考察一批,除当年没有生产外。所考察批次采取随机抽取的
方式。
4.3.4重大变更或生产和包装有重大偏差的药品批次。
4.3.4.1任何采用非正常工艺重新加工、返工或有回收操作的批次,均需做持续稳定性考察。
4.3.4.2改变主要物料供应商时所作验证的批次,均需做持续稳定性考察。
4.4持续稳定性考察样品留样量:
4.4.1持续稳定性考察样品留样量,由质量部根据不同品种包装规格及检验用量的不同要求制定,不得随意变更。
4.4.2进行长期稳定性考察和有效期确定试验的产品,每批留样量至少为一次全检量的10倍量。每一品种至少留3批进行长期稳定性考察和有效期确定试验。
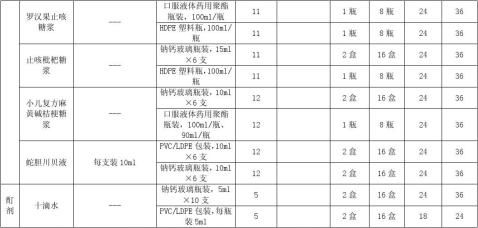
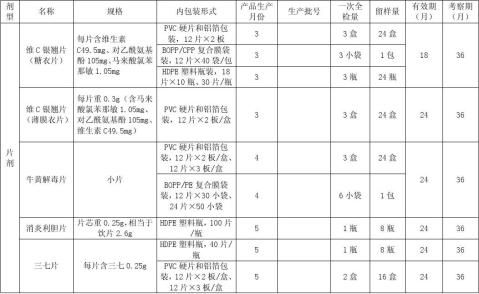
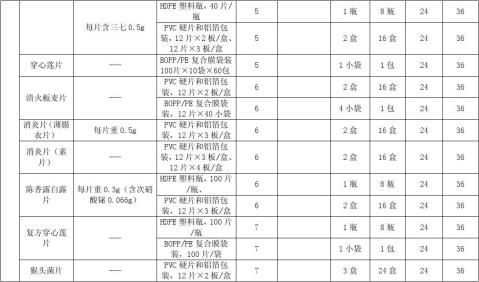
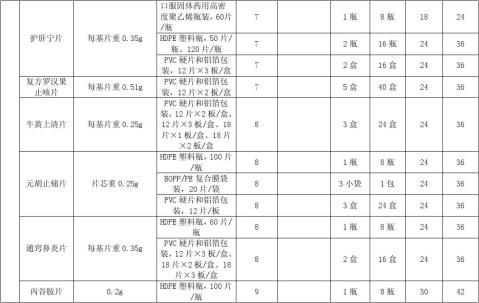
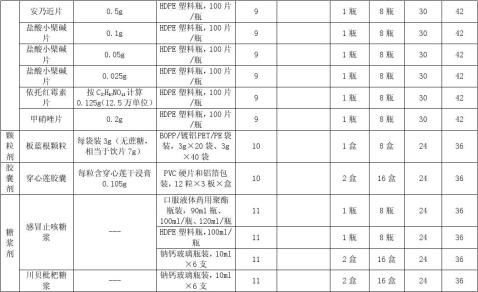
4.4.3各种剂型品种持续稳定性考察留样量如下:

4.5留样环境:
4.5.1长期稳定性考察样品留样环境:
长期稳定性考察留样样品的贮藏环境必须与法定标准中规定的贮藏条件一致,并经常保持清洁。室内应有温湿度计,留样管理员每天(节假日除外)检查留样室的温湿度情况并作好记录。
4.5.2用于加速试验考察的留样样品须在恒温恒湿仪中进行。
4.6持续稳定性考察的留样样品的存放:
4.6.1持续稳定性考察留样样品要专人专室保管,并按品种、规格、生产日期、产品批号分别排列整齐。
4.6.2每个留样柜内的品种、批号应有明显标志,并易于识别,不同品种或同一品种不同规格的样品应分别存放,不可存放于同一留样柜内,以便定期进行持续稳定性考察。
4.6.3加速试验的留样样品需在恒温恒湿仪中分类摆放。
4.6.4所有留样样品都是极为重要的实物档案,不得销售或随意取走,除留样观察外,不
得动用。
4.7持续稳定性考察留样样品的保存期:
4.7.1对于进行持续稳定性考察的留样样品。从留样日算,按稳定性试验考察方法定期复检和观察(一般观察期限为该产品有效期后1年),并作好详细的记录和报告。
4.7.2重点留样样品和长期稳定性试验、有效期确定试验的样品至少保存5年,可继延长至产品质量发生变化为止。
4.8 稳定性试验样品的取样
4.8.1 长期稳定性取样
4.8.1.1 6个月以前的监测点,必须在理论取样点的±7天内取样,并在取样后即刻检验,检验应在20天内完成。
4.8.1.2 6个月的监测点,必须在理论取样点的±14天内取样,并在取样后即刻检验,检验应在20天内完成。
4.8.1.3 6个月以后的监测点,必须在理论取样点的±30天内取样,并在取样后即刻检验,检验应在30天内完成。
4.8.1.4 如果检验不能在规定时间内进行或完成,样品必须冷藏或冷冻保存。
4.8.2 加速稳定性样品取样
4.8.2.1 必须在理论监测点的5天内取样,并在取样后即刻检验,检验应在14天内完成。
4.8.2.2 如果检验不能在规定时间内进行或完成,样品必须冷藏或冷冻保存,且有书面说明。
4.8.2.3 对于冷藏或冷冻储存的加速稳定性,样品必须在取样后的当天检验,不能滞后且所有检测必须及时进行,应在14天内完成。
4.8.3 任何计划外的试验间隔点取样,应写明原因,经质量负责人批准,并登记在册,必须保证有足够的样品用于余下的稳定性研究。
4.8.4 稳定性试验样品的取样需保证完成所有测试的需求。如果需要可多留一份或两份以便复测。
4.8.5持续稳定性考察留样样品考察期满后一个月,由留样管理员填写留样样品销毁记录,经质量部经理批准后,按期妥善处理(超过留样期限的样品每半年集中销毁一次),销毁时由2人以上现场销毁,并填写留样样品销毁记录。
4.9制定稳定性计划
4.9.1质量部QA人员于每年年初依据本年度的生产计划制订年度稳定性试验计划,确定
本年度将进行的和可能要增加进入稳定性试验程序的品种,并于每年年终对本年度公司的
稳定性试验工作做出年度总结报告。
4.9.2对不符合质量标准的结果或重要的异常趋势进行调查。任何已确认的不符合质量标准的结果或重大不良趋势,都应向当地药品监督管理部门报告;还应考虑是否可能对已上市药品造成影响,必要时应实施召回。
4.10建立稳定性试验方案
4.10.1 QA应负责建立各个产品的稳定性试验方案,由质量部经理批准实施,在方案中应明确考察对象、考察项目、考察时间、考察条件等;同时注明样品包装,要求所用材料和封装条件及厚度等与市场包装一致。
4.10.2考察对象与批次:
4.10.2.1针对上述4.3.1项、4.3.2项规定所叙述情况进行持续稳定性试验的产品,加速试验和长期试验均采用三批样品进行;
4.10.2.2针对上述4.3.3项和4.3.4项的规定,只需进行长期稳定性试验。
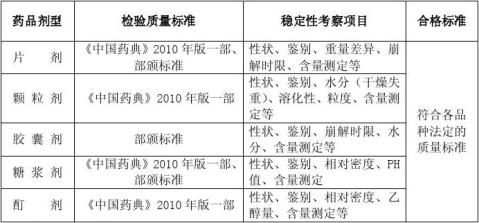
4.10.3考察项目:依据《中国药典》2010版二部中《原料药与药物制剂稳定性试验指导原则》进行确定。
4.11持续稳定性考察阶段性报告及结论:
4.11.1留样观察员根据每年所获得的持续稳定性考察试验全部数据资料,录入电脑EXCEL分品种、规格进行趋势分析,并做成曲线。
4.11.2留样观察员应当作出考察的阶段性结论,每年撰写总结报告,报质量部经理审核并向质量受权人汇报。
5相关记录
持续稳定性考察报告 SMP-QA0032-J01-01
稳定性试验记录 SMP-QA0032-J02-01
6变更历史
第二篇:XXXX年度产品持续稳定性考察计划
质量管理部 年度
产品持续稳定性考察计划
为考察我公司所有生产品种的质量稳定性,决定对所有生产品种进行长期稳定性考察试验,为确保患者能够安全、有效的用药和对各品种有效期确定等提供有效的数据。
1.对各品种生产的不同包装规格成品的正式开始生产前三批进行稳定性考察,以后每年对同一包装规格取一批次产品进行稳定性考察。
2.考察方法
2.1、按市售包装,在药品标示的贮存条件下保存12个月(温度25℃±2℃、相对湿度60%±10%)。每3个月取样一次,分别于0个月,3个月,6个月,9个月,12个月取样,按各剂型品种具体的稳定性考察项目进行检测。12个月后,仍需继续考察,分别于18个月,24个月,36个月取样进行检测。将结果与0个月比较以确定药品有效期。
2.2、由于实验数据的分散性,一般应按95%可信限进行统计分析,得出合理的有效期。如三批统计数据分析结果差别较小,则取平均值为有效期。若差别较大,则取其最短的为有效期。同时能够明确各剂型品种的安全性、稳定性及有效性。
2.3、对于每种规格、每种内包装形式的药品,每年考察一个批次,若是原计划考察当月的指定包装规格的品种未生产,则选取离原计划最近月份所生产的相同内包装形式的品种进行稳定性考察,除非当年没有生产。
2.4、某些情况下,持续稳定性考察中应当额外增加批次数,如重大变更或生产和包装有重大偏差的药品应列入稳定性考察。此外,重新加工、返工或回收的批次,也应当考虑列入考察,除非已经验证和稳定性考察。
1
三、方案的实施
本方案由质量管理部完成,记录上述所有数据,并对试验过程中不符合质量标准的结果或重要异常情况记录与调查。对任何已经确认的不符合质量标准的结果或重大不良趋势,必要对产品实施召回,并对调查结果盒采取的措施报告当地药品监督管理部门。
四、考察结果的报告
产品稳定性考察完毕后,根据所获得的全部数据资料,包括考察的阶段性结论,撰写总结报告并保存,并定期审核总结报告。
2
3
4
5
6
种生产的,则以相近月份生产的1个批号进行持续稳定性考察。
7