实验一 动物组织切片观察
一.实验目的
1.正确书写实验报告
2.系统发生及个体发生
3.生物量级:组织层次
4.多细胞生物与单细胞生物
二.实验原理
光学显微镜由机械装置和光学系统两大部分组成(见下图)。机械装置一般包括镜筒、物镜转换器、镜台、镜臂和镜座部分等;光学系统包括目镜、物镜、聚光器、光源等。标本经物镜和管镜放大后,形成放大倒立的实像;实像经目镜再次放大后,形成放大的虚像。
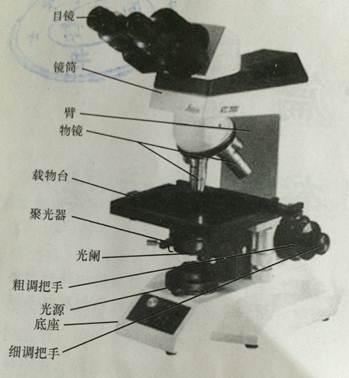
三.动物与器材
动物组织切片,显微镜
四.方法与步骤
1.显微镜工作原理
2.动物组织构成
3.切片观察
五.实验结果
六.实验结论
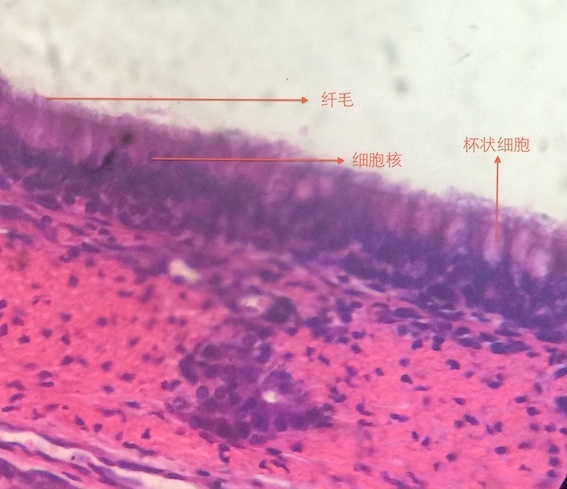
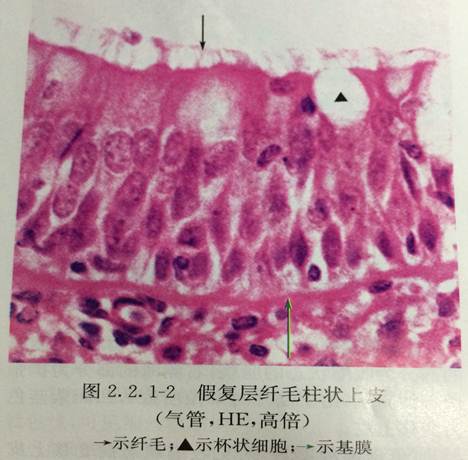
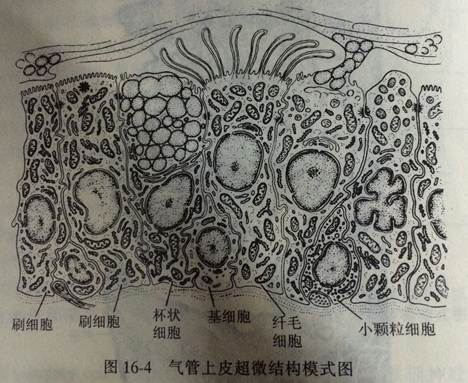
假复层纤毛柱状上皮主要分布在呼吸管道,由纤毛细胞、杯状细胞、刷细胞、基细胞和小颗粒细胞等组成(图2.2.1-2、图16-4)。其中纤毛细胞最多,呈柱状,游离面有密集的纤毛,纤毛向咽部快速摆动,将粘液及附着其上的尘埃、细菌等推向咽部被咳出,净化吸入的空气。杯状细胞较多,形态与肠道杯状细胞相同。分泌的粘蛋白与混合腺的分泌物在上皮表面构成粘液性屏障,可粘附空气中的异物颗粒,溶解吸入的SO2等有毒气体。刷细胞呈柱状,游离面有排列整齐地微绒毛,形如刷状。小颗粒细胞是一种内分泌细胞,数量少,锥形,单个或成团分布在上皮深部,胞质内有许多致密核心颗粒,可调节呼吸道平滑肌的收缩与腺体的分泌。基细胞呈锥形,位于上皮深部,为干细胞,可增殖分化为上皮中其它各类细胞。
七.问题解答
1.显微镜下观察标本切片的基本程序依次为哪些?
显微镜的准备→标本的肉眼观察→低倍镜→高倍镜→油镜
2.气管HE染色横切片在低倍镜和高倍镜下分别可以看到那些结构?
低倍镜:从内向外依次为:黏膜(表面为假复层纤毛柱状上皮;上皮深面的细密结缔组织为固有层,其内可见小血管、淋巴组织和气管腺的导管,有时可见导管在黏膜上的开口),黏膜下层(为疏松结缔组织,含有成团的混合性腺,即气管腺),外膜(由疏松结缔组织和“C”形透明软骨环组成,由于切面关系软骨环可能呈节段样。软骨环切口处,有弹性纤维组成的韧带、平滑肌束和腺体)
高倍镜:固有层内含丰富的弹性纤维,断面呈红色点状。混合性的气管腺可见浆液性、粘液性、混合性的气管腺可见浆液性、黏液性、混合性腺泡和复层上皮的导管。
八.参考文献
1.《组织学与胚胎学第五版》邹仲之主编 人民卫生出版社
2.《人体显微形态学实验》 汪维伟 王娅兰主编 科学出版社
第二篇:病理组织切片技术是病理实验室最基本的方法
病理组织切片技术是病理实验室最基本的方法,是病理学的一项极有使用价值的专业技能。它包括组织固定、脱水、透明、包埋、切片、漂片、烤片、脱蜡、染色、脱水、透明和封固等程序。HE 染色是既基本又十分重要的工作,HE 染色的好坏直接影响病理医生的正确诊断,而HE 染色质量好坏与HE 制片的每一步骤关系都十分密切。只要某一步骤出了问题都直接影响下一步工作,时常会出现个别片子色调不正、颜色对比不协调、染色不匀、模糊不清等现象,使切片的质量和诊断的准确性受到影响。本文作者在实验过程中就制作优良动物病理切片的体会阐述如下:
一、取材要及时、规范
(一)要取最新鲜的材料。由于各器官组织坏死变化很快,所以取材要求迅速。取材时要用锋利的刀片或剪刀,勿用镊子对组织加以压迫,以免组织破裂和变形。
(二)选取组织块的大小、厚薄亦应力求适度。过大、过厚的组织,固定液不宜渗透,亦可造成固定不佳,过小、过薄的组织又可能在固定或脱水的过程中发生扭曲变形情况[1]。
(三)应有代表性,能够反映出组织的基本结构,如肝要有肝小叶;肾要有皮质和髓质;肺要有支气管等。另外,要采取病变部位和健康部位交叉处的组织,这样才可以通过健康部位的对照,清楚地看到各种病理变化。
二、固定要充分
(一)一般固定液,都以新配为好,配好后应贮存在阴凉处,不宜放在日光下,以免引起化学变化,失去固定作用。笔者常用的固定液是10%福尔马林溶液。
(二)应及时固定,这样可保持细胞与生活时的形态相似,防止组织自溶而产生死后变化。将取下的材料立即放在固定液中固定24小时以上,固定液必须充足,一般为材料块的20~30倍,有些水分多的材料,中间应更换1~2次新液。目的是防止腐败、保持原有结构并使组织硬化,便于处理。笔者为了让组织块固定充分,常在此步骤增加一步重新修块和重复固定,做法是修块大小为10 mm×10 mm×2 mm,然后放入新配制好的10%福尔马林溶液中固定12小时以上,避免了因固定不充分带来的切片问题,收到很好的效果。
(三)材料固定完毕后,保存于严密紧塞或加盖的容器里,同时在容器外贴上标签,并随同材料在溶液中投入相应的标签,以免相互混淆。标签上注明固定液、材料来源、日期等。标签上的文字,应用黑色
铅笔或绘图黑墨水书写。
(四)材料经固定后,除乙醇外,组织中的固定液必须冲洗干净。因为残留在组织中的固定液,有的不利于染色,有的产生沉淀或结晶影响观察。冲洗方法根据固定液的性质而定,固定液为水溶液的常用水洗涤,方法是将组织块放入冲洗盒中,流水冲洗12小时以上;陈旧的固定时间长的组织应冲洗24小时左右,保证冲洗干净。
三、脱水、透明要彻底
(一)脱水采用酒精梯度脱水法,让组织块依次经过70%、80%、95%Ⅰ、95%Ⅱ、100%Ⅰ、100%Ⅱ等各级酒精溶液中,脱水必须在有盖的玻璃瓶中进行,防止吸收空气中的水分和酒精挥发,保证脱水彻底。否则不易透明,甚至使透明剂内出现白色混浊现象。
(二)笔者在实践中得出脱水的时间为70%2小时、80%2小时、95%Ⅰ1.5小时、95%Ⅱ1.5小时、100%Ⅰ0.5小时、100%Ⅱ0.5小时,就能达到彻底脱水的效果。如需过夜,应停留在95%酒精中。在100%酒精中,每级停留的时间不宜太长,否则会使组织变脆,影响切片。
(三)使用二甲苯作为透明剂时,要随时盖紧盖子,以免空气中的水分进入。更换每级透明剂,动作要迅速,一方面为了不使材料块干涸,另一方面能避免吸收湿气。
(四)在透明过程中, 如果材料周围出现白色雾状,说明材料中的水未被脱净,应退回纯酒精中重新脱水,然后再透明。
四、浸蜡包埋要认真
(一)透蜡温度要恒定,不可忽高忽低;由于作者使用的石蜡溶点为58℃,所以恒温箱的温度设定为60℃,保持不变。
(二)操作要迅速,力求在最短的时间内完成石蜡透入过程,以免引起组织变硬、变脆、收缩等。作者采用两次浸蜡,每次各15分钟,这样浸蜡较为充分,没有发生组织变硬、变脆、收缩等情况。
(三)包埋过程可在恒温箱中进行,避免由于温度变化导致组织块和蜡的分离,影响切片。放置组织
块时注意切面朝下放置,并用温镊子轻轻拨动材料,使之摆放平整。待石蜡完全凝固(约30min)后即可取出备用。
五、切片要完整,贴片要恰当。
(一)切片刀要锋利,切片刀如果不锋利,切出的片会自行卷起,如刀片有缺口,将使制成的切片断裂、破碎、不完整。此时可通过更换刀片解决。
(二)切片刀放置的倾角要合适。过大则切片上卷,过小则切片皱起。切片厚度一般要在4-6微米;过厚,会出现双层细胞的现象,不便于观察。一张优良的切片,在切片时应尽可能的将所要的组织结构切出,要力求完整,铺片时要平整,没有折叠[2]。笔者在切片之前将包埋好的组织块预先冰冻10分钟,避免皱褶产生且利于展片。
(三)贴片过程中,用小镊子夹取预先用刀片割开的蜡带,放入38℃ 恒温水浴锅的水面上,注意蜡片光亮平整的一面贴于玻片上,并使之处于稍偏玻片的一端。
(四)展片后将载玻片放在平盘上做好标记,置于60℃温箱中烘片至少12小时以上,防止染片过程中脱片。
六、染色封固要细心
(一)染色液多数为水溶液,因此,染色前必须将蜡脱去,一般采用二甲苯脱蜡,逐级复水与脱水浸蜡过程正好相反,但是,由于蜡片较薄,所需时间比脱水浸蜡要短的多。石蜡切片经二甲苯Ⅰ、Ⅱ脱蜡各5~10min,然后放入100%、95%、90%、80%、70%等各级酒精溶液中各3~5min,再放入蒸馏水中3min。
(二)染色:切片放入苏木精中染色约5~10min。染色时间应根据染色剂的成熟程度及室温高低,适当缩短或延长。室温高时促进染色,染色时间可短些,否则可适当延长时间,冬季室温低时可放入恒温箱中染色。一般常用的苏木素染液染色之后需要分化,但是往往分化时间难以掌握,所以作者采用了Gill改良苏木精染液[3],不需要分化过程,效果非常理想。
(三)水洗:用自来水流水冲至少15min。冲洗过程中要注意流水不能过大,不能直冲,以防切片脱落,并随时用显微镜检查见颜色变蓝为止。以作者的经验流水冲洗30 min左右效果最为理想,此时低倍镜检查见细胞核呈蓝色、结构清楚,红细胞颜色为金黄色。
(四)对于一张染色良好的切片来说伊红染色也是重要的一步。有时伊红染色淡,这可能是某些原因导致伊红不易着染,或者在后面的酒精脱水过程中,又把伊红的颜色脱掉。伊红染色也不宜过深。一张染色好的切片应该是苏木素伊红染色对比度适当鲜艳亮丽。
(五)封固:切片经染色、脱水、透明后,即可用封固剂将其封藏起来,目的是永久保存切片,便于镜检。封固时不应该等切片上的二甲苯干了在封固,否则,切片中易出现色素[4]。放置盖玻片时避免产生气泡。如胶液不足,可以用玻棒再滴一滴树胶从盖玻片边缘补足。如胶液过多,可在干燥以后用刀刮去,并用纱布蘸二甲苯拭去残留的树胶。
笔者认为,制片过程的每一步骤都必须认真对待、科学处理,否则就会影响制片质量。一张优良的切片从外观上看要平整、无皱折、无破裂,厚薄适度,分化良好,HE染色对比度好、明亮鲜艳,封胶、标签整洁。只有认真、科学、严谨的对待切片制作的每一个步骤,掌握每一个细节,不断总结经验,才能制作出优良的病理组织切片,为教学、科研提供依据。
