20##~20##学年学业水平测试模拟试卷(五)
化 学
2016.1
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分100分,考试时间75分钟。
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Na—23 Mg—24
Cl—35.5 Fe—56 Cu—64 Ag—108
第Ⅰ卷(选择题 共69分)
一、 单项选择题:本部分共23小题,每小题3分,共69分。在每小题的4个选项中,只有1个选项是符合要求的。
1. 为扼制温室效应,使用下列燃料可实现二氧化碳零排放的是( )
A. 氢气 B. 天然气
C. 汽油 D. 乙醇汽油
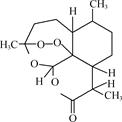
2. 中国著名药学家屠呦呦因制成了青蒿素而获得20##年度诺贝尔生理学或医学奖。青蒿素的结构如右图,关于该物质的分类正确的是( )
A. 单质 B. 有机物
C. 无机物 D. 有机高分子化合物
3. 下列过程属于物理变化的是( )
A. 光合作用 B. 铁块锈蚀 C. 矿石粉碎 D. 石油裂化
4. 钚(Pu)是制造威力更大原子弹的良好原料。下列有关说法错误的是( )
A. 原子序数为94 B. 质子数为94 C. 质量数为239 D. 中子数为94
5. 用一束光通过淀粉溶液时,产生丁达尔现象,说明淀粉溶液属于( )
A. 溶液 B. 胶体 C. 悬浊液 D. 乳浊液
6. 下列物质中含有共价键的离子化合物是( )
A. HCl B. NaOH C. CaCl2 D. N2
7. 下列各组物质中互为同分异构体的是( )
A. CH3CH2OH 和CH3OCH3 B. CH4和CH3CH3
C. C与C D. 金刚石和石墨
8. 下列气体中能用排水法收集的无色气体是( )
A. SO2 B. Cl2 C. NO2 D. NO
9. 用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的的是 ( )
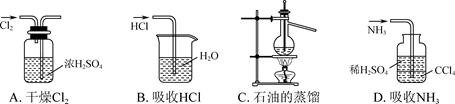
10. 下列物质的名称、俗名与化学式完全对应的是( )
A. 氯化钠 食盐 NaCl2 B. 碳酸氢钠 纯碱 NaHCO3
C. 氢氧化钠 烧碱 NaOH D. 氢氧化钙 熟石灰 CaO
11. 在汽车尾气处理装置中加入某种催化剂,发生如下反应:4CO+2NO2===4CO2+N2。下列对该反应的说法中错误的是( )
A. 该反应中氧化剂是CO、还原剂是NO2
B. 该反应是氧化还原反应
C. 该反应生成28 g N2时,转移8 mol e-
D. 该反应能减少汽车尾气对环境的污染
12. 下列化学用语书写正确的是( )
A. 氯原子的结构示意图: 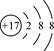
B. 乙烯的结构简式为CH2CH2
C. 氯化镁的电子式: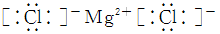
D. 硫酸的电离方程式:H2SO4===H+SO
13. 对于硫酸工业中SO2的催化氧化反应 2SO2+O2 2SO3,下列说法错误的是( )
2SO3,下列说法错误的是( )
A. 使用催化剂能加快化学反应速率
B. 增大O2浓度可以使SO2转化率达到100%
C. 降低反应温度,化学反应速率减慢
D. 增大O2浓度,化学反应速率增大
14. 下列关于乙酸的说法正确的是( )
A. 酸性比碳酸弱
B. 可以使紫色石蕊试液变红
C. 难溶于水
D. 能被氧化为乙醛
15. 某溶液中存在大量的OH-、Na+、SO,该溶液中还可能大量存在的离子是( )
A. Al3+ B. Ba2+ C.NH D. CO
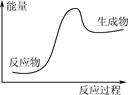
16. 下列反应过程中的能量变化情况符合右图的是( )
A. NaOH与H2SO4发生中和反应
B. 氧化钙和水反应
C. NH4Cl和Ba(OH)2·8H2O的反应
D. 一氧化碳气体的燃烧
17. 用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A. 54 g Al分别与足量的稀硫酸及氢氧化钠溶液反应失去的电子数都是6NA
B. 同温同压下,NA个NO2与NA个N2和O2的混合气体的体积不相等
C. 1 mol·L-1的MgCl2溶液中,含有Cl-个数为2NA
D. 11.2 L氧气中所含有的原子数为NA
18. 下列反应的离子方程式书写正确的是( )
A. 硫酸和氢氧化钡溶液反应:Ba2++SO===BaSO4↓
B. 碳酸钠与盐酸反应:Na2CO3+2H+===2Na++CO2↑+H2O
C. Ca(NO3)2溶液和Na2CO3溶液混合:Ca2++CO===CaCO3↓
D. 铁钉放入硫酸铁溶液中:Fe+Fe3+===2Fe2+
19. 对于某些离子的检验及结论正确的是( )
A. 向某溶液中滴加NaOH溶液并加热,用湿润的蓝色石蕊试纸于试管口以检验NH
B. 加入氯化钡溶液有白色沉淀产生,再加入盐酸,沉淀不消失,一定有SO
C. 某待测液焰色反应呈黄色,则待测液中一定不含有K+
D. 某溶液中加入KSCN后,溶液无变化,再加入H2O2后,溶液变成血红色,说明原溶液中一定含有Fe2+
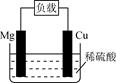
20. 某原电池结构如右图所示,下列有关该原电池的说法正确的是( )
A. 电池反应为Mg+2H+===Mg2++H2↑
B. 镁棒发生还原反应
C. 电子从铜棒经外电路流向镁棒
D. 铜棒为负极
21. 下列有机反应属于加成反应的是( )
A. CH4+Cl2CH3Cl+HCl
B. CH3CH2OH+CH3COOH浓硫酸△CH3COOCH2CH3+H2O
C. H2C===CH2+HCl—→H3C—CH2Cl
D. 2CH3CH2OH+O2Cu△2CH3CHO+2H2O
22. X、Y、Z、R、W是原子序数依次增大的短周期主族元素,X是元素周期表中原子半径最小的元素。X与Z同主族,Y与W同主族,R最外层电子数是电子层数的2倍。下列叙述正确的是( )
A. 原子半径:W>R>Z
B. W的最高价氧化物对应的水化物酸性比R的强
C. W与X形成的是离子化合物
D. W的气态氢化物的热稳定性比Y的强
23. 某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路。某课外活动小组为确定反应后的废液组成,进行如下实验:(1) 取100.00 mL反应后的废液加入足量的AgNO3溶液,生成沉淀12.915 g。(2) 另取100.00 mL反应后的废液加入过量铜片充分反应,铜片质量减少了0.32 g。下列关于反应后的废液组成判断正确的是( )
A. 只含有Fe2+、Cu2+、Cl-,不含有Fe3+
B. c(Fe2+)∶c(Cu2+) =1∶1
C. c(Fe3+)∶c(Fe2+)=1∶3
D. c(Cl-) =0.9 mol·L-1,c(Fe3+) = 0.1 mol·L-1
第Ⅱ卷(非选择题 共31分)
二、 非选择题:本部分共3小题,共31分。
24. (15分)本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题,每位考生只可选做1题。若两题都作答,则以A题计分。
A. 《化学与生活》
(1) (5分)改善环境质量已成为全球共识。保护环境,人人有责。
① 空气质量报告的各项指标可以反映出该地区的空气质量状况,下列不需要监测的成分是________(填字母)。
a. SO2 b. N2 c. 可吸入颗粒物
② pH<________的雨水称为酸雨,煤炭燃烧产生的SO2所形成的酸雨,其最终的主要成分是________(填化学式)。
③ 煤中加入石灰石可以大大减少SO2的排放,发生反应的化学方程式为______________________________。
(2) (6分)保持营养均衡,合理使用药物是人类健康的重要保证。
① 人体内提供能量的主要营养物质为________、糖类和蛋白质,人体内蛋白质在蛋白酶作用下水解的最终产物是________。
② 维生素C能防治坏血病并具有还原性,验证维生素C有还原性可以使用淀粉溶液和________试剂共同完成。
③ 咽喉发炎的病人可以使用药物____________(填“氢氧化铝”或“青霉素”),起到杀菌消炎作用。
④ 阿司匹林(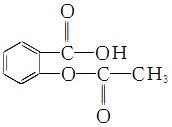 )在人体内可以水解为水杨酸(
)在人体内可以水解为水杨酸(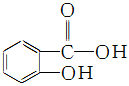 )和一种生活中常见的酸味剂,具有解热镇痛疗效,写出其水解的化学方程式:______________________________。
)和一种生活中常见的酸味剂,具有解热镇痛疗效,写出其水解的化学方程式:______________________________。
(3) (4分)材料是人类生活的物质基础,新型材料的制造则是科技快速发展的重要标志。
① 钢铁是制造铁路、桥梁、轮船等的主要材料,钢铁在潮湿的空气中主要发生________(填“吸氧”或“析氢”)腐蚀,腐蚀时Fe作为原电池的________极。
② 目前,很多地方使用的泡沫塑料快餐具的主要成分是聚苯乙烯(简称EPS),聚苯乙烯属于________(填字母)。
a. 无机非金属材料 b. 金属材料 c. 有机高分子材料
③ 工业上生产玻璃、水泥都要用到的原料是________。
B. 《有机化学基础》
(1) (3分)根据结构对有机物进行分类,有助于对其性质的掌握。
① 有机物苯属于________(填字母)。
a. 芳香烃 b. 烯烃 c. 炔烃
② 下列有机物属于酚类的是________(填字母)。
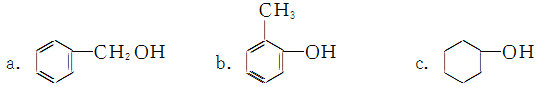 ③ 纤维素属于________(填字母)。
③ 纤维素属于________(填字母)。
a. 糖类 b. 油脂 c. 蛋白质
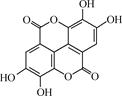
(2) (5分)柴胡红景天中的活性成分之一是鞣花酸(结构式如右图)。
① 鞣花酸的分子式为________。
② 鞣花酸分子中含氧官能团为________和________(填名称)。
③ 1 mol鞣花酸最多可与________mol Br2发生取代反应;1 mol鞣花酸最多可与含________mol NaOH的溶液发生反应。
(3) (7分)莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。

① 区别两种酸的方法是______________________。莽草酸与溴水的反应方程式为__________________。
② 等物质的量的两种酸与足量NaOH溶液反应,消耗氢氧化钠物质的量之比是______________。
③ 鞣酸的核磁共振氢谱图(H核磁共振谱图)上有________个吸收峰。
25. (6分)下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质。气体B与气体C相遇产生白烟,A是强碱,D的焰色反应呈紫色(部分反应物和生成物及溶剂水已略去)。
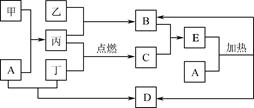
请回答下列问题:
(1) D的化学式为____________。
(2) C的电子式为____________。
(3) 写出A溶液和甲反应的离子方程式:__________________________________。
(4) 写出工业上制备B的化学方程式:__________________________________。
26. (10分) 胆矾(CuSO4·5H2O)是铜的重要化合物,有着广泛的应用,如用来配制农药波尔多液。以下是CuSO4·5H2O的实验室制备流程图:
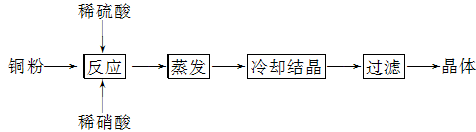
请回答下列问题:
(1) 向含有铜粉的稀硫酸中滴加硝酸,在铜粉溶解时最终可以观察到的实验现象是____________________、____________________。
(2) 如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4·5H2O中可能存在的杂质是________________(填化学式)。
(3) 将CuSO4·5H2O与NaHCO3按一定的比例共同投入到150 mL沸水中,剧烈搅拌,冷却后,有绿色晶体析出。该晶体的化学组成为Cux(OH)y(CO3)z·nH2O。实验所得的绿色晶体需充分洗涤,检验是否洗涤干净的方法是__________________________________________________________。
(4) 为了确定晶体的化学式,某实验小组进行如下实验:
a. 称取3.640 g晶体,加入足量的稀盐酸使固体完全溶解,收集到标准状况下的气体448.0 mL;
b. 称取等质量的晶体,灼烧至完全分解,得到2.400 g残余固体。
通过计算确定晶体的化学式(写出计算过程)。
20##~20##学年学业水平测试模拟试卷(五)(宿迁)
化学参考答案及评分标准
1. A 2. B 3. C 4. D 5. B 6. B 7. A 8. D 9. D 10. C 11. A 12. C 13. B 14. B 15. D 16. C 17. A 18. C 19. D 20. A 21. C 22. B 23. D
24. (15分)
(1) (5分)① b(1分) ② 5.6(1分) H2SO4(1分)
③ 2CaCO3+2SO2+O22CaSO4+2CO2
(或CaCO3CaO+CO2↑ 2CaO+2SO2+O2===2CaSO4)(2分)
(2) (6分)① 油脂(1分) 氨基酸(或α-氨基酸)(1分) ② 碘水(1分) ③ 青霉素(1分)
④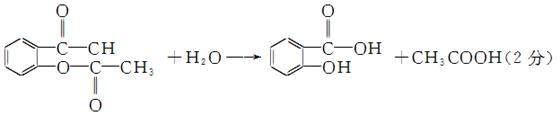 (3) (4分,每空1分)① 吸氧 负极 ② c ③ 石灰石(或CaCO3)
(3) (4分,每空1分)① 吸氧 负极 ② c ③ 石灰石(或CaCO3)
24B. (15分)
(1) (3分,每空1分)① a ② b ③ a
(2) (5分,每空1分)① C14H6O8 ② 羟基 酯基 ③ 2 8
(3) (7分) ① 氯化铁溶液(或溴水)(2分)
 ② 1∶4(2分) ③ 4(1分)
② 1∶4(2分) ③ 4(1分)
25. (6分)(1) KCl(1分) (2)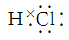 (1分)
(1分)
(3) 2Al+2OH-+2H2O===2AlO+3H2↑(2分) (4) N2+3H2 2NH3(2分)
2NH3(2分)
26. (10分)(1) 溶液呈蓝色、有红棕色气体产生(2分)
(2) Cu(NO3)2(2分)
(3) 取最后一次洗涤液少许与试管中,加入盐酸酸化的BaCl2溶液,若没有白色沉淀生产,则洗涤干净(2分)
(4) n(CO)=n(CO2)=0.448 L/22.4 mol·L-1=0.02 mol
灼烧最终得到的固体是CuO
n(Cu2+)=n(CuO)=2.400 g/80 g·mol-1=0.03 mol(1分)
根据电荷守恒:n(Cu2+)×2=n(OH-)+n(CO)×2
n(OH-)=n(Cu2+)×2-n(CO)×2=0.03 mol×2-0.02 mol×2=0.02 mol(1分)
n(H2O)=(3.640 g-0.03 mol×64g·mol-1-0.02mol×17g·mol-1-0.02mol×60g·mol-1)/18g·mol-1=0.01 mol(1分)
x∶y∶z∶n=0.03 mol∶0.02 mol∶0.02 mol∶0.01 mol=3∶2∶2∶1
晶体的化学式为Cu3(OH)2(CO3)2·H2O或Cu(OH)2·2CuCO3·H2O(1分)
