第三章 第三节 金属晶体
一、选择题(每小题只有一个选项符合题意,3分×10)
1、下列有关金属晶体的说法中正确的是( )
A.常温下都是晶体
B.最外层电子数少于3个的都是金属
C.任何状态下都有延展性
D.都能导电、传热
2、金属Mg晶体中含有的粒子是( )
A.Mg原子 B.只有Mg2+ C.Mg原子和Mg2+ D.Mg2+与自由电子
3、下列有关化学键、氢键和范德华力的叙述中,不正确的是( )
A.金属键是金属离子与“电子气”之间的较强作用,金属键无方向性和饱和性
B.共价键是原子之间通过共用电子对形成的化学键,共价键有方向性和饱和性
C.范德华力是分子间存在的一种作用力,分子的极性越大,范德华力越大
D.氢键不是化学键,而是分子间的一种作用力,所以氢键只存在于分子与分子之间
4、关于晶体的下列说法正确的是( )
A、在晶体中只要有阴离子就一定有阳离子
B、在晶体中只要有阳离子就一定有阴离子
C、原子晶体的熔点一定比金属晶体的高
D、分子晶体的熔点一定比金属晶体的低
5、金属的下列性质中,与自由电子无关的是 ( )
A.密度大小 B.容易导电 C.延展性好 D.易导热
6、金属晶体的熔沸点之间的差距是由于( )
A.金属键的强弱不同
B.金属的化合价的不同
C.金属的晶体中电子数的多少不同
D.金属的阳离子的半径大小不同
7、下列物质的熔沸点依次升高的是( )
A.K、Na、Mg、Al B.Li、Na、Rb、Cs
C.Al、Mg、Na、K D.C、K、Mg、Al
8、金属具有延展性的原因是( )
A.金属原子半径都较大,价电子较少
B.金属受外力作用变形时,金属阳离子与自由电子间仍保持较强烈作用
C.金属中大量自由电子受外力作用时,运动速度加快
D.自由电子受外力作用时能迅速传递能量
9、金属晶体堆积密度大,原子配位数高,能充分利用空间的原因是( )
A.金属原子的价电子数少
B.金属晶体中有自由电子
C.金属原子的原子半径大
D.金属键没有饱和性和方向性
10、石墨晶体中不存在的化学作用力是( )
A.共价键 B.氢键 C.金属键 D.范德华力
二、选择题(每小题有一至两个选项符合题意,4分×7)
11、下列说法不正确的是( )
A.金属单质的熔点一定比非金属单质高
B.离子晶体中不一定含有金属元素
C.在含有阳离子的晶体中,一定含有阴离子
D.含有金属元素的离子不一定是阳离子
12、下列有关金属晶体的说法中不正确的是( )
A.金属晶体是一种“巨分子”
B.“电子气”为所有原子所共有
C.简单立方堆积的空间利用率最低
D.钾型堆积的空间利用率最高
13、下列叙述正确的是 ( )
A、同主族金属的原子半径越大,熔点越高
B、稀有气体的原子序数越大沸点越高
C、晶体中存在离子的一定是离子晶体
D、金属晶体中的自由电子属于整个晶体共有
14、下列何种物质的导电性是由自由电子的运动所决定的 ( )
A 熔融的食盐 B 饱和食盐水 C 石墨 D 铜
15、石墨是层状晶体,每一层内,碳原子排成正六边形,许多个正六边形排列成平面状结构,如果将每对相邻原子间的化学键看成一个化学键,则石墨晶体每一层内碳原子数与C-C化学键数的比是 ( )
A 2︰3 B 1︰3 C 1︰1 D 1︰2
16、下列叙述中,可以肯定是一种主族金属元素的是( )
A.原子最外层有3个电子的一种金属
B.熔点低于100℃的一种金属
C.次外电子层上有8个电子的一种金属
D.除最外层,原子的其他电子层电子数目均达饱和的一种金属
17、下列数据是对应物质的熔点,有关的判断错误的是 ( )

A.只要含有金属阳离子的晶体就一定是离子晶体
B.在共价化合物分子中各原子都形成8电子结构
C.同族元素的氧化物可形成不同类型的晶体
D.金属晶体的熔点不一定比分子晶体的高
三、填空题(共42分)
18、(6分)(1)金属导电是____________________的结果.
(2)金属导热是____________________的结果.
(3)金属抽成丝或压成薄板是金属受到外力作用,紧密堆积的原子(离子)层发生了________________,而金属离子和自由电子之间的____________________没有改变.
19、(14分)有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A+与D2-离子数之比为2:1。
请回答下列问题:
(1)A元素形成的晶体属于 晶体,其熔沸点比同周期的金属元素单质的要低,这是因为 。
(2)B—的电子排布式为 ,在CB3分子中C元素原子的原子轨道发生的是 杂化。
(3)C的氢化物的空间构型为 。
(4)B元素的电负性 D元素的电负性(填“>”,“<”或“=”);用一个化学方程式说明B、D两元素形成的单质的氧化性强弱:_ 。
20、(8分)用X射线研究某金属晶体,测得在边长为360pm的立方晶胞中含有4个金属原子,此时金属的密度为 9.0g/cm3。试回答:
(1)此金属晶体的堆积模型为
(2)每个晶胞的质量是 g(保留三位有效数字)
(3)此金属的相对原子质量为 。
(4)此金属原子的原子半径 pm。
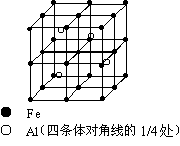
21、(4分)晶体是质点(分子、离子、或原子)在空间有规则地排列的,具有整齐外形,以多面体出现的固体物质。在空间里无限地周期性的重复能成为晶体的具有代表性的最小单元,称为晶胞。一种Al-Fe合金的立体晶胞如图所示。
(1)确定该合金的化学式____________。
(2)若晶胞的边长=a nm,计算此合金的密度________________g/cm3。
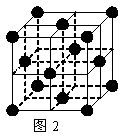
 22、(10分)1183 K以下纯铁晶体的基本结构单元如图1所示,1183 K以上转变为图2所示结构的基本结构单元,在两种晶体中最邻近的铁原子间距离相同。
22、(10分)1183 K以下纯铁晶体的基本结构单元如图1所示,1183 K以上转变为图2所示结构的基本结构单元,在两种晶体中最邻近的铁原子间距离相同。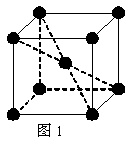
(1)铁原子的简化电子排布式为 ;铁晶体中铁原子以 键相互结合。
(2)在1183 K以下的纯铁晶体中,与铁原子等距离且最近的铁原子数为_______个;在1183 K以上的纯铁晶体中,与铁原子等距离且最近的铁原子数为____个;
(3)纯铁晶体在晶型转变前后,二者基本结构单元的边长之比为(1183 K以下与1183 K以上之比)__________ _。
(4)转变温度前后两者的密度比(1183 K以下与1183 K以上之比)___________ _。
第三章 第三节 金属晶体 答案卷
班级: 姓名:
18、(1)自由电子在电场作用下定向移动
(2)自由电子碰撞金属离子而将能量传给金属离子
(3)相对滑动 较强烈的相互作用(金属键)
19、.(1)金属;因为钠在同周期中的原子半径大,单位体积内的自由电子数目少,所以金属键弱,熔沸点低。
(2)ls22s22p63s23p6,sp3
(3)三角锥形
(4)>;H2S+Cl2=2HCl+S↓
20、(1)面心立方晶格类型;(2)4.20×10-22g;(3)63.21;(4)127.26pm
21、(1)Fe2Al (2)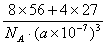 =
=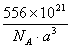
22、.(1)[Ar]3d64s2 金属
(2) 8 (2分) 12
(3)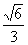 (4)
(4)
边长a=3.16×10;半径r=1.37×10-8cm
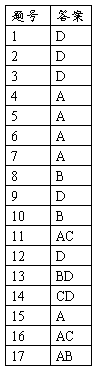
答案:DDDAA AABDB AC D BD D A AC AB
18、(1)自由电子在电场作用下定向移动
(2)自由电子碰撞金属离子而将能量传给金属离子
(3)相对滑动 较强烈的相互作用(金属键)
19、.(1)金属;因为钠在同周期中的原子半径大,单位体积内的自由电子数目少,所以金属键弱,熔沸点低。
(2)ls22s22p63s23p6,sp3
(3)三角锥形
(4)>;H2S+Cl2=2HCl+S↓
边长a=3.16×10;半径r=1.37×10-8cm
20、(1)面心立方晶格类型;(2)4.2×10-22g;(3)63.21;(4)127.28pm
21、(1)Fe2Al (2)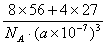 或
或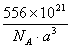
22、.(1)[Ar]3d64s2 金属
(2) 8 (2分) 12
(3)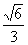 (4)
(4)
金属钨晶体为体心立方晶格,如图所示,实验测得钨的密度为19.30 g·cm-3,原子的相对质量为183,假定金属钨原子为等径的刚性球。
(1)每个晶胞含有 个钨原子;
(1)钨晶胞的边长 cm;
(2)钨原子的半径为 cm。
第二篇:人教版选修《物质结构与性质》第三章 第三节金属晶体

集各地最新资料精华 按“教材目录、知识体系”编排 高中化学人教版选修《物质结构与性质》
第三章 晶体结构与性质
第三节 金属晶体
金平区鮀浦中学 冯海鹏
教材分析:
在《普通高中化学课程标准(实验)》中,涉及金属晶体的内容标准包括:
(1)知道金属键的涵义;
(2)能用金属键理论解释金属的一些物理性质(良好的导电性、导热性和延
展性);
(3)能列举金属晶体的基本堆积模型;
(4)知道金属晶体与其它晶体的结构微粒、微粒间作用力的区别。
关于金属键的涵义,教材上的说法有些模糊,不利于学生的理解,教学中应点明金属键是脱落下来的自由电子跟形成的金属正离子的相互作用,而所谓的“电子气”,不过是一种比较形象的说法,指的是脱落下来的电子好像气体一样遍布整块晶体。
在这四点中,第二点要求的程度是“解释”,显然比其余三点高,因此,第二点应该作为本节的教学重点之一,而教材除对延展性有较为详细的解释外,其它物理性质的解释都是一笔带过,所以教学过程中应作详细讲解。
第三点的要求虽然较低,但在前面分子晶体和原子晶体的学习中,《课程标准》里要求学生学会运用模型来研究结构问题,因此本节教学中可以利用讲解该部分知识的机会继续培养学生运用模型研究结构问题的能力,所以也作为教学重点之一。教师的演示模型可将不同颜色的弹珠用胶水黏合制得,而学生实验所需的小球则可使用自行车中所用的那种轴承滚珠,也可提前要求学生自己准备,培养学生的创造力。
第四点的教学则可以在讲解完金属键的本质后,与分子晶体和原子晶体的相关知识进行比较、区分。也可以在讲新课之前先进行复习。另外一种处理方法则是等讲完离子晶体后再全面对四种晶体进行对比。以下教学设计将采用第一种方法,并将在本章复习中对四种晶体进行更全面的比较。
此外,教材中出现了“配位数”这个名词,这涉及到第二章第二节中有关配位化合物的知识,但配位数的涵义在《课程标准》中并无要求,而且在配位化合物这部分的知识中也没有出现该名词,因此不宜作深入探讨,可简单解释为:配位数是指任意一个原子周围与之相接触的原子的数目。资料卡片中有两个内容,一个是“金属晶体的四种堆积模型对比”,另一个是“混合晶体”,前者在教学中可以引导学生进行阅读,后者理解起来较难,可视各所学校学生的具体情况灵活处理。以下教学设计将不涉及“混合晶体”的引导阅读。
集全国化学资料精华,按“四套教材(旧人教版、新课标人教版、苏教版、鲁科版)目录、知识体系”编排。资源丰富,更新及时。欢迎上传下载。 1

集各地最新资料精华 按“教材目录、知识体系”编排
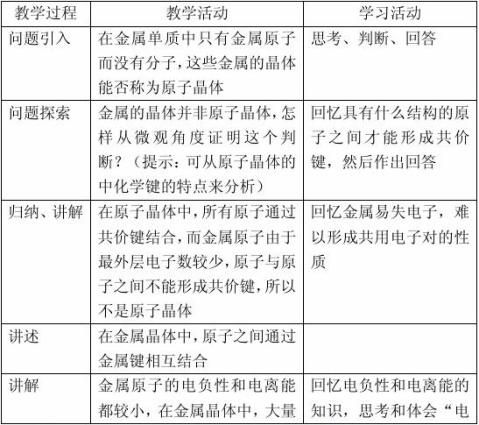
基于以上分析,本节教学设计如下:
【教学目标】
(1)知道金属键的涵义;
(2)能用电子气理论解释金属的一些物理性质,如延展性、导电性、导热性
等;
(3)能运用模型研究晶体的结构;
(4)知道金属晶体与分子晶体、原子晶体在结构微粒、微粒间作用力上的区
别
【教学重点】
用金属键理论解释金属的物理性质,金属晶体的原子堆积模型
【教学难点】
电子气理论,镁型和铜型堆积模型
【教学方法】
问题探究、实验探究
【教学用时】
1课时
【教学过程】
版)目录、知识体系”编排。资源丰富,更新及时。欢迎上传下载。 2

集各地最新资料精华 按“教材目录、知识体系”编排 集全国化学资料精华,按“四套教材(旧人教版、新课标人教版、苏教版、鲁科版)目录、知识体系”编排。资源丰富,更新及时。欢迎上传下载。 3

集各地最新资料精华 按“教材目录、知识体系”编排 集全国化学资料精华,按“四套教材(旧人教版、新课标人教版、苏教版、鲁科版)目录、知识体系”编排。资源丰富,更新及时。欢迎上传下载。 4

集各地最新资料精华 按“教材目录、知识体系”编排
板书设计: §3 金属晶体
一、金属键
1、自由电子与金属正离子的相互作用称为金属键
2、自由电子与金属物理性质的关系
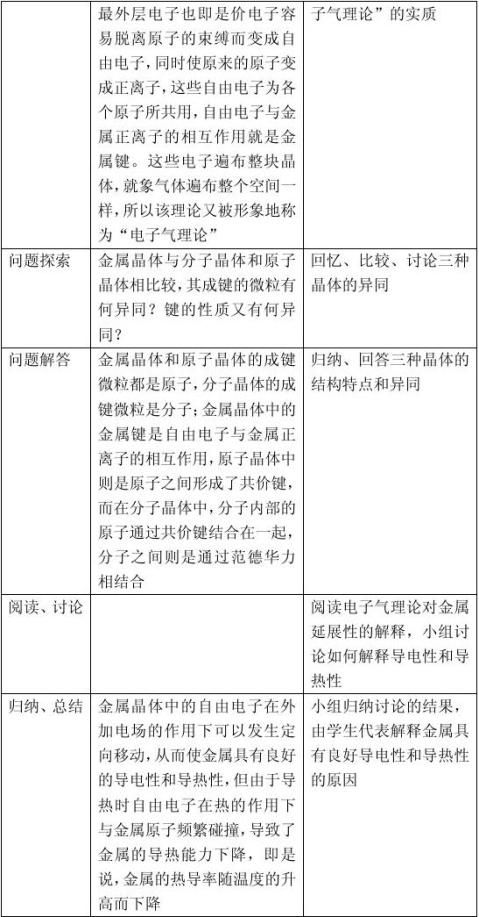
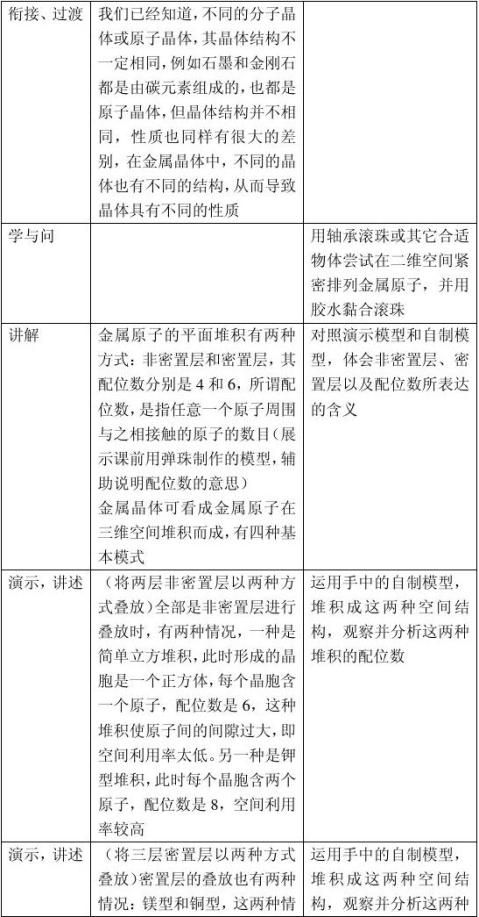
二、金属晶体的原子堆积模型
1、 非密置层
密置层
2、简单立方堆积:非密置层+非密置层 配位数:6
钾型: 非密置层+非密置层 配位数:8
镁型: 密置层+密置层+密置层 配位数:12
铜型: 密置层+密置层+密置层 配位数:12
集全国化学资料精华,按“四套教材(旧人教版、新课标人教版、苏教版、鲁科版)目录、知识体系”编排。资源丰富,更新及时。欢迎上传下载。 5