实验 15 蔗糖水解反应速率常数测定
一、实验目的
1.学习测定反应级数、反应速率常数的方法;
2.掌握旋光仪的使用;掌握通过测量系统物理量跟踪反应系统浓度的方法。
二、实验原理
蔗糖水溶液在H+存在的条件下,按下式进行水解:
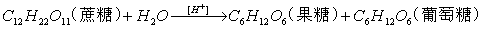
在该反应中,H+是催化剂,当温度、H+浓度一定时,反应速率与蔗糖和水的浓度成正比, 即:
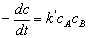 (15.1)
(15.1)
式中, 分别代表蔗糖浓度和水的浓度。
分别代表蔗糖浓度和水的浓度。
当蔗糖浓度很低时,反应过程中H2O浓度相对与蔗糖浓度改变很小,故,可近似认为cB为常数,令:
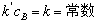 (15.2)
(15.2)
则(15.1)式可写成:
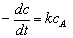 (15.3)
(15.3)
将(15.3)式分离变量后进行定积分:
当 t=0时, CA=CA0 ;
t=t时, CA=CA;
定积分式为:
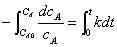 (15.4)
(15.4)
积分结果:
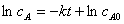 (15.5)
(15.5)
(15.5)式是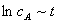 的直线方程。反应进行过程中,测定不同时刻 t 时反应系统中蔗糖的浓度cA,取得若干组cA、t 的数据后,以lncA对t 作图,得一直线,表明该反应为一级反应(准一级反应),直线斜率为-k。
的直线方程。反应进行过程中,测定不同时刻 t 时反应系统中蔗糖的浓度cA,取得若干组cA、t 的数据后,以lncA对t 作图,得一直线,表明该反应为一级反应(准一级反应),直线斜率为-k。
物理化学的研究方法是采用物理的方法测定反应系统某组分的浓度,所谓物理的方法是利用反应系统某组分或各组分的某些物理性质(如面积、压力、电动势、折光率、旋光度等)与其有确定的单值函数关系的特征,通过测量系统中该物理性质的变化,间接测量浓度变化。此种物理化学的实验方法最大的优点是可以跟踪系统某组分或各组分的物理性质的变化,从而,不需要终止反应,便可以随时测定某一时刻反应系统某组分或各组分的浓度。
本实验利用反应物与产物旋光度这一物理性质上的差异确定反应系统中反应物浓度CA。
实验过程中某一时刻反应系统中蔗糖浓度CA与同一时刻反应系统的旋光度βt、反应完成时反应系统的旋光度β∞之差成正比,即:
t=t时, cA∝βt-β∞; (15.6a)
或 cA=f(βt-β∞) (15.6b)
式中f 是比例系数。
同理,t=0时,cA=cA0,
cA0∝β0-β∞; (15.7a)
或: cA0=f(β0-β∞); (15.7b)
(15.6b) 式除以(15.7b)代入(15.5)式得:
 (15.8a)
(15.8a)
则,  (15.8b)
(15.8b)
(15.8b)为 ~t 的直线方程,式中,β0、β∞为反应初始及反应终了时反应系统的旋光度,它们均不随时间改变。实验过程中只需要测定反应进行的不同时刻t时反应系统的旋光度βt(若干个数据)和反应终了时反应系统的旋光度β∞(一个数据),以
~t 的直线方程,式中,β0、β∞为反应初始及反应终了时反应系统的旋光度,它们均不随时间改变。实验过程中只需要测定反应进行的不同时刻t时反应系统的旋光度βt(若干个数据)和反应终了时反应系统的旋光度β∞(一个数据),以 对t作图得一直线,直线斜率为-k,用作图法可求出反应速率常数k。
对t作图得一直线,直线斜率为-k,用作图法可求出反应速率常数k。
β∞也可以不测,而用数据处理中介绍的方法计算得到。
关于偏振光的知识在物理课中已经有所介绍,以下就本实验有关的问题介绍如下:
当偏振光通过旋光物质的溶液时,偏振光的振动面偏转一定角度β,此角度的大小与偏振光通过的溶液浓度C及液层厚度L成正比,即:
 ∝c×L (15.9a)
∝c×L (15.9a)
写成等式为:
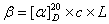 (15.9b)
(15.9b)
(15.9b)式中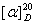 为被测溶液的比旋光度,即当旋光物质溶液浓度C为 1kg.dm-3, 液层厚度为0.1m时溶液的旋光度。又因为光波的波长对旋光度有影响,故规定以20℃的钠光(波长为2896×10-9m, 记为“D”)为标准,记作
为被测溶液的比旋光度,即当旋光物质溶液浓度C为 1kg.dm-3, 液层厚度为0.1m时溶液的旋光度。又因为光波的波长对旋光度有影响,故规定以20℃的钠光(波长为2896×10-9m, 记为“D”)为标准,记作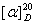 。
。
使偏振光顺时针偏转的物质称为右旋物质,反之为左旋物质,以右旋为正,左旋则为负。本实验所涉及的三种旋光物质的比旋光度分别为:
蔗糖: 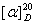 = 66.55º
= 66.55º
葡萄糖: 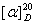 = 52.50º
= 52.50º
果糖: 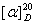 =-91.90º
=-91.90º
以此为根据,可以判断本实验反应系统的旋光度,反应初始时应为正值,随着反应的进行,旋光度逐渐减小,反应终了时,反应系统的旋光度为负值。
三、 仪器药品
旋光仪一台;25ml移液管两支;洗耳球一个;100ml三角瓶一个(带胶塞);盐酸水溶液2mol.dm-3(或3mol.dm-3);0.25kg.dm-3蔗糖溶液;恒温水浴一套(共用, 当用数据处理中介绍的方法计算β∞时,不用恒温水浴)。
四、实验步骤
1. 测定旋光仪零点:旋光仪接通电源,点亮钠光灯,等约5~10分钟,待光源正常后,测零点,测量方法有二:
⑴当采用测量β∞的方法进行实验时,旋光仪内不装入旋光管,盖上盖,调整焦距,使视野清晰,然后缓慢转动手轮,使视野中的三部分亮度均匀(注意,此时三部分亮度均匀但较暗),从刻度盘游标尺上读取读数(在零度附近),其精度为0.05º。
⑵当用数据处理中介绍的方法计算β∞,而不测量时,将旋光管内灌满纯净的蒸馏水,放入旋光仪,盖上盖,调整焦距,使视野清晰,然后缓慢转动手轮,使视野中的三部分亮度均匀(注意,此时三部分亮度均匀但较暗),从刻度盘游标尺上读取读数(在零度附近),其精度为0.05º。
2.反应系统旋光度的测定:用指定移液管取25ml蔗糖溶液置于碘量瓶中,用另一支移液管取25ml盐酸溶液迅速注入碘量瓶中,注入一半时开始记时,全部注入后,将混合液摇均匀,灌入准备好的、洁净的旋光管,盖上小玻璃片及管盖,擦干旋光管,将旋光管放入旋光仪,尽快(最好在记时后5分钟之内)测定反应系统的第一个旋光度βt,方法同“1”,此后,分别测量第10、15、20、25、30、35、40、45、50、55、60、90分钟左右系统的旋光度。
3.β∞的测量:将盛有剩余溶液的三角瓶作上标记,放入公用的恒温水浴中,恒温45~60分钟后,取出自然冷却至室温,“2”步完成后,将旋光管中溶液倒掉,灌入三角瓶中的溶液,按照“2”中介绍的方法测量β∞。测量一次以后,隔约20分钟后,再测量一次,两次测量结果基本相同说明反应已进行到底。
五、注意事项
1.先掌握旋光仪的使用,主要是掌握三分视野均匀且很暗的视野的确定.
2.旋光管在应用前必须洗干净,实验完成后先用自来水洗净,再用蒸馏水涮净;
3.液体装入旋光管后,管内不能有大气泡,光路内不能有气泡,有小气泡,可将其赶至旋光管的凸部。
4旋光管必须擦净后才能放入旋光仪,否则液体中的盐酸会腐蚀仪器;
5.旋转手轮(旋转检偏镜)时,动作不能过猛,并尽可能顺时针旋转
6.每次测量后,应将旋光管取出,下次测量前再放入,避免仪器升温给测量带来误差;
7.转动检偏镜,找到三分视野均匀但较暗处即为溶液该时刻的旋光度,注意与三分视野均匀但很亮处的区别。
六、数据记录
实验温度: 测量前T0 = 29 ℃; 测量前Td= 28 ℃; 平均温度Tm= 28.5 ℃
旋光管长度: L = 2 dm;
反应液中蔗糖溶液的初始浓度:cA0= 0.125 kg ?dm-3
反应液中盐酸溶液的浓度: cH = 1.00 mol ?dm-3
表1 实验数据记录表

七、数据处理
⑴.用测得的不同时刻 t 时的βt 减同一个β∞,得一组βt-β∞ ,取自然对数(或常用对数)得ln(βt-β∞)数据,记入下表2.13.2。
表2 数据处理记录表
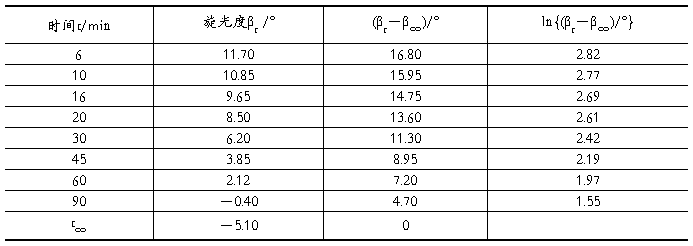
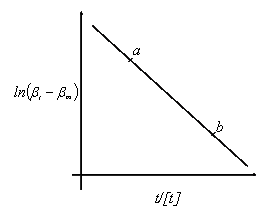 ⑵ 在坐标纸上,以ln(βt-β∞)为纵坐标,以t/min为横坐标绘图得一直线,在线上取点求直线斜率m,由直线斜率求出反应速率常数 m/min = -k。
⑵ 在坐标纸上,以ln(βt-β∞)为纵坐标,以t/min为横坐标绘图得一直线,在线上取点求直线斜率m,由直线斜率求出反应速率常数 m/min = -k。

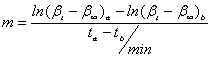
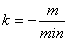
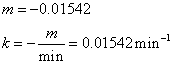

八、思考题
1蔗糖浓度、盐酸浓度对反应速率常数k有什么影响?
答:蔗糖的浓度对k没有影响;盐酸是催化剂,其浓度对k有影响,盐酸浓度越高,k值越大。
2 某一时刻数据未来得及测出怎么办?
答:反应开始后,任何时刻的ln(βt-β∞)与t的关系都符合直线关系,故可以测量相邻任意时刻(如下一分钟)的数据。
3. 如何确认反应终了时的β∞可靠?
答:反应结束后,如果温度不变,β∞值不再改变,两次测量β∞值基本不变(考虑读数误差,故基本不变)就可以认为β∞可靠。
4. 旋光管内有小气泡怎么办?
答:将小气泡赶到玻璃球处,使光路中没有气泡即可。
5. 为什么用测量β∞的方法时,零点的测量时可以不放入旋光管?
答:因为数据处理时,用ln(βt-β∞)对t作图,仪器零点对零点的影响在βt-β∞中已经减掉了。
6. 旋光仪的零点是怎么设计的?
答:旋光仪的零点设计使检偏镜的透光轴处于起偏镜透光轴与石英玻璃透光轴两轴垂直线的角平分线上。
九、旋光仪介绍
1. 旋光仪结构
WXG-4型旋光仪如图所示:

图2. WXG—4型旋光仪
1. 钠光灯 2. 起偏镜 3. 石英玻离片 4. 旋光管 5. 检偏镜 6. 手轮
7. 游标刻度盘 8. 焦距调节钮 9. 目镜
2. 测量原理
自钠光灯发出的波长为2890~2896A的非偏正光,经起偏镜2后成为强度为E0的偏振光(图2.13.2a所示)。起偏镜后面的石英玻离片3是旋光物质, 其旋光度约为3º, 其宽度为起偏镜直径的三分之一, 放置在光路的中间, 将光路的视野分成了三部分(图2.13.2b所示)。若Ⅰ、Ⅲ部分偏振光(电磁波)的振动方向为0º(图中AA),则第Ⅱ部分偏振光的振动方向为右旋3º(图中BB)。
调零点时,若将检偏镜6偏振光振动化方向KK与AA垂直(图2.13.2c所示),根据物理学中的马吕萨定律:
E=E0COS2θ
θ- 起偏镜振动化方向与检偏镜振动化方向的夹角。
此时从目镜中看进去,视野的Ⅰ、Ⅲ部分是黑的(EⅠ=EⅢ= E0COS290º=0),而位于中间的第Ⅱ部分是亮的, 不过光强度很小(EⅡ= E0COS287º)。若将检偏镜偏振光振动化方向KK与BB垂直(图2.13.2d所示), 则位于中间的第Ⅱ部分是黑的(EⅡ= E0COS290º=0),而视野的Ⅰ、Ⅲ部分是亮的,同样光强度很小(EⅠ=EⅢ=E0COS293º)。
旋光仪把仪器的零点设计在了OO轴位置上(图2.13.2e所示),在此位置上OO轴与AA轴的夹角θ1、OO轴与BB轴的夹角θ2同为88.5º (90-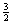 )º, 在此位置, θ1=θ2, 光路视野的三部分强度相等(EⅠ= EⅡ=EⅢ= E0COS288.5º)。若OO轴稍偏于AA轴,Ⅰ、Ⅲ部分变黑,第Ⅱ部分变亮,反之OO轴稍偏于BB轴,第Ⅱ部分变黑,Ⅰ、Ⅲ部分变亮,有明与暗的比较,偏于零点位置时容易鉴别,可使仪器的测量精度较高。
)º, 在此位置, θ1=θ2, 光路视野的三部分强度相等(EⅠ= EⅡ=EⅢ= E0COS288.5º)。若OO轴稍偏于AA轴,Ⅰ、Ⅲ部分变黑,第Ⅱ部分变亮,反之OO轴稍偏于BB轴,第Ⅱ部分变黑,Ⅰ、Ⅲ部分变亮,有明与暗的比较,偏于零点位置时容易鉴别,可使仪器的测量精度较高。
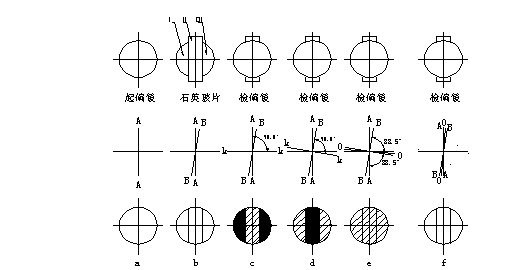
图2.13.2 旋光仪测量原理示意图
放入装有旋光物质的旋光管后,旋光物质把AA、BB两个方向的偏振光同时偏转一角度β,此时光路视野必然变化。将检偏镜同样旋转β,再找到光路三分视野均匀,光强度很小的位置,检偏镜从零点旋转到此位置的角度β,可以从游标刻度盘上读到,此角度就是旋光物质的旋光角。
 要注意的是,若将检偏镜偏振化方向置于AA轴与BB轴夹角的平分线O’O’上,(如图Ⅱ-8-2f所示),光路视野的三部分也是均匀的,但光很亮,光强度为EⅠ= EⅡ=EⅢ= E0COS21.5º。生理学研究发现人对弱光敏感,而对强光不敏感,故若将检偏镜偏振化方向置于O’O’附近的很大范围内变化,尽管视野的三部分光强度有不同变化,但人们凭视力难于分辨,从目镜看进去,检偏镜在较大范围内旋转,光路视野的三部分似乎都没有变化。此种情况特别容易与正常的三分视野均匀弄混,使用时应特别予以注意。
要注意的是,若将检偏镜偏振化方向置于AA轴与BB轴夹角的平分线O’O’上,(如图Ⅱ-8-2f所示),光路视野的三部分也是均匀的,但光很亮,光强度为EⅠ= EⅡ=EⅢ= E0COS21.5º。生理学研究发现人对弱光敏感,而对强光不敏感,故若将检偏镜偏振化方向置于O’O’附近的很大范围内变化,尽管视野的三部分光强度有不同变化,但人们凭视力难于分辨,从目镜看进去,检偏镜在较大范围内旋转,光路视野的三部分似乎都没有变化。此种情况特别容易与正常的三分视野均匀弄混,使用时应特别予以注意。
旋光仪的正确使读数
第二篇:8实验八蔗糖水解反应速率常数的测定
 宁 波 工 程 学 院
宁 波 工 程 学 院
物理化学实验报告
专业班级 化工095 姓名 何可欣 序号 09402010507
同组姓名 吴陆萍 指导老师罗利娟、蒋仲庆 实验日期 2011.5.25
实验名称 实验八 蔗糖水解反应速率常数的测定
一、实验目的
1. 了解蔗糖水解反应体系中各物质浓度与旋光度之间的关系。
2. 测定蔗糖水解反应的速率常数和半衰期。
3.了解旋光仪的基本原理,掌握其正确的操作技术。
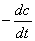 二、实验原理
二、实验原理
反应速率只与某反应物浓度的一次方成正比的反应称为一级反应,速率方程可由下式表示:
—
式中c为时间t时的反应物浓度,k为反应速率常数。
积分可得: lnc=-kt + lnc0
c0为反应开始时反应物浓度。
当c= c0/2时,对应t可用t1/2表示,称为反应的半衰期,即反应物浓度反应掉一半所用时间,得一级反应的半衰期为: t1/2=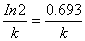
蔗糖在水中转化成葡萄糖与果糖,其反应为:
C12H22O11 + H2O C6H12O6 + C6H12O6
C6H12O6 + C6H12O6
(蔗糖) (葡萄糖) (果糖)
它属于二级反应,在纯水中此反应的速率极慢,通常需要在H+离子催化作用下进行。由于反应时水大量存在,尽管有部分水分子参与反应,仍可近似地认为整个反应过程中水的浓度是恒定的,而且H+是催化剂,其浓度也保持不变。因此蔗糖转化反应可看作为一级反应。
蔗糖及其转化产物,都具有旋光性,而且它们的旋光能力不同,故可以利用体系在反应进程中旋光度的变化来度量反应进程。
测量物质旋光度所用的仪器称为旋光仪。溶液的旋光度与溶液中所含旋光物质的旋光能力,溶剂性质,溶液浓度,样品管长度及温度等均有关系。当其它条件均固定时,旋光度α与反应物浓度c呈线性关系,即
α=Kc
式中比例常数K与物质旋光能力,溶剂性质,样品管长度,温度等有关。
物质的旋光能力用比旋光度来度量,比旋光度用下式表示:

式中“20”表示实验时温度为20℃,D是指用纳灯光源D线的波长(即589毫微米),α为测得的旋光度,l为样品管长度(dm),cA为浓度(g/100mL)。
作为反应物的蔗糖是右旋性物质,其比旋光度 =66.6°;生成物中葡萄糖也是右旋性物质,其比旋光度
=66.6°;生成物中葡萄糖也是右旋性物质,其比旋光度 =52.5°,但果糖是左旋性物质,其比旋光度
=52.5°,但果糖是左旋性物质,其比旋光度 =-91.9°。由于生成物中果糖的左旋性比葡萄糖右旋性大,所以生成物呈左旋性质。因此随着反应的进行,体系的右旋角不断减小,反应至某一瞬间,体系的旋光度可恰好等于零,而后就变成左旋,直至蔗糖完全转化,这时左旋角达到最大值α∞。
=-91.9°。由于生成物中果糖的左旋性比葡萄糖右旋性大,所以生成物呈左旋性质。因此随着反应的进行,体系的右旋角不断减小,反应至某一瞬间,体系的旋光度可恰好等于零,而后就变成左旋,直至蔗糖完全转化,这时左旋角达到最大值α∞。
设最初系统的旋光度为 α0=K反cA,0 (t=0,蔗糖尚未水解) (1)
最终系统的旋光度为 α∞=K生cA,0 (t=∞,蔗糖已完全水解) (2)
当时间为t时,蔗糖浓度为cA,此时旋光度为αt
αt= K反cA+ K生(cA,0-cA) (3)
联立(1)、(2)、(3)式可得:
cA,0= =K′(α0-α∞) (4)
=K′(α0-α∞) (4)
cA=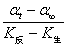 = K′(αt-α∞) (5)
= K′(αt-α∞) (5)
将(4)、(5)两式代入速率方程即得:
ln(αt-α∞)=-kt+ln(α0-α∞)
我们以ln(αt-α∞)对t作图可得一直线,从直线的斜率可求得反应速率常数k,进一步也可求算出t1/2。
三、实验仪器、试剂
仪器:旋光仪,停表,恒温水浴一套,移液管(50mL),磨口锥形瓶(100mL),烧杯(100mL),台秤,洗耳球
试剂:蔗糖(AR),盐酸 (3mol/L,AR)
四、实验步骤
(一)旋光仪的校正
1.了解旋光仪的构造、原理,掌握其使用方法(见附录)。
2.开启水浴恒温水槽的电源开关,并将水浴恒温槽的温度控制在60℃。
3.蒸馏水为非旋光性物质,可用来校正仪器的零点(即α=0时,仪器对应的刻度)。洗净样品管,将样品管一端盖子打开,转入去离子水,然后盖上玻璃片,此时管内不应有空气泡存在,再旋上套盖,使玻璃片紧贴旋光管,勿使漏水。但必须注意旋紧套盖时,不能用力过猛,以免压碎玻璃片,用滤纸擦干样品管,再用擦镜纸将样品管两端的玻璃片擦干净。放入旋光仪,打开电源,预热5-10min,钠灯发光正常。调目镜聚焦,使视野清晰;调检偏镜至三分视野暗度相等为止,记录游标(右边)刻度为检偏镜旋角,记录仪器零点。读数注意0度以下的实际旋光度(读数-180)。读数三次取平均值,即为零点,用来校正仪器的系统误差。
(二)测定
1、 配制蔗糖溶液:用天平称取10克蔗糖放入烧杯中,加蒸馏水溶解后转移到50ml容量瓶中,稀释至刻度。
2、用50ml移液管移取50mlHCL溶液放入蔗糖水溶液,边放边振荡,当HCL溶液放出一半时按下秒表开始计时(注意:秒表一经启动,勿停直至实验完毕)。迅速用反应混合液将样品管洗涤三次后,将反应混合液装满样品管,擦净后放入旋光仪,测定规定时间的旋光度。测得第一个数据时间应该为反应开始的前三分钟内。测量时先将三分视场调节到全暗,再记录时间(注意时间要记录准确,以实际反应时间为准),后读数。分别记录5min、10min、15min、20min、25min、30min、40min、50min、60min的旋光度。
3、α∞的测量:测定过程中,可将剩余的反应混合物放入60℃恒温槽中加热30min,使反应充分后,冷却至室温后测定体系的旋光度,连续读数三次平均值。
由于反应液的酸度很大,因此样品管一定要擦干净后才能放入旋光仪内,以免酸液腐蚀旋光仪,实验结束后必须洗净样品管。
3.
五、数据记录与处理
实验温度: 26.4℃ ; HCl浓度: 3mol/L ;零点:0.275 α∞: -4.725 。
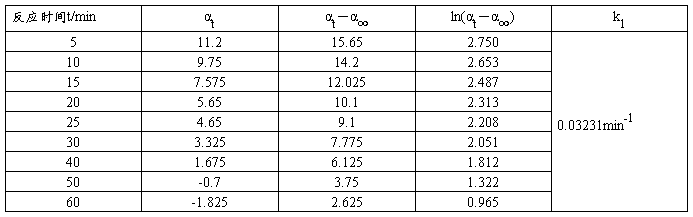
以ln(αt—α∞)对t作图,并由直线斜率求速率常数k1。

斜率=-0.032316,所以k1=0.03231 min -1=5.385×10-4 s-1
t1/2= ln 2 /k1 =0.693 / k1 = 0.693 / 5.385×10-4 =1286.9 s
六、结果与讨论
本实验是测定蔗糖水解反应速率常数,实验过程中应该注意:
1、 装样品时,旋光管管盖旋至不漏液体即可,不要用力过猛,以免压碎玻璃片。
2、 在测定α∞时,通过加热使反应速度加快转化完全。但加热温度不要超过60℃。
大约60min后基本分解完全。
3、 由于酸对仪器有腐蚀,操作时应特别注意,避免酸液滴漏到仪器上,实验结束后必须将旋光管洗净。
七、思考题
1. 为什么可用蒸馏水来校正旋光仪的零点?
答:主要是因为蒸馏水没有旋光性,其旋光度为零,其次是因为它无色透明,方便可得,化学性质较为稳定。
2. 在旋光度的测量中为什么要对零点进行校正?它对旋光度的精确测量有什么影响?在本实验中若不进行校正对结果是否有影响?
答:旋光仪由于长时间使用,精度和灵敏度变差,故需要对零点进行校正。若不校正会使测量值的精确度变差,甚至产生较大的误差。本实验数据处理时,用旋光度的差值进行作图和计算,仪器精度误差可以抵消不计,故若不进行零点较正,对结果影响不大。
3. 为什么配置蔗糖溶液可用上皿天平称量?
答:蔗糖水解为一级反应,反应物起始浓度不影响反应速度常数,又因为蔗糖浓度大用量较多,量值的有效数字位数较多,故不需要精确称量,只要用上皿天平称量就可以了。
