中学化学竞赛试题资源库——银镉金汞
A组
[1].a、b、c、d、e分别是Cu、Ag、Fe、Al、Mg五种金属中的一种。已知:①a、c均能与稀硫酸反应放出气体;②b与d 的硝酸盐反应,置换出单质d;③c与强碱反应放出气体;④c、e在冷浓硝酸中发生钝化。由此判断.a、b、c、d、e分别是
A Fe、Cu、Al、Ag、Mg B Al、Cu、Mg、Ag、Fe
C Mg、Cu、Al、Ag、Fe D Mg、Ag、Al、Cu、Fe
[2].在含有Cu(NO3)2、Mg(NO3)2和AgNO3的溶液中加入适量锌粉,首先置换出的是
A Mg B Cu C Ag D H2
[3].要使溶液中的Ag+、Ba2+、Cu2+、Mg2+、Al3+等离子逐一形成沉淀析出,选择的试剂及其加入的顺序都正确的是
A NaCl-Na2SO4-Na2S-NaOH-CO2
B HCl-H2SO4-H2S-NaOH-CO2
C H2SO4-HCl-H2S-NaOH-CO2
D Na2S-Na2SO4-NaCl-NaOH-HCl
[4].为了测定某铜银合金的成分,将30.0g合金完全溶于80mL 13.5mol/L的浓硝酸中,待合金完全溶解后,收集到气体6.72L(标准状况),并测得溶液的pH值等于零。假设反应后溶液的体积仍为80mL,试计算:
(1)被还原的硝酸的物质的量
(2)合金中银的质量百分含量
(3)求气体的成分及各自的含量
[5].在250mL氯化汞溶液里放入75g铜片,反应一段时间后,把铜片从溶液里取出、洗净、干燥后,称其质量为76.37g。将上述反应后的含氯化汞和氯化铜的混合溶液取出25mL,滴入0.2mol/L硝酸银溶液20mL,恰好使其中的氯离子全部转为沉淀。计算:
(1)原氯化汞溶液的物质的量的浓度;
(2)反应后铜片上铜、汞的质量各为多少克?
(3)反应后混合溶液中氯化汞与氧化铜的物质的量浓度各为多少?
B组
[6].不能使溶液中Hg22+还原的是
A Cu B Ag C Fe D Au
[7].在一光洁的紫铜片上滴上一滴硝酸汞溶液,充分反应后,用酒精灯烘烤留下的液体直至烘干。以下说法和实验现象不符合事实的是
A 铜片恢复至光亮的紫红色 B 加热时有金属(汞)蒸气逸出
C 铜片上留有黑色的斑点 D 加热时有水蒸气逸出
[8].给盛有少量硝酸汞的试管加热长时间,最后试管中
A 无剩余物 B 留下少量白色硝酸汞
C 留下银白色汞 D 留下红色氧化汞
[9].已知下列两个反应,前者比后者更易发生①NH3+H+=NH4+ ②2NH3+Ag+=[Ag(NH3)2]+,欲从银氨溶液中转化出大量Ag+,适宜的试剂是
A H2SO4 B HNO3 C HCl D NaOH
[10].三种金属离子的溶液,进行下列实验:

符合上述情况的三种金属离子是
A Cu2+、Ag+、Al3+ B Cu2+、Ag+、Zn2+ C Ag+、Ba2+、A13+
D Ca2+、Hg2+、A13+ E Hg2+、Ba2+、Mg2+
[11].有100mL Cu(NO3)2、AgNO3混合液,其中[NO3-]=4mol/L,加入一定量Zn,充分反应,生成沉淀24.8g,此沉淀不与HCl反应,过滤出的滤液不与BaCl2溶液反应,向滤液中加入过量的NaOH溶液,有沉淀析出,过滤后将固体灼烧至恒重,称得质量为4g。则原加入Zn的质量为[提示:Zn(OH)2可溶于NaOH溶液]
A 6.5g B 13.0g C 11.7g D 9.75g
[12].如果一种元素在一种无机化合物中呈现不同的化合价(严格讲,是氧化态),则该无机化合物称为混合价态化合物。AgO是一种混合价态化合物,其中,银的化合价是 。下列物质Al2O3、Fe3O4、CuO、Mn5O8、CO2,其中属于混合价态化合物的是 。
[13].室温下为液态的金属是 (填汉字名称)。电解它的一价金属的硝酸盐溶液时,阴极得到的产物是该金属的单质。当阴极消耗2mol该盐的正离子时,阳极可得1mol的气体产物,则此气体的产物是 (填分子式)。由此可推断得知该盐的化学式是_______(填化学式)。其阴极上所发生的还原反应方程式是:________________________。
[14].在浅色衣服上作一洗不掉记号的一种方法是:用含Ag(NH3)2+液书写,并立即用热熨斗灼热书写的部位,记号得以固定。要去掉这个记号时,用浓KI液处理记号,然后用水洗涤。请回答作记号和去掉记号时各发生了什么化学反应?
[15].指出液态金属(如汞)的特性,并阐明金属键的正确性。
[16].某工厂的污水中含有Fe3+、Cu2+、Hg2+等离子,为了充分利用资源和保护环境,需要回收污水中的铜和汞。请你设计一个回收的实验方案,要求写明简要的操作步骤和有关的化学方程式或离子方程式。
[17].取一小块钠,用纸擦干,放入盛有少量汞的研钵中,小心研磨得液态钠汞合金(以NaHg表示),均分成一份。
(1)把一份放入试管中,加少量水,搅拌。实验现象是:释出少量氢气,液体物质(指含汞部分)体积未见明显改变,最终留下的汞在管底。
(2)把另一份放入试管中,加少量饱和NH4Cl溶液,搅拌。实验现象是:有气体释出,液态物质膨胀,最终在管底留有汞。
写出反应式。
[18].闻名世界的八大公害之一的水俣病,主要是重金属 污染造成的。那么海洋中的污染物是通过生态系统的 进入人体的。这种重金属在海水和鱼体中哪个浓度大 。人长期食用由于海水、湖水中含有重金属离子而中毒的鱼,会吸入重金属积聚体内,可引起中毒,其原因是金属离子如Hg2+等,能使含有巯基的蛋白酶(酶(SH)2)失去活性,产生汞中毒,临床常用一种解毒剂,如二巯基丙醇(CH2(SH)—CH(SH)—CH2(OH))可以解毒使蛋白酶恢复活性。试用有关化学反应解释这种现象:
①
②
[19].重金属能引起污染的有汞、镉、铅、铬、钒、钴、钡等,其中以汞的毒性最大。在汞蒸气浓度为10-5kg/m3的空气中停留一两天人就会中毒,因此水银温度计车间必须采取措施防止汞中毒。
(1)万一不慎将汞撒落在工作台上或地面上,可以用硫黄粉覆盖,反应的化学方程式为 。
(2)室内有汞蒸气时应该通风以降低汞的浓度,通风口装在墙的 比装在墙的 效率高,这是因为
(3)液态汞的蒸气压与温度的关系式为lgp=a-b/T a=7.08,b=3190,p的单位为kPa,打碎一根温度计会洒失0.5g Hg,某温度计厂一车间空间为 30m3,若在288K时不慎打破了一根水银温度计,试通过计算判断在该车间工作是否合会导致汞蒸汽中毒。
[20].现有下列化学试剂:浓氨水、NaCl溶液、KI溶液、Na2S溶液、KCN溶液。选用适合的试剂填空:
(1)AgNO3溶液 白色沉淀
白色沉淀 无色透明溶液
无色透明溶液 黄色沉淀
黄色沉淀 无色透明溶液
无色透明溶液 黑色沉淀。
黑色沉淀。
(2)离子方程式(按顺序):
[21].已知AgCl、Ag2O都可溶于氨水中,现有化合物A的较浓的溶液,取等量分别盛放在a、b两只试管中,分别加入少量的AgNO3溶液都出现白色沉淀。在a试管中加入稀HNO3后沉淀不溶解,而在b试管中滴加几滴浓NaOH溶液,振荡后沉淀立即溶解;由此推断A是 ,试用离子方程式及简要的文字说明你作出这种判断的理由 。
[22].唐代医书《外合秘要》中制造“水银霜”的方法是把硫和水银共炒,加食盐后放在铁盘中,用盆扣紧,在盘下用火烧,最后在盆内壁上得到洁白的水银霜,这种“水银霜”是 ,生成它的化学方程式是 。
[23].汞与次氯酸(摩尔比1︰1)发生反应,得到2种反应产物,其一是水。该反应的方程式为 ;反应得到的含汞产物的中文名称为 。
[24].有一固体混合物可能含有NaF、FeCl3、NaNO2、Ca(OH)2、AgNO3、CuCl2、NH4Cl七种物质中的若干种。若将此混合物加水后,可得白色沉淀和无色溶液。过滤分离,在此无色溶液中加KSCN没有变化;无色溶液可使酸化后的KMnO4溶液紫色褪去;白色沉淀可溶于NH3·H2O中。根据上述现象指出:
(1)哪些物质肯定存在。
(2)哪些物质可能存在。
(3)哪些物质肯定不存在。
[25].根据《本草纲目》有关记载:“水银乃至阴之毒物,因火煅丹砂而出,加以盐、(明)矾而为轻粉(Hg2Cl2),加以硫磺升而为银朱”。写出主要化学反应方程式。
[26].银以游离态单质银或以硫化矿(如Ag2S)的形式存在于自然界。无论以何种形式存在的银矿,都可用氰化钠溶液浸取,而获得银氰配合物的溶液,再在溶液中用锌还原即可得粗银。试写出上述有关的三个配平的化学方程式。
[27].工业上生产银的方法是NaCN浸取硫化矿,再用锌置换出银,写出化学反应方程式。
[28].从金矿中提取金,传统的也是效率极高的方法是氰化法。氰化法提金是在氧存在下氰化物盐类可以溶解金。试写出配平的化学方程式。
[29].做银镜实验时需要用的银氨溶液,必须临用时配制。这是由于久置的银氨溶液常析出黑色的氮化银沉淀。写出并配平这一反应式,并说明“久置”为什么会析出氮化银。
[30].将银币溶于硝酸中制取AgNO3,结果发现溶液略带蓝色,试判断银币中掺有何种金属?欲得到纯AgNO3晶体,你准备怎样实验?将你的设想用化学方程式表示出来,并辅以必要的文字说明。(已知AgNO3晶体在温度控制在200℃~300℃之间时,不会分解)
[31].根据下列所列的反应和现象,写出A、B、C、D、E、F、G、H、I、J的分子式,并写出①~⑥的化学反应方程式和D的热分解方程式。
①A(红色固体) B(液体)+C(无色气体)
B(液体)+C(无色气体)
②B+HNO3→D(溶液)+E(无色气体)+H2O
③C+E→F(红棕色气体)
④D(溶液)+G(溶液)→H(红色沉淀)(G的焰色反应呈紫色)
⑤H+G(溶液、过量)→I(无色溶液)
⑥C十G溶液)+H+→J(棕黄色溶液)(写出离子方程式)
J通淀粉溶液变蓝色
[32].某不活泼金属 X在氯气中燃烧的产物Y溶于盐酸得黄色溶液,蒸发结晶,得到黄色晶体Z,其中 X的质量分数为50%。在500mL浓度为0.10mol/L的Y水溶液中投入锌片,反应结束时固体的质量比反应前增加4.95g。
X是 ;Y是 ;Z是 。
推理过程如下:
[33].A是最高价氧化物的水合物,其成酸元素X位于ⅥA族,在A中的质量分数为54.5%。A的浓溶液与金属B反应,可得C和X的氧化物D。已知金属B在C中呈+3价,87.0g A与足量的B反应,最终可生成82.3g C。若将A和B在盐酸介质中反应,可生成D和E。已知E中阴离子呈平面正方形,B位于正方形中心。
(1)写出A~E的化学式:A_________;B________;C_______;D_______;E_______;
(2)写出A+B→C+D;A+B+HCl→D+E的化学反应方程式。
(3)A+B+HCl→D+E反应中,可能会有一种气体单质产生。该单质是什么?为什么?
[34].1.176g的盐A溶于少量水中,向所得溶液中加入过量的硝酸钙溶液,结果析出含钙51.33%的沉淀0.362g。然后向滤液中加入稍过量的乙酸钠浓溶液,得到白色沉淀B(沉淀认为是定量进行的,在溶解度表里此物质被指明微溶)。向物质B的吡啶(Py)溶液中加入过量脱水剂(CH3CO)2O,反应结果得到一种沉淀物,它是物质C与可以小心地蒸馏的吡啶的加合物。在150℃下于氩气中物质C分解,并伴有爆炸。此时,生成1.028g的固体残留物和567mL(18℃,98.925kPa)的气体化合物D。固体残留物在空气中锻烧时,其质量减少了0.028g,并生成气体E。气体D在空气中燃烧也生成气体E,E的体积是气体D原有体积的3倍(在同一条件下)。
试确定A~E的所有物质,并写出所进行的反应方程式。
C组
[35].HgF2有强烈的水解性,即使在2mol·dm-3 HF中水解度高达80%,生成HgO和HF。
HgCl2溶于水,只发生极弱的水解作用,25℃0.0078mol·dm-3HgCl2的水解度为1.4%;
HgF2水解性明显强于HgCl2、HgBr2的可能原因是:
[36].做过银镜反应实验的试管,可以用铁盐溶液洗涤,这是因为Fe3+与Ag发生可逆反应:Fe3++Ag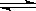 Fe2++Ag+
Fe2++Ag+
(1)若使该平衡向右移动,应采取的措施是:____________________________
(2)c(Fe3+)相同的FeCl3,Fe2(SO4两种溶液,洗涤效果最好的是___________,原因是:_________________________________________________________________________
(3)有人认为Fe(NO3)3溶液也可以做洗涤剂,因为发生反应:3Ag+NO3-+4H+=Ag++NO↑+2H2O。你认为H+是由什么反应提供的(用离子方程式表示)。
[37].地球化学家用实验证实,金矿常与磁铁矿共生的原因是:在高温高压的水溶液(即所谓“热液”)里,金的存在形式是[AuS-]络离子,在溶液接近中性时,它遇到Fe2+离子会发生反应,同时沉积出磁铁矿和金矿,试写出配平的化学方程式。
[38].把Hg(NO3)2滴入KI和把KI滴入Hg(NO3)2所看到的现象是一样的:首先,刚滴入的溶液附近出现红色沉淀,但一振荡便消失了。后来,继续滴入溶液便产生红色沉淀。试予以解释。
[39].汞是一种重要的化学元素。试根据下列问题写出化学反应方程式。
(1)HgO能与足量的CH3SH反应,生成两种等物质的量的产物,其中一种物质既能与酸性氧化物反应,又能与碱性氧化物反应。
(2)HgCl2的强氨性溶液在NaCN水溶液的介质中与等量的SeO2混合,并通入SO2,可得到一种二元化合物A。A为紫黑色晶体,其结构为立方ZnS型。将反应后的溶液分成两等分,一份逐滴加入酸化的AgNO3溶液,有白色沉淀生成,摇动溶液,沉淀又溶解;另一份中加入酸化的BaCl2溶液,也有白色沉淀生成。
[40].白银首饰和器皿以其洁白素雅,光泽好而深受人们喜爱。但银器使用日久逐渐变黑而失去美丽的外观。对变黑的银器多用抛光的方法使之恢复光泽,但这样黑绣中的银也随之损失掉。一种化学除银黑锈的简便方法是:配制含小苏打和食盐的稀溶液于铝容器内,将变黑银器浸入溶液中,并使银器与铝容器接触,放置一段时间后,黑锈就会褪去,而银却极少损失,试问:
(1)银器表面的黑锈是
(2)写出除锈的化学反应方程式。
(3)叙述上述反应的过程(尽可能以反应式表达)。
[41].把(NH4)2CO3浓溶液逐滴滴入AgNO3稀溶液中,开始时出现浑浊,其后逐渐成为无色透明溶液。试回答:
(1)试述出现上述现象的主要原因;
(2)若向得到的透明溶液中加入过量的稀盐酸,试述发生的现象,并写出有关的离子反应方程式。
[42].白色固体溶于水后得到无色溶液A。向A中加入氢氧化钠溶液得到黄色沉淀B,B不溶于过量的氢氧化钠溶液。B溶于盐酸又得到A,向A中滴加少量氯化亚锡溶液有白色沉淀C生成。用过量碘化钾溶液处理C得到黑色沉淀D和无色溶液E。向无色溶液E中通入硫化氢气体得到黑色沉淀F,F不溶于硝酸。将F溶于王水后得到黄色沉淀已无色溶液H和气体I,I可使酸性高锰酸钾溶液褪色。请写出A、B、C、D、E、F、G、H、I所代表的化合物或离子。
[43].向无色溶液A中加人HI溶液,有无色气体B和黄色沉淀C生成,C在KCN溶液中部分溶解得到无色溶液D,向D中通入H2S时析出黑色沉淀E,E不溶于浓盐酸。若问A中加入KI溶液,有黄色沉淀F生成,将F投入KCN溶液则F全部溶解。请写出A、B、C.D、E、F所代表的物质。
[44].无色晶体A溶于水后加入盐酸得到白色沉淀B。分离后将B溶于Na2S2O3溶液得到无色溶液C。向C中加入盐酸得到白色沉淀混合物D和无色气体E。E与碘水作用后转化为无色溶液F。向A的水溶液中滴加少量Na2S2O3溶液立即生成白色沉淀G,该沉淀由白变黄、变橙、变棕最后转化为黑色,说明有H生成。请写出A、B、C、D、E、F、G、H所代表的化合物或离子,并写出有关反应的化学方程式。
[45].(1)废定影液中含Na3Ag(S2O3)2和未反应的Na2S2O3,请拟出废定影液再生和回收银的方案。(提示:AgCl易溶于Na2S2O3溶液,AgBr能溶于Na2S2O3溶液,AgI能溶于一定浓度的Na2S2O3溶液,而Ag2S不溶于Na2S2O3溶液)
(2)用再生的定影液定影的照片有“发花”的现象,即使是再生条件掌握得很好的定影液,用不多久(和新鲜配制的定影液相比)也会出现“发花”的现象。为什么?
[46].照相时若曝光不足,则已显影和定影的黑白底片图像淡薄,需对其进行“加厚”;若曝光过度,则需对图像进行“减薄”。
(1)加厚的一种方法是:把底片放入由硝酸铅、赤血盐溶于水配成的溶液,取出,洗净,再用硫化钠溶液处理。写出底片图像加厚的反应方程式;
(2)减薄的一种方法是:按一定比例混合硫代硫酸钠溶液和赤血盐溶液,把欲减薄的底片用水充分湿润后没入,适当减薄后,取出冲洗干净。写出底片图像减薄的反应方程式;
(3)如底片经过加厚处理后,图像仍不够明显,能否再次用以上方法继续加厚?又经减薄后的底片,能否再次用以上方法减薄?说明理由。
[47].化合物A为白色固体,不溶于水。A受热剧烈分解,生成固体B和气体C。固体B不溶于水或盐酸,但溶于热的稀硝酸得无色溶液D和无色气体E,E在空气中变棕色。向溶液D中加人盐酸时得到白色沉淀F。气体C与普通试剂不起反应,但与热的金属镁作用生成白色固体G。G与水作用得到白色沉淀H及气体I,I能使湿润的红色石蕊试纸变蓝。H可溶于稀硫酸,得到溶液J。化合物A以H2S溶液处理时得到黑色沉淀K、无色溶液L和气体C。过滤后,固体K溶于浓硝酸得到气体E、黄色沉淀M和溶液D。用NaOH溶液处理滤液L,又得到气体I。
请指出A、B、C、D、E、F、G、H、I、J、K、L、M所代表的物质的化学式,并写出有关反应的化学方程式。
[48].向无色溶液A中加入过量硝酸时有白色沉淀B和无色溶液C生成。向C中加入过量铜粉得到蓝色溶液D并放出红棕色气体E。浓缩溶液D,颜色逐渐变黄,最后析出浅棕色晶体;晶体与稀硫酸反应得到蓝色溶液并有白色沉淀F析出。
(1)试确定B、E、F各代表何种物质?
(2)浓缩D时,溶液为什么变黄色?
(3)溶液C中除H+外,还可能有哪两种阳离子?
[49].白色固体A为三种硝酸盐的混合物,进行如下实验:
(1)取少量固体A溶于水后,加入NaCl溶液,有白色沉淀生成。
(2)将(1)的沉淀离心分离,离心液分成三份:一份加入少量Na2SO4,有白色沉淀生成;第二份加入K2CrO4溶液,有黄色沉淀生成;第三份加入NaClO有棕黑色沉淀生成。
(3)在(1)所得的沉淀中加入过量氨水,白色沉淀部分溶解,部分转化为灰白色沉淀。
(4)在(3)所得的离心液中加入过量的硝酸,又有白色沉淀产生。
试确定A中含哪三种硝酸盐,并写出实验(2)、(3)的有关反应的化学方程式。
[50].周期表中汞与锌、铜等元素同族,试回答以下问题:
(1)写出汞原子的核外电子排布式;
(2)化合物中汞常为+1价或+2价,而+1价汞以二聚体形式存在,如Hg2Cl2,Hg2(NO3)2等。试用电子式表示Hg2Cl2和Hg2(NO3)2的结构,并说明Hg2Cl2分子的形状;
(3)已知下列电对的标准电极电势。ΦøHg2+/Hg22+=0.905V,ΦøHg22+/Hg=0.799,ΦøAg+/Ag=0.800V,ΦøCu2+/Cu=0.340V。试判断:Ag与Hg(NO3)2溶液能否反应?若能,则写出反应的离子方程式。若不能,则说明理由;
(4)写出过量汞与稀硝酸反应的化学方程式;
(5)周期表中Tl与B、Al、Ga、In同族,Tl在化合物中有+3和+1价,而Tl3+有强氧化性,Tl+则较稳定,这是由于什么原因?
[51].从含金、银、铜、铂的金属废料中提取金、银、铂的一种工艺如下图所示:
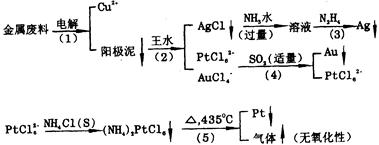
(1)电解时,以纯铜为阴极,金属废料为阳极,CuSO4溶液作为电解液,说明为何铜能够与金、银、铂分离?
(2)写出阳极泥用王水(一体积浓HNO3与三体积浓盐酸的混合物)处理的化学反应方程式。
(3)写出图中(3)示步骤的离子反应方程式。
(4)写出图中(4)示步骤的离子反应方程式。
(5)(NH4)2PtCl6沉淀加热到435℃,只留下金属铂,写出此步的化学反应方程式。
[52].黄金的提取通常采用氰化氧化法。
(1)该法是向含氰化钠(NaCN)的矿粉(Au粉)混合液中鼓入空气,将金转移到溶液中,再用锌粉还原提取Au。请写出反应过程的离子方程式,计算反应的平衡常数。
已知:EyAu+/Au=1.68V,EyO2/OH-=0.401V,EyZn2+/Zn=-0.77V,K稳Au(CN)2-=2.0×1038,K稳Zn(CN)42-=1.0×1016
(2)纯度达99.95%~99.98%的黄金可用AuCl3的盐酸溶液进行电解制取,有证据表明,AuCl3在浓盐酸中是以[H9O4]+[AuCl4]-存在,请写出H9O4+的结构式。
(3)为了富集AuCl3,常用含磷酸三丁酯的苯溶液萃取,请说明其中原理。
(4)为保护环境,必须对废水进行处理,请设计两个原理不同的处理方案,比较它们的优缺点。
[53].金属金常常可以在铝硅酸盐岩石中发现,它很细地分散在其他矿物之中。通过暴露在空气中的氰化钠溶液处理破碎后的矿石来提取,在这个过程中金慢慢地转变成可溶于水的Au[(CN)2]-(反应1)。达到平衡后,被泵出的水相用锌与金的配合物反应转化为金属金,而锌则转变成Zn[(CN)4]2-(反应2)
(1)写出反应(l)和(2)的配平的离子方程式。
金在自然界中经常和银形成合金,银也可以被暴露在空气中的氰化钠溶液氢化。
(2)500L 0.0100mol/L的Au[(CN)2]-和0.0030mol/L的Ag[(CN)2]-的溶液经蒸发掉三分之一体积的液体后用锌处理(40 g)。假设偏离标准条件是不重要的,而且所有的氧化还原反应都进行到底了,试计算在反应停止后Au[(CN)2]-和Ag[(CN)2]-的浓度。已知:
Zn[(CN)4]2-+2e→ Zn+4CN- Eo=-1.26V
Au[(CN)2]-+e→Au+2CN- Eo=-0.60V
Ag[(CN)2]-+e→Ag+2CN- Eo=0.31V
(3)Au[(CN)2]-在一定条件下是很稳定的络合物。欲使99%的金在溶液中以该氰配合物的形式存在,问需要多大浓度的氰化钠?已知:Au[(CN)2]-:Kf=4×1028
(4)已经发展了另一些提取金的方法来代替氰化法,为什么?选择一个答案
A 氰化钠溶液腐蚀采矿机械
B 氰化钠流失在地下水中会生成氢化氰,后者对许多动物是有毒的
C 用氰化法得到的金是不纯的
[54].周期表中汞与锌、镉等元素同族,试回答以下问题:
(1)写出汞原子的核外电子排布式;
(2)化合物中汞常为+1价或+2价,而+1价汞以二聚体形式存在,如Hg2Cl2,Hg2(NO3)2等。试用电子式表示Hg2Cl2和Hg2(NO3)2的结构,并说明Hg2Cl2分子的形状;
(3)已知下列电对的标准电极电势。ΦøHg2+/Hg22+=0.905V,ΦøHg22+/Hg=0.799,ΦøAg+/Ag=0.800V,ΦøCu2+/Cu=0.340V。试判断:Ag与Hg(NO3)2溶液能否反应?若能,则写出反应的离子方程式。若不能,则说明理由;
(4)写出过量汞与稀硝酸反应的化学方程式;
参考答案(A3)
[1] C
[2] C
[3] B
[4] (1)0.3mol (2)36% (3)V(NO)︰V(NO2)=2︰1
[5] (1)0.08mol/L (2)Cu:74.365g;Hg:2.005g (3)0.04mol/L
[6] B、D
[7] A
[8] A
[9] B
[10] A、D
[11] D
[12] +3和+1;Fe3O4,Mn5O8
[13] 汞 O2 Hg 2(NO3)2 Hg22++2e-=2Hg
[14] 作记号时,Ag(NH3)2灼热分解成微细的Ag;去掉记号时,Ag与KI及空气中氧反应生成溶解度很小的AgI,可被水漂去。
[15] 因为液态或固态金属原子轨道上的电子的能量很接近,基本上是连续的,所以金属能够吸收和反射各种波长的光从而呈现出金属的光泽性。金属具有导电性和导热性是由于金属中电子的快速运动的结果。液态金属的流动性是由于在金属晶体中只有一种电子且其键是非定域的。
[16] 此题可分4步完成,反应方程式略
①取污水加过量的铁粉,充分搅拌后过滤,可得滤渣。
②用足量盐酸洗涤滤渣,过滤,再用水洗涤滤渣,即得Cu、Hg的固体混合物。
③加热Cu、Hg混合物,汞变为蒸气,冷却回收汞。同时Cu变为CuO。
④用氢气还原CuO,回收Cu。
[17] (1)2NaHg+2H2O=2NaOH+2Hg+H2↑
(2)NaHg+NH4Cl=NH4Hg+NaCl 2NH4Hg=2Hg+2NH3+H2↑
[18] 汞 食物链 鱼 ①Hg2+与酶(SH)2反应:Hg2++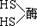 →
→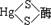 +2H+而中毒;②与
+2H+而中毒;②与 反应而解毒:
反应而解毒: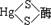 +
+ →
→ +
+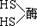
[19] (1)Hg+S=HgS
(2)下部 上部 汞蒸气比空气密度大
(3)8.3×10-6 kg/m3 不会导致中毒
[20] (1)NaCl溶液;浓氨水;KI溶液;KCN溶液;Na2S溶液
(2)①Ag++Cl-=AgCl↓ ②AgCl+2NH3=[Ag(NH3)2]++Cl-
③[Ag(NH3)2]++I-=AgI↓+2NH3 ④AgI+2CN-=[Ag(CN)2]-+I-
⑤2[Ag(CN)2]-+Na2S=Ag2S+4CN-
[21] NH4Cl 略
[22] 升汞HgCl2 Hg+S=HgS↓ HgS+2NaCl=HgCl2+Na2S
[23] 2Hg+2HClO=Hg2OCl2+H2O 碱式氯化汞(或氯氧化汞)
注:Hg2OCl2也可写成HgO·HgCl2或HgCl2·HgO
[24] (1)NaNO2、AgNO3、NH4Cl (2)NaF (3)FeCl3、Ca(OH)2、CuCl2
[25] HgS+O2=Hg+SO2
12Hg+12NaCl+4KAl(SO4)2+3O2=6Hg2Cl2+6Na2SO4+2K2SO4+2Al2O3
Hg+S=HgS
[26] 4Ag+8NaCN+2H2O+O2=4Na[Ag(CN)2]+4NaOH
Ag2S+4NaCN=2Na[Ag(CN)2]+Na2S Zn+2Na[Ag(CN)2]=Na2[Zn(CN)4]+2Ag↓
[27] Ag2S+4NaCN=2Na[Ag(CN)2]+Na2S 2Na[Ag(CN)2]+Zn=Na2[Zn(CN)4]+2Ag
[28] 4Au+8NaCN+2H2O+O2=4NaAu(CN)2+4NaOH
[29] 3Ag(NH3)2OH=5NH3+3H2O+Ag3N
由于NH3的挥发使平衡向右移动,促进Ag3N的生成
[30] 显蓝色说明银币中掺有金属铜。将含有Cu(NO3)2的AgNO3溶液蒸干,加热到200~300℃,这时Cu(NO3)2分解成CuO,而在此温度下,AgNO3不分解,用水溶解AgNO3,滤掉不溶的CuO,重结晶得AgNO3晶体。
[31] A:HgO;B:Hg;C:O2; D:Hg(NO3)2;E:NO;
F;NO2;G:KI;H:HgI2;I:K2[HgI4];J:I2
①2HgO 2Hg+O2↑
2Hg+O2↑
②2Hg+8HNO3=3Hg(NO3)2+2NO+4H2O
③2NO+O2=2NO2
④Hg(NO3)2+2KI=HgI2+2KNO3
⑤HgI2+2KI=K2[HgI4]
⑥4I-+O2+4H+=2I2+2H2O(或6I-+O2+4H+=2I3-+2H2O)
[32] X是Au Y是 AuCl3 Z是HAuCl4·3H2O
[33] (1)A:H2SeO4;B:Au;C:Au2(SeO4)3;D:SeO2;E:H[AuCl4];
(2)6H2SeO4+2Au→Au2(SeO4)2+3SeO2+6H2O
3H2SeO4+8HCl+2Au→2HAuCl4+6H2O+3SeO2
(3)Cl2;因为H2SeO4是一种氧化性酸。同时HAuCl4生成后,增强了Au的还原性,氧化还原反应增强,此时H2SeO4会把Cl-氧化成Cl2。
[34] A中加入Ca(NO3)2,有难溶性钙盐沉淀可初步推知:A中的阴离子为弱酸根离子,再由滤液中加太浓NaAc有微溶物B产生,并向B中加Py及(CH3CO)2O对有爆炸性物质产生的特点,推断A中阳离子可能为Ag+,再定量计算印证A为AgF所以:
A:AgF B:CH3COOAg C:Ag2C2O D:C3O2 E:CO2
反应为:2AgF+Ca(NO3)2=2AgNO3+CaF2↓ AgNO3+CH3COONa=NaNO3+CH3COOAg↓ 2CH3COOAg+(CH3CO)2O+Py=Ag2C2O·Py+3CH3COOH 2Ag2C2O=4Ag+C+C3O2 C+O2=CO2 C3O2+2O2=3CO2
[35] HgF2溶于水发生双水解,所以有较强的水解作用。 HgCl2、HgBr2水解性弱是HgCl2、HgBr2难电离(或Hg2+和Cl-、Br-结合力强)之故。HgBr2水解度更小,表明HgBr2比HgCl2更难电离(或Hg2+与Br-的键的共价性强于Hg2+和Cl-,HgBr2更难溶)
[36] (1)增大c(Fe3+)或降低c(Ag+)
(2)FeCl3;因为AgCl难溶,Ag2SO4微溶。因此在Fe3+将Ag氧化为Ag+后,Ag+与Cl-反应产生AgCl沉淀,c(Ag+)被降低的程度大,更有利于使平衡向右移动。
(3)Fe3++3H2O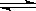 Fe(OH)3+3H+
Fe(OH)3+3H+
[37] 2AuS-+3Fe2++4H2O=2Au+Fe3O4+2H2S+4H+
[38] (1)把Hg(NO3)2滴入KI溶液,KI过量。在滴入的Hg2+暂时局部过量时,产生红色的HgI2沉淀。一旦溶液摇匀,HgI2与过量的I-反应,生成[HgI4]2-络离子;继续滴入Hg(NO3)2,直至游离的I-“完全耗尽”,则[HgI4]2-将与满入的Hg2+反应,又生成红色的HgI2沉淀。
(2)把KI滴入Hg(NO3)2溶液,Hg(NO3)2过量,而在I-暂时局部过量时,会产生红色的HgI2沉淀。一旦溶液摇匀,HgI2与过量的Hg2+反应,生成[HgI]+络离子;继续加入I-,直至游离的Hg2+“完全耗尽”,则[HgI]+将与滴入的I-反应,生成红色的HgI2沉淀。
[39] (1)HgO+2CH3SH=Hg(SCH3)2+H2O;
(2)HgCl2+8NH3+SeO2+3SO2+4H2O=HgSe↓+2NH4Cl+3(NH4)2SO4;(5分)
[40] (1)Ag2S
(2)Al+3Ag2S+6H2O=6Ag+2Al(OH)3+3H2S(2Al+3Ag2S+6H2O+3NaHCO3=6Ag+2Al(OH)3+3H2CO3+3NaHS)
(3)利用电化学原理去锈——负极:2Al-6e=2Al3+;正极:3Ag2S+6e=6Ag+3S2-;2Al3++3S2-十6H2O=2Al(OH)3+3H2S(①首先必须准确地判断黑锈的成分,否则,将会全题皆错。同学们容易想到Ag2O和Ag2S两种物质,它们都是黑色的,且都可能在Ag与空气接触过程中产生。是哪一种呢?需要比较二者的稳定性,Ag2S比Ag2O稳定得多,Ag2O很不稳定,稍加热即会分解,如果是AgO的话,也用不着采用如此复杂的方法来去锈,加热就行了。故黑锈为Ag2S。②银器与铝器接触一段时间后黑锈褪去,银却很少损失。说明反应中生成了单质银,当然,还原剂就是Al。那么,生成什么呢?显然,Al失去电子会生成Al3+,Ag2S中的Ag+被还原生成Ag后,S2-进入溶液;Al3+与S2-不能共存,会发生双水解而生成Al(OH)3和H2S,H2CO3与H2S的Ka1相差不大,生成的H2S也可能跟溶液中的HCO3-作用,生成 H2CO3和H2S。③反应过程会怎样呢?整过程是一个氧化还原反应,小苏打和食盐显然是起电解质的作用,使之形成原电池。故反应为:Al先失去电子生成Al3+,电子传给Ag2S,得到电子生成Ag和S2-,然后Al与S2-发生双水解。
[41] (1)(NH4)2CO3量少时,CO32-与Ag+结合成Ag2CO3沉淀出现浑浊,(NH4)2CO3量多时,水解生成的NH3·H2O与Ag2CO3生成Ag(NH3)2+而变澄清
(2)产生白色沉淀,并逸出无色气体
[Ag(NH3)2]++2H++Cl-=AgCl↓+2NH4+ CO32-+2H+=CO2↑+H2O
[42] A:HgCl2 B:HgO C:Hg2Cl2 D:Hg E:[HgI4]2- F:HgS G:S
H:[HgCl4]2- I:NO
[43] A:[Ag(S2O3)2]3- B:SO2 C:AgI+S D:[Ag(CN)2]- E:Ag2S F:AgI
[44] A:AgNO3 B:AgCl C:[Ag(S2O3)2]3- D:AgCl+S E:SO2 F:H2SO4 G:Ag2S2O3 H:Ag2S
[45] (1)往废定影液中滴加Na2S溶液到不产生沉淀为止:
2Na3Ag(S2O3)2+2Na2S=Ag2S↓+4Na2S2O3
过滤,滤液就是再生定影液,沉淀经洗涤、干燥,在通风橱中加热得到Ag:
Ag2S+O2 Ag+SO2
Ag+SO2
(2)若再生时多加了Na2S,用它定影将和底片上的AgX发生如下反应:2AgX+S2-=Ag2S↓+2X-,“发花”现象是Ag2S造成的。即使再生条件掌握得很好,溶液中有X-离子特别是Br-、I-离子的存在将影响底片上AgBr,尤其是AgI的溶解,也会造成“发花”现象。
[46] (1)加厚:4Ag+4K3Fe(CN)6=Ag4Fe(CN)6+3K2Fe(CN)6
K4Fe(CN)6+2Pb(NO3)2=Pb2Fe(CN)6+4KNO3
用Na2S处理:Ag4Fe(CN)6+2Na2S=2Ag2S↓+Na4Fe(CN)6
Pb2Fe(CN)6+2Na2S=2PbSO4+Na4Fe(CN)6
发生以上反应,增加2mol PbS的黑度。
(2)减薄:4Ag+4K3Fe(CN)6=Ag4Fe(CN)6+3K4Fe(CN)6
Ag4Fe(CN)6+8Na2S2O3=4Na3Ag(S2O3)2+Na4Fe(CN)6
(3)不可能再次加厚,因K3Fe(CN)6氧化不了Ag2S和PbS。但能再次减薄,因K3Fe(CN)6能氧化Ag,Na2S2O3能溶解Ag4Fe(CN)6。
[47] A:AgN3 B:Ag C:N2 D:AgNO3 E:NO F:AgCl\ G:Mg3N2 H:Mg(OH)2 I:NH3 J:MgSO4 K:Ag2S L:(NH4)2S M:S
[48] (1)B:AgCl,E:NO2,F:BaSO4;
(2)有[CuCl4]2-生成,因[CuCl4]2-为黄色;
(3)还可能有NH4+和Ba2+
[49] AgNO3、Pb(NO3)2、Hg2(NO3)2
[50] (1)1s22s22p63s23p63d104s24p64d104f145s25p65d106s2或[Xe]4f145d106s2
(2)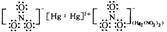
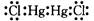 (Cl-Hg-Hg-Cl)直线型
(Cl-Hg-Hg-Cl)直线型
(3)能 2Ag+2Hg2+=2Ag++Hg22+
(4)6Hg(过量)+8HNO3=3Hg2(NO3)2+2NO↑十4H2O
(5)惰性电子对效应。或答镧系收缩导致6s2较为稳定,难于参加成键
[51] (1)根据金属活动性顺序(或标准电极电势),Cu最先失去电子,以Cu2+进入溶液,而Au、Ag、Pt从阳极上脱落,形成阳极促泥。
(2)3Ag+3HCl+HNO3=3AgCl↓+NO↑+2H2O
Au+4HCl+HNO3=H[AuCl4]+NO↑+2H2O
3Pt+18HCl+4HNO3=3H2[PtCl6]+4NO↑+8H2O
(3)4[Ag(NH3)2]++N2H4+4OH-=4Ag↓+N2↑+8NH3+4H2O
(4)2[AuCl4]-+3SO2+6H2O=2Au↓+3HSO4-+8Cl-+9H+
(5)3(NH4)2PtCl6=3Pt+2NH3↑+2N2↑+18HCl↑
[52] (1)4Au+8CN-+2H2O+O2=4Au(CN)2-+4OH- 3.10×1066
2Au(CN)2-+Zn=2Au+Zn(CN)42- K=2.8×1022
(2)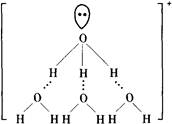 或
或
(3)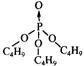 +
+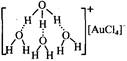 →
→
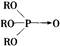 与[H9O4]+形成氢键,螫合效应,-OR基亲油,进入苯溶液,富集[AuCl4]-
与[H9O4]+形成氢键,螫合效应,-OR基亲油,进入苯溶液,富集[AuCl4]-
(4)①络合沉淀法:Fe2++6CN- Fe(CN)64-
Fe(CN)64- Fe4[Fe(CN)6]3↓
Fe4[Fe(CN)6]3↓
优点:成本低;缺点:二次污染。
②氧化法:CN-+OH- CNO-→CO2+N2
CNO-→CO2+N2
优点:处理彻底;缺点:成本高。
[53] (1)4Au+8CN-+O2+2H2O=4[Au(CN)2]-+4OH-
Zn+2[Au(CN)2]-=[Zn(CN)4]2-+2Au
(2)E0(Ag/Zn)=-0.31-(-1.26)=0.95V E0(Au/Zn)=-0.60-(-1.26)=0.66V E0(Ag/Zn)>E0(Au/Zn),所以Ag(Ⅰ)络合物先还原。
①molAg(Ⅰ)在500mL中=500×0.0030=1.5mol
②molAu(Ⅰ)在500mL中=500×0.010=5.0mol
③mol Zn在40g中=40/65.38=0.61mol
0.61mol Zn消耗1.2mol[Ag(CN)2]- 剩余的[Ag(CN)2]-=1.5-1.2=0.3mol
[Au(CN)2]-不会被还原。 反应停止时[Au(CN)2]-的浓度=0.010×3=0.030M
反应停止时[Ag(CN)2]-的浓度=0.3×3/500=0.002 M
(3)Au++2CN-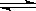 [Au(CN)2]- Kf=4×1028
[Au(CN)2]- Kf=4×1028
[Au(CN)2-]/{[Au+]+[Au(CN)2-]}=99/100
[Au+]=[Au(CN)2-]/99 [CN-]=5×10-14 M
(4)B
[54] (1)1s22s22p63s23p63d104s24p64d104f145s25p65d106s2或[Xe]4f145d106s2
(2)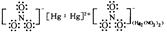
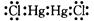 (Cl-Hg-Hg-Cl)直线型
(Cl-Hg-Hg-Cl)直线型
(3)能 2Ag+2Hg2+=2Ag++Hg22+
(4)6Hg(过量)+8HNO3=3Hg2(NO3)2+2NO↑十4H2O
