
紫外线消毒效果验证方案
方案编号:V-SOP-015-01
生效日期: 年 月 日

实施
实施日期: 年 月 日
目 录
一、目的................................................................................................................................ 3
二、 范围.............................................................................................................................. 3
三、 验证小组成员及其职责.................................................................................................. 3
四、 培训.............................................................................................................................. 3
五、 相关法规或文件的符合性.............................................................................................. 4
六、 设备描述....................................................................................................................... 4
1. 设备功能描述............................................................................................................. 4
2. 设备参数描述............................................................................................................. 4
七、 确认前准备................................................................................................................... 4
八、 验证内容....................................................................................................................... 5
1.1设计确认................................................................................................................... 5
1.2安装确认................................................................................................................... 5
1.3 运行确认.................................................................................................................. 5
1.4 性能确认.................................................................................................................. 5
九、 偏差及偏差处理............................................................................................................ 5
十、 完成验证报告................................................................................................................ 5
十一、 验证结果评审............................................................................................................ 5
十二、 验证文件变更历史及归档........................................................................................... 5
十三、 附件.......................................................................................................................... 6
一、 目的
本方案为确认紫外线灭菌灯能够对物体表面进行有效的消毒而进行验证。进入净化车间的零配件或其它物品通过传递窗活,进入微生物室的物品通过传递窗,经过紫外消毒后进入微生物室。为了确认传递窗紫外灯的消毒效果,特起草方案对其进行验证。本验证用于生产车间、微生物室、无菌室传递窗、车间物料缓冲间的紫外灯表面消毒效果检查。
验证过程应严格按照本方案规定的内容进行,若因特殊原因确需变更时,应填写验证方案变更申请及批准书,报验证委员会批准。
二、 验证小组成员及其职责
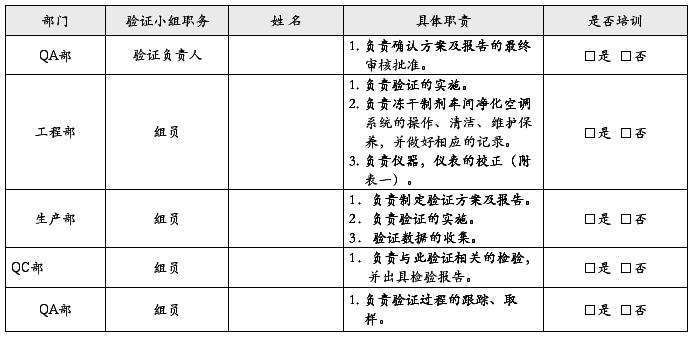
三、培训
验证小组组长应在本确认方案批准后组织对本确认小组成员及其相关操作人员进行本确认方案及确认与本方案相关 SOP、技术资料的专项培训,并确保所有参加本次确认工作的人都已悉知本方案及相关 SOP、技术资料的要求。
四、相关法规或文件的符合性
《药品生产验证指南》(20##年版)
《药品生产质量管理规范》(20##年修订版)
洁净厂房设计规范 GB50073-2001
五、功能描述
1. 设备功能描述:
紫外线灭菌灯(简称紫外灯)主要用于洁净工作台、层流罩、物料传递窗、物料传递间或洁净室空气和物体表面的消毒。紫外线波长为136~390nm,以253.7nm的杀菌力最强,但紫外线穿透力极弱,只适用于表面杀菌。紫外灯的杀菌力度随使用时间增加而减退,以点燃100h的输出功率为额定输出功率,把紫外灯点到70%额定功率的点灯时间定为平均寿命,紫外灯使用超过平均寿命时,就达不到预期效果,则必须更换,国产紫外灯“平均寿命一般为2000h。紫外灯通常按相对湿度为60%的基准设计,室内湿度增加时,照射量应相应增加。紫外线强度要求在操作面上达40uW/cm2 以上。
六、确认前准备
1. 文件资料确认
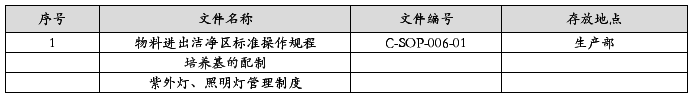
2. 仪器、试剂的准备:
2.1. 仪器
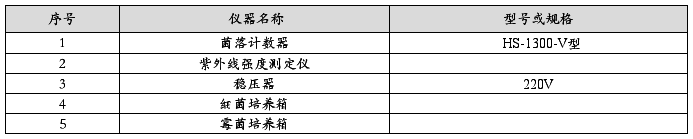
2.2. 器材
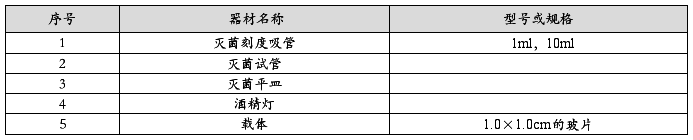
2.3. 试剂
2.3.1. 营养肉汤培养基
2.3.2. 改良马丁培养基
2.3.3. 金黄色葡萄球菌[CMCC(B)26 003]
2.3.4. 枯草芽孢杆菌[CMCC(B)63 501]
2.3.5. 大肠杆菌[CMCC(B)44 102]
2.3.6. 白色念珠菌[CMCC(F)98 001]
2.3.7. 稀释液(0.1%吐温80,0.1%蛋白胨溶液)
2.3.8. 枯草杆菌黑色变种(ATTC 9372)芽孢黑曲霉(ATTC16404)等细胞及其芽孢和真菌悬液及菌片。
2.4. 紫外线照度计。
3. 培养基的制备:

4. 方法验证试验
4.1. 辐照强度测定:开启紫外灯5min后,用中心波长为253.7nm的紫外线强度测定仪在灯管下方垂直1.5m处分别测量其辐照度值(uW/cm2)。
4.2. 测量时,电压应稳定在220V。
4.3. 普通型或低臭氧型直管紫外线灯(30W),在灯管下方垂直1.5m的中心处,新灯管的辐照度值应≥90 uW/cm2 。使用中的灯管的辐照度值应≥70 uW/cm2 ,低于此值者应予更换。
4.4. 照射剂量:表面消毒接受的照射剂量,应达杀灭目标微生物所需。对大肠杆菌,照射剂量应达到7.5×103 uW·s/cm2,对金黄色葡萄球、白色念珠菌、枯草芽孢杆菌应达到2.53×104uW·s/cm2。
4.5. 照射剂量计算:
照射剂量(uW·s/cm2 )=紫外灯管强度(uW/cm2)×时间(s)
根据照射剂量确定物品的放置位置与紫外灯的照射时间。
细菌及其芽孢和真菌杀灭效果的测定
5. 菌液的制备

5.1. 金黄色葡萄球菌、枯草芽孢杆菌、大肠杆菌、白色念珠菌培养后,将菌液进行活菌计数。
5.2. 将灭菌载体平放于灭菌平皿内,每个载体滴注定量菌悬液,(载体回收菌量达5×105~5×106 cfu/片),涂匀,放37℃培养箱烘干备用。
5.3. 开启紫外灯5min后,将16个染菌玻片平放于灭菌平皿内,水平放于距紫外1.5m、处照射,于4个不同间隔时间(15min、30 min、45 min、60 min)各取出4个染菌玻片,分别投入4个盛有5ml洗脱液试管中,振打80次。
5.4. 经适当稀释后,取1ml洗脱液,作平板倾注,每个染菌玻片接种两个,细菌放30~35℃培养48小时作活菌计数,真菌放23~28℃培养72小时作活菌计数。
5.5. 阳性对照,除不做照射处理外,取4个染菌玻片,分别投入4个盛有5ml洗脱液试管中,振打80次。培养按5.4同样操作。
5.6. 计算杀灭率
阳性对照回收菌数-试验组回收菌数
 杀灭率(%)= ×100%
杀灭率(%)= ×100%
阳性对照回收菌数
5.7. 判定标准 对指示菌杀灭率≥99.9%判为消毒合格。
验证结果记录:试验菌数量测定原始记录
七、偏差及偏差处理
1. 验证方案与实际情况不符,或者无法执行时,需要及时修改验证方案。
2. 当验证数据没有达到预期结果时,分析数据偏离程度,并确定:是否进行重复实验;是否扩大数据偏离范围;是否需要重新校正测量仪器、方法等。
3. 偏差及偏差处理必须如实、详细记录在验证报告中。
八、完成验证报告:
1. 整理总结验证过程各项验证、试验结果记录。
2. 拟定日常监测程序及验证周期。
3. 验证结果评定与结论。
九、验证结果评审:
验证委员会负责对验证结果进行综合评审,做出验证结论。
十、验证文件变更历史及归档:
1. 变更历史
2. 由验证小组组长负责整理记录及报告,交QA部存档。
十一、附件
附表一 仪器仪表校验记录

检查人: 日期:
第二篇:75%乙醇、0.1%新洁尔灭消毒效果验证方案
苏州万庆药业有限公司 QC-VAL-535-01
75%乙醇、0.1%新洁尔灭
消毒效果验证方案
验证编号:QC-VAL-535-01
苏州万庆药业有限公司
20xx年11月
苏州万庆药业有限公司 QC-VAL-535-01
验证方案确定
苏州万庆药业有限公司 QC-VAL-535-01
目 录
1. 验证方案介绍、目的、范围、相关文件··································································································1
2. 验证准备. ·····························································································································································1
3. 验证内容·······························································································································································3
4. 变更与偏差 ··························································································································································7
5. 验证结论 ·····························································································································································8
6. 附件·······································································································································································8
7. 参考文献 ·····························································································································································8
苏州万庆药业有限公司 QC-VAL-535-01

1. 验证方案简介、目的、范围、相关文件 1.1验证方案简介:
本验证共分三部分:
1.1.1 第一部分是对验证方案的介绍,包括验证目的、范围以及相关验证、文件的介绍。 1.1.2 第二部分是验证的相关内容: 75%乙醇及0.1%新洁尔灭的喷洒消毒效果试验。验证在微生
物实验室阳性菌对照室完成。
1.1.3 第三部分是验证结论及再验证。 1.2 目的
通过喷洒消毒的方法验证75%乙醇及0.1%新洁尔灭在实验室条件下对各种载体上已知菌的消毒效果,为其正确使用提供保障。 1.3 范围
本验证方案适用于本公司微生物实验室及其他洁净环境需要外表面清洁消毒的物料。
1.4
2. 验证准备 2.1试验仪器和设备
苏州万庆药业有限公司 QC-VAL-535-01
2.2 试验用品
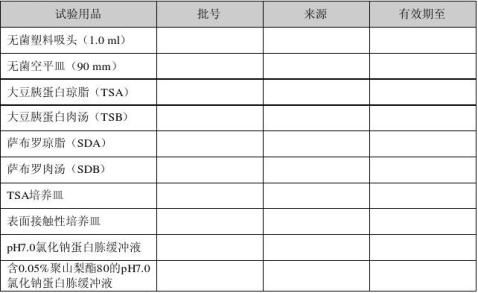
2.3 菌种及菌液
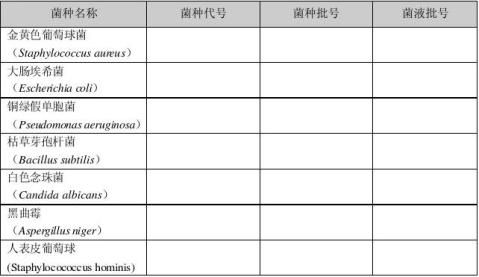
苏州万庆药业有限公司 QC-VAL-535-01
2.4 消毒剂
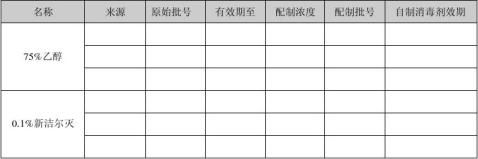
2.5载体
软塑料(自封袋、取样袋),硬质塑料(桶、校验仪器外壳、喷壶、计算器、写字板),不锈钢(桶、盒、器具),纸张(标示卡),玻璃(玻璃瓶),洁净服面料(布袋),橡胶(橡胶手套),铝合金。
3. 验证内容 3.1菌液制备:
3.1.1将金黄色葡萄球菌、大肠埃希菌、铜绿假单胞菌接种至大豆胰蛋白肉汤培养基(TSB)中,在30~
35℃培养18~24小时;枯草芽孢杆菌划线接种至大豆胰蛋白琼脂培养基(TSA)上,在30~35℃培养18~24小时后洗脱琼脂表面菌苔;白色念珠菌接种于萨布罗葡萄糖肉汤培养基(SDB)中,在20~25℃培养48~72小时;黑曲霉菌划线接种至萨布罗葡萄糖琼脂培养基(SDA)上,在20~25℃培养5~7天,洗脱琼脂表面孢子;吸取金黄色葡萄球菌、大肠埃希菌、铜绿假单胞菌、枯草芽孢杆菌增菌后的培养物各1ml加入到9ml pH7.0氯化钠蛋白胨缓冲液中,充分混匀后作为10-1稀释级,依次10倍稀释至10-7稀释级计数确认菌数,同时预留10-2稀释级作为菌片制备使用;吸取白色念珠菌增菌后的培养物及黑曲霉孢子液各1ml加入到9ml pH7.0氯化钠蛋白胨缓冲液中,充分混匀后作为10-1稀释级,依次10倍稀释至10-5稀释级计数确认菌数,同时预留浓菌液作为菌片制备使用。
3.1.2菌液计数:吸取1ml上述菌液置无菌空平皿中,倾倒温度不超过45℃的TSA或SDA培养基,平
行倾到2个平板,细菌用TSA培养基在30-35℃培养72h 后观察最终结果,真菌用SDA培养基在 20-25℃培养5天后观察最终结果。
苏州万庆药业有限公司 QC-VAL-535-01
3.1.3菌液计数结果:

3.2菌片的制备:
3.2.1试验中使用的菌片是以菌悬液滴加于载体上制成。载体是根据消毒对象选择常用材质如软塑料
(自封袋、取样袋),硬质塑料(桶、校验仪器外壳、喷壶、计算器、写字板),不锈钢(桶、盒、器具),纸张(标示卡),玻璃(玻璃瓶),洁净服面料(布袋),橡胶(橡胶手套),铝合金,规格均为5×5cm;
3.2.2所用载体于染菌前,应进行脱脂处理。脱脂方法如下:①将载体放在含肥皂的水中煮沸30 min;
②而后以自来水洗净;③用纯化水煮沸10 min;④用纯化水漂洗;⑤晾干备用。
3.2.3载体经压力蒸汽灭菌(耐湿热灭菌载体)或用75%乙醇浸泡消毒后晾干(不耐湿热灭菌载体),
统一使用滴染法:将经灭菌的载体片平铺于无菌平皿内,逐片滴加菌液。菌液滴加量每片为0.1ml,细菌选择10-2稀释级,真菌选择原菌液。用精密移液器接无菌吸头,滴染菌液,并用接种环涂匀整个载体表面。滴染菌液后置室温下自然阴干后再使用。每种菌对应的一种载体制备4片。
注:菌片含菌量应为5×10cfu/片。 3.3菌片菌数确定:
3.3.1取一片已制备好的金黄色葡萄球菌、大肠埃希菌、铜绿假单胞菌、枯草芽孢杆菌、人表皮葡萄
球菌菌片,完全浸泡于100ml pH7.0氯化钠蛋白胨缓冲液中反复荡洗15分钟,将此荡洗液作为10-2稀释级,然后吸取1ml荡洗液加入到9ml pH7.0氯化钠蛋白胨缓冲液中,混匀作为10-3稀释级,同法再进行10倍至10稀释级,吸取1ml置无菌空平皿中,倾倒融化的温度不超过45℃的TSA培养基,平行倾到2个平板,先置于在20-25℃培养3 天,再置于30-35℃培养2天,观察最终结果;取一片已制备好的白色念珠菌菌片,完全浸泡于100ml pH7.0氯化钠蛋白胨缓冲液中反复荡洗15分钟,将此荡洗液作为10-2稀释级,然后吸取1ml荡洗液加入到9ml pH7.0氯化钠蛋白胨缓冲液中,混匀作为10-3稀释级,同法再进行10倍至10-4稀释级,吸取1ml置无
-5
3-4
苏州万庆药业有限公司 QC-VAL-535-01
菌空平皿中,倾倒融化的温度不超过45℃的TSA培养基,平行倾到2个平板,先置于在20-25℃培养3 天,再置于30-35℃培养2天,观察最终结果;取一片已制备好的黑曲霉菌片,完全浸泡于100ml 含0.05%聚山梨酯80的pH7.0氯化钠蛋白胨缓冲液中反复荡洗15分钟,将此荡洗液作为10-2稀释级,然后吸取1ml荡洗液加入到9ml 含0.05%聚山梨酯80的pH7.0氯化钠蛋白胨缓冲液中,充分混匀后作为10稀释级,吸取1ml置无菌空平皿中,倾倒融化的温度不超过45℃的TSA培养基,平行倾到2个平板,先置于在20-25℃培养3天,再置于30-35℃培养2天,观察最终结果。
3.3.2菌片菌数确定结果:
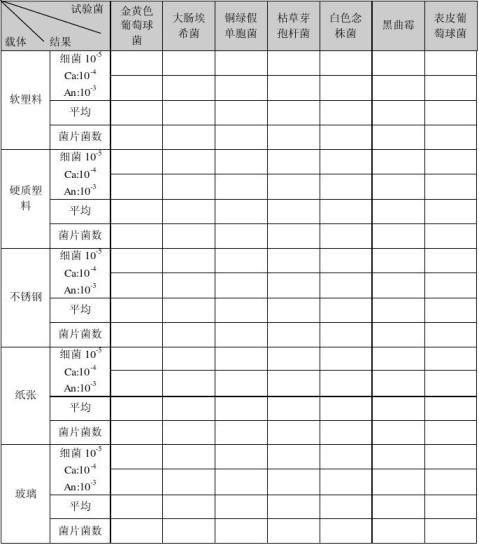
-3
苏州万庆药业有限公司 QC-VAL-535-01
3.3.3合格标准:回收菌片的含菌量应应不小于10cfu/片。
3.4载体喷洒消毒杀菌效力试验:
3.4.1选择常用于喷洒消毒的物料材质进行试验。
3.4.2每种菌所染菌片应分开进行试验,试验时,每种载体菌片各取 1片,每次喷雾量于实际试验操
作要求一致且距离和压力保持相同,使喷到物料载体上的雾粒大小和数量一致。
3.4.3待喷洒载体表面充分挥发至干。
3.4.4按照QC510-04洁净区表面的微生物监测程序对平整光滑的表面进行接触碟取样。
3.4.5接触碟取样:取样时打开碟盖,使无菌培养基表面与取样表面直接接触,均匀按压接触碟底板,
确保全部琼脂表面与取样点表面均匀接触10秒钟左右,再盖上碟盖,做好标记;接触碟先在20~25℃培养箱培养 3天,然后在 30~35℃培养箱培养 2天,观察最终结果。
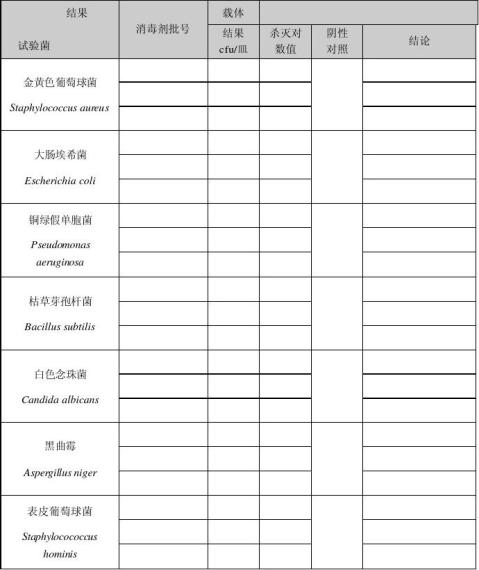
3.4.6 试验重复3 次 ,计数各组的活菌量(cfu/片),计算杀灭对数值。(结果保留到小数点后两位)
杀灭对数值=试验前菌片活菌浓度的对数值-试验后菌片活菌浓度的对数值
3.4.7合格标准:要求各次试验的杀灭对数值均≥3,可判定消毒合格。
3.4.8载体擦拭消毒杀菌效力试验结果:(载体:软塑料,硬质塑料,不锈钢,纸张,玻璃,洁净服面
料,橡胶,铝合金。)
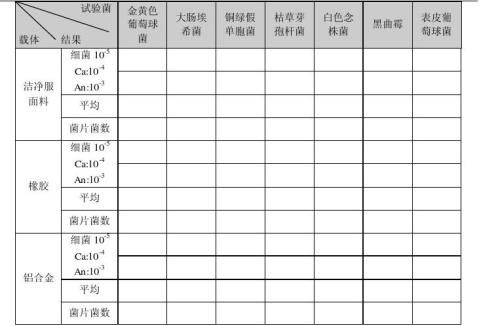
5
苏州万庆药业有限公司 QC-VAL-535-01
4.变更与偏差
4.1在执行验证过程中,检测人员需要及时记录出现的任何偏差,并按照相关操作规程处理。
4.2本验证方案批准实施之后,任何的变更需要按照相关操作规定,由申请人提出书面申请,交由验证
小组审核,批准之后,方能执行变更。
苏州万庆药业有限公司 QC-VAL-535-01
5. 验证结论
5.1验证完成之后,汇总所有检测数据,进行统计分析。由验证部门起草验证报告,总结验证结论,并
交由相关部门审核,批准。
5.2当检测数据满足下列规定时,方可认为验证合格:
5.3统计数据表明所有的检测数据均在规定的范围内;
5.4如果检测数据不符合规定标准,经偏差调查发现是由与验证人员无关的因素造成的,并经审核批准。
6.附件
6.1原始记录1菌液制备;
6.2原始记录2载体制备;
6.3原始记录3载体菌片制备;
6.4原始记录4载体喷洒消毒杀菌效力试验;
6.5原始记录5消毒剂配制;
7.参考文献:
7.1中华人民共和国国家标准,消毒与灭菌效果的评价方法与标准;
Evaluating method and standard for the efficacy of disinfection and sterilization;
GB 15981一1995
7.2消毒技术规范;Technical Standard For disinfection;中华人民共和国卫生部(2002 年版);
2002.11.
