实验 血糖的测定(葡萄糖氧化酶法)
【目的】
1. 了解葡萄糖氧化酶法测定血糖的原理,能进行血糖测定的操作。
2. 掌握血糖测定的临床意义。
【原理】
葡萄糖氧化酶 (GOD) 能将葡萄糖氧化为葡萄糖酸和过氧化氢。后者在过氧化物酶 (POD)作用下,分解为水和氧的同时将无色的4-氨基安替比林与酚氧化缩合生成红色的醌类化合物,其颜色的深浅在一定范围内与葡萄糖浓度成正比,在500nm波长处测定吸光度,与标准管比较可计算出血糖的浓度。反应式如下:
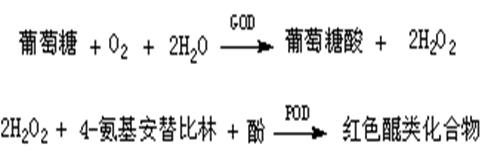
【器材】
试管、吸管、试管架、恒温水浴箱、分光光度计
【试剂】
1. 0.1mol/L磷酸盐缓冲液(pH7.0) 称取无水磷酸氢二钠8.67g及无水磷酸二氢钾5.3g溶于800ml蒸馏水中,用1mol/L氢氧化钠(或1mol/L盐酸)调节pH至7.0,然后用蒸馏水稀释至1L。
2. 酶试剂 称取过氧化物酶1200U,葡萄糖氧化酶1200U,4-氨基安替比林10mg,叠氮钠100mg,溶于上述磷酸盐缓冲液80ml中,用1mol/L NaOH调pH至7.0,加磷酸缓冲液至100ml。置冰箱保存,4℃可稳定3个月。
3. 酚溶液 称取重蒸馏酚100mg溶于100ml蒸馏水中(酚在空气中易氧化成红色,可先配成500g/L的溶液,贮存于棕色瓶中,用时稀释),用棕色瓶贮存。
4. 酶酚混合试剂 取上述酶试剂与酚溶液等量混合,4℃可以存放一个月。
5. 12mmol/L苯甲酸溶液 溶解苯甲酸1.4g于蒸馏水约800ml中,加温助溶,冷却后加蒸馏水至1L。
6.葡萄糖标准贮存液(100mmol/L) 称取已干燥恒重的无水葡萄糖1.802g,溶于12mmol/L苯甲酸溶液约70ml中,并移入100ml容量瓶内,再以12mmol/L苯甲酸溶液加至100ml。
7.葡萄糖标准应用液(5mmol/L) 吸取葡萄糖标准贮存液5.0ml 于100ml 容量瓶中,加12mmol/L 苯甲酸溶液至刻度。
【操作】
取3 支试管,编号,按下表操作。
表 血糖测定操作步骤

混匀,置 37 ℃水浴中保温 15分钟,在波长 505nm 处比色,以空白管调零,读取标准管及测定管吸光度。
【计算】血清葡萄糖(mmol/L) =( 测定管吸光度/标准管吸光度) × 5.55
【正常参考范围】
3.9~6.1mmol/L
【临床意义】
1. 生理性高血糖 可见于摄入高糖饮食或注射葡萄糖后,或精神紧张、交感神经兴奋,肾上腺分泌增加时。
2. 病理性高血糖
⑴糖尿病:病理性高血糖常见于胰岛素绝对或相对不足的糖尿病患者。
⑵对抗胰岛素的激素分泌过多:如甲状腺功能亢进、肾上腺皮质功能及髓质功能亢进、腺垂体功能亢进、胰岛α-细胞瘤等。
⑶颅内压增高:颅内压增高(如颅外伤、颅内出血、脑膜炎等)刺激血糖中枢,出现高血糖。
⑷脱水引起的高血糖:如呕吐、腹泻和高热等也可使血糖轻度增高。
3. 生理性低血糖 饥饿或剧烈运动、注射胰岛素或口服降血糖药过量。
4. 病理性低血糖
⑴胰岛素分泌过多:由胰岛β细胞增生或胰岛β细胞瘤等引起。
⑵对抗胰岛素的激素分泌不足:如腺垂体功能减退、肾上腺皮质功能减退和甲状腺功能减退等。
⑶严重肝病患者:肝贮存糖原及糖异生功能低下,不能有效调节血糖。
【结果及分析】
【思考题】
1. 血糖有哪些来源和去路,机体是如何调节血糖浓度恒定的?
第二篇:16-第十六次课-实验二 7-21分光光度计的使用 血糖的测定
郑州铁路职业技术学院教师教案
序号 16

实验二 721分光光度计的使用
[目的]
了解分光光度法的基本原理,熟悉721分光光度计的操作方法,为今后使用该仪器奠定基础。
[原理]

分光光度法(Spectrophotography)是利用物质特有的吸收光谱来鉴别物质或测定其含量的一种技术。光线是一种电磁波。其中可见光波长范围约由760nm的红色-400nm紫色,波长短于400nm的光线叫做紫外线,长于760nm的光线叫做红外线。当光线通过透明溶液介质时,其中一部分光可透过,一部分光被吸收,这种光波被溶液吸收的现象可用于某些物质的定性及定量分析。
光源 单色器 测量池 接收器
单色器 测量池 接收器
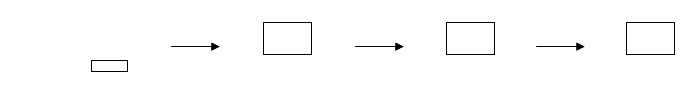
参照池

有色溶液的深浅与其中呈色物质的含量呈正比关系。在定量分析中,利用比较有色物质溶液的颜色深浅来测定物质含量的分析方法称为比色法。被测物质中,有的本身就是有颜色,但多数被测物质本身无色或颜色很浅,须加入某些化学试剂使被测物质与之发生反应生成有色的物质。
物质的颜色是由于物质吸收某种波长的光线后,通过或反射出某种颜色的结果。当一定波长的单色光通过该物质的溶液时,该物质都能有一定程度的吸光作用。浓度越高,对光线吸收就越多,利用物质对一定波长光线吸收的程度测定物质含量的方法,称为分光光度法。
分光光度法依据朗伯-比耳(Lamber-Beer)定律。设一束单色光I0射入溶液,由于部分光线被溶液吸收,通过光线为It,则It/ I0之比为透光度,若透光度为T(%),则
T= It/ I0×100%
透光度 (T)的倒数(1/T)反应了物质对光的吸收程度。实际应用中,取1/T的对数值,做为吸光度(A),即
A=Lg(1/T)=-Lg T
依据朗伯-比耳(Lamber-Beer)定律推倒,当一束平行单色光通过均匀、无散射现象的溶液时,在单色光强度、溶液温度等条件不变的条件下,溶液对光的吸光度(A)与溶液的浓度(C)及溶液层厚度(L)的乘积成正比。即
A=KCL
在实验比色时,标准液与被测液使用相同的比色杯,即液层厚度(L)相同,K为常数。所以,溶液对光吸光度(A)与其浓度(C)之间的关系即为正比关系,溶液浓度越大,吸光度越大。
可以通过测定吸光度求待测溶液的浓度。
设:测定液的吸光度和浓度分别为A测和C测,标准液的吸光度和浓度分别为A标和C标,计算公式为
A测:A标=C测:C标
上式中C标为已知,A测和A标可在比色时读出数值,把这些数值代入公式,即可测出测定液的浓度。
[实验仪器和药品]
721-分光光度计;吸管;试管;蒸馏水;标准液(硫酸铜);待测液(硫酸铜).
[721-分光光度计的使用]
1. 接通电源,打开开关指示钮,打开比色箱盖。
2. 选择所需波长(630nm)、转动灵敏度旋钮选择适宜灵敏度。
3. 转动0旋钮,使检流针对准T为0,将空白液、标准液、测定液分别倒入3个比色杯中,将比色杯放入比色盒,再将比色盒放入比色箱中,使空白液对准光路,合上比色箱盖。
4. 转动100旋钮,使检流指针对准T为100%(A为0)。预热20分钟,观察指针是否稳定。
5. 预热后,反复几次调节T=0、T= 100%,即开盖调“0”,闭盖调“100”。
6. 轻轻拉动比色槽拉杆,先后将标准液、测定液对准光路,分别记录A标数值和A测数值。
7. 比色完毕,关闭电源拔下插头,恢复各旋钮至原来位置,取出比色杯,合上比色箱盖。将比色杯洗净后倒置晾干。
8. 计算:根据记录的A测、A标和已知的C标3个数值。
C测=A测/A标×C标公式算出C测数值。
【注意事项】
1.波长可选择(400~650)nm之间
2.向比色杯加入比色液时,比色杯应保持干燥,否则会导致比色液稀释
3.所加液体的量:比色杯高度的(1/2 ~2/3)
4.比色杯光面朝向光源
5.手不能触摸比色杯的光面;有液体污染时可用软布擦干
6.比色后,应将比色液倒掉,然后用自来水、蒸馏水冲洗比色杯,倒置干燥
实验现象及结果
实验三 血糖浓度测定
【目的要求】
了解氧化酶测定血糖的基本原理,掌握氧化酶法测定血糖的实验方法及临床意义。
【实验原理】
血中的葡萄糖与酶酚混合液反应,生成有色物质,其颜色的深浅与葡萄糖的含量成正比,与同样处理的葡萄糖标准液比色,测定红色化合物的吸光度则可计算血糖浓度。整个反应可简单表示如下:
葡萄糖氧化酶
 葡萄糖+O2+H2O 葡萄糖酸+H2O2
葡萄糖+O2+H2O 葡萄糖酸+H2O2
过氧化物酶
 H2O2+苯酚+4-氨基安替比林 红色化合物+H2O
H2O2+苯酚+4-氨基安替比林 红色化合物+H2O
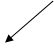 同样处理(酶酚混合液)
同样处理(酶酚混合液)

 血糖(G) 有色溶液(红色)
血糖(G) 有色溶液(红色)
 葡萄糖标准液 有色溶液(红色)
葡萄糖标准液 有色溶液(红色)
【实验用品】
血清、葡萄糖标准液(5.55mmol/L)、酶工作液(酶酚混合液)、滴管、试管、试管架、微量吸液器、恒温水浴、72-1型分光光度计。
【实验方法】
1、取试管3支,按下表操作:
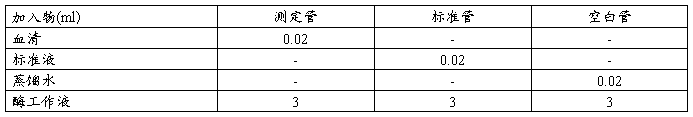
2、将上述各管混匀后放入恒温水浴(37℃)中加热12分钟,注意在恒水浴中的水面必须高于试管内的液面,否则温度不均而影响比色。
3、用波长500nm分光光度计进行比色,空白调节零点,读取测定管与标准管吸光度。
4、计算
血糖(mmol/L)=测定管吸光度/标准管吸光度×5.55
5、参考正常值:3.89-6.11mmol/L
【思考题】
讨论血糖升高和降低的临床意义及其维持恒定的因素?
