实验三、分馏实验
一、实验目的
1.了解分馏的原理和意义,蒸馏与分馏的区别,分馏的种类及特点;
2.掌握实验室分馏的操作方法。
二、实验原理
1.分馏的概念
沸点不同但可互溶的液体混合物,通过在分馏柱中多次的汽化-冷凝,从而使沸点相近的混合物得到分离,这个过程称为分馏。简单地说,分馏就是多次的蒸馏。
注:当两种或者三种液体混合物以一定比例混合,可组成具有固定沸点的混合物,将这种混合物加热至沸腾时,在气液平衡体系中,气相组成和液相组成一样,故不能使用分馏法将其分离出来,只能得到按一定比例组成的混合物,这种混合物称为共沸混合物。共沸混合物有固定的组成和沸点,不能通过分馏的方法分离。
2.分馏的原理
当混合物蒸气进入分馏柱中时,由于柱外空气的冷却,蒸汽中高沸点组分易被冷凝回流入烧瓶中,故上升的蒸气中低沸点组分就会相对地增多,当冷凝液回流途中,遇到上升的蒸气时,二者之间进行热交换,使冷凝液中低沸点组分再次受热汽化,高沸点仍呈液态回流,通过多次的汽化-冷凝-回流等程序,当分馏柱的效率相当高且操作正确时,在分馏柱顶部出来的蒸气就越接近于纯低沸点组分,而烧瓶里残留的几乎是纯高沸点组分,最终使沸点相近的两组分得到较好的分离。
简言之,分馏柱的作用就是使高沸点组分回流,低沸点组分得到蒸馏的仪器装置。分馏的用途就是分离沸点相近的多组分液体混合物。
三、仪器和药品
四、实验步骤
1、分馏装置及安装
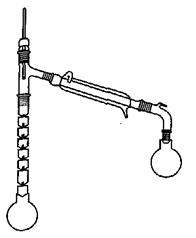

2、主要试剂用量
沸石(2~3粒), 丙酮与水按1:1的比例混合(30 mL)
3、操作步骤
⑴加料:往圆底烧瓶内加入丙酮与水混合液30 mL,2~3粒。
⑵通冷凝水。
⑶加热:适当控制加热速度,以1-2滴/秒为宜。
⑷收集:用量筒收集馏出液。
⑸读数:注意温度计、量筒的读数与有效数字。
⑹分馏完毕,先停止加热再停止通水,拆卸仪器,其程序与装配时相反。
五、实验结果
丙酮与水混合物的分馏数据记录表

用坐标纸作图(以馏出液体积为横坐标,温度为纵坐标作图)
第二篇:蒸馏和分馏实验比较
实验 2 蒸馏和分馏实验比较
(丙酮—水混合物分离)
实验讲解前提问:
1.分馏装置由几部分组成?与蒸馏比较有何不同
2.分馏的主要目的
一、实验目的:
(1)理解蒸馏和分馏的基本原理,应用范围,什么情况下用蒸馏,什么情况下用分馏。
(2)熟练掌握蒸馏装置的安装和使用方法。
(3)掌握分馏柱的工作原理和常压下的简单分馏操作方法。
蒸馏和分馏的基本原理是一样的,都是利用有机物质的沸点不同,在蒸馏过程中低沸点的组分先蒸出,高沸点的组分后蒸出,从而达到分离提纯的目的。不同的是,分馏是借助于分馏柱使一系列的蒸馏不需多次重复,一次得以完成的蒸馏(分馏就是多次蒸馏),应用范围也不同,蒸馏时混合液体中各组分的沸点要相差30℃以上,才可以进行分离,而要彻底分离沸点要相差110℃以上。分馏可使沸点相近的互溶液体混合物(甚至沸点仅相差1-2℃)得到分离和纯化。
二、实验原理
蒸馏——将液态物质加热到沸腾变为蒸气,又将蒸气冷凝为液体的联合操作过程。用蒸馏方法分离混合组分时要求被分离组分的沸点差在30℃以上才能达到有效分离或提纯的目的。蒸馏是分离和提线液态有机物常用方法之一;也可用来测量液态物质的沸点(常量法)。
分馏——装置上比蒸馏多一个分馏柱,在分馏柱内反复进行汽气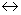 冷凝
冷凝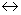 回流过程,相当于是多次的简单蒸馏,最终在分馏柱顶部出来的蒸气为高纯度的低沸点组分,这样能把沸点相差较小的混合组分有效的分离或提纯出来。
回流过程,相当于是多次的简单蒸馏,最终在分馏柱顶部出来的蒸气为高纯度的低沸点组分,这样能把沸点相差较小的混合组分有效的分离或提纯出来。
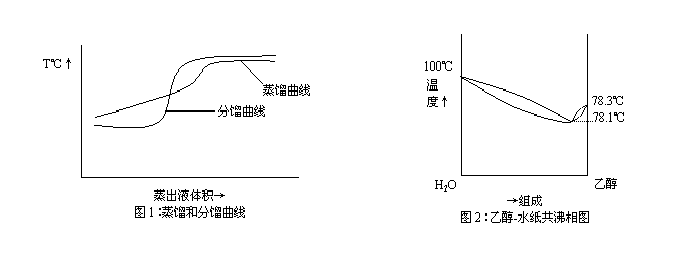
用图1表示蒸馏和分馏的分离效率,能形成共沸混合物的混合物不能用蒸馏或分馏分离或提纯(见图2)。
影响分离效率的因素:
①分馏柱效率——理论塔板数 一块理论塔板相当于一次普通蒸馏的效果
②回流比——回流比越大,分馏效率越好(即馏出液速度太快时分离效果差)
③柱的保温
三、简单的分馏装置和蒸馏装置(略)、冷凝管的选用原则(略)
四、实验步骤
1.按图安装好蒸馏或分馏装置,接受器改用量筒以便读取馏出液体积(两人配合)
2.丙酮—水混合物分馏
3.丙酮—水混合物蒸馏
实验关键:①馏出速度 1滴/1~2秒
②注意平稳加热和分馏柱保温
六、根据记录及结果
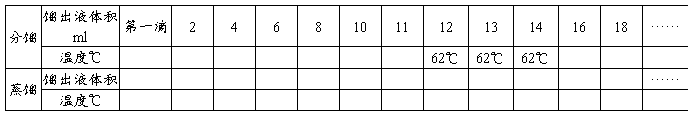
依上表数据在同一坐标上图作分馏曲线和蒸馏曲线
七、结果讨论

