自20##年1月,国家食品药品监管总局开展中药材专业市场进行飞行检查以来,各地食品药品监管部门陆续开展了飞行检查、跟踪检查或专项检查。
据不完全统计,截止至9月30日,今年全国共有82家药品批发或零售连锁企业被撤销或收回GSP认证证书。其中广东数量最多,为43家,占比为52.43%。其次是山东12家、湖北9家、吉林5家、陕西3家,安徽、福建、黑龙江、江西、辽宁各2家。

此外,还有部分企业因严重违规被吊销《药品经营许可证》,失去了药品经营资格。
除在飞行检查或跟踪检查中,被撤销或收回GSP证书的,另有470多家药品批发企业因有效期满未向食品药品监管部门提出换证申请或未通过换证现场检查,而被监管部门依法注销终止药品经营。
现在除了新版GSP认证之外,各地药监局飞行检查、跟踪检查工作日益常态化,相当于随时可能进行的摸底考试,要想不被淘汰,规范经营,时刻警醒,持续做好各项质量管理工作,牢记GSP或许才是关键。
一、被吊销《药品经营许可证》的药品批发企业汇总
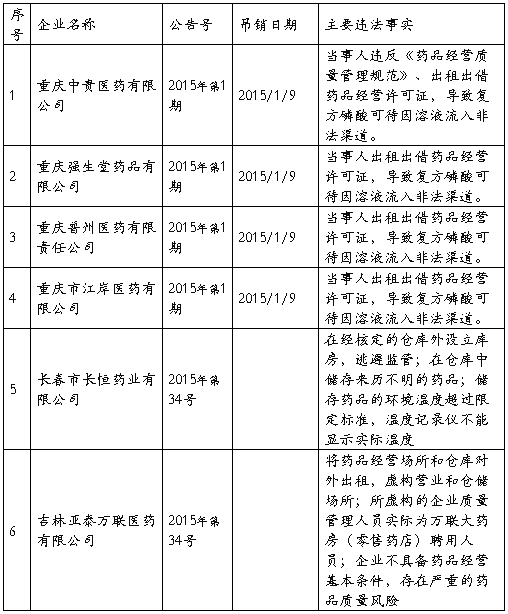
二、被撤销GSP证书的药品批发企业汇总
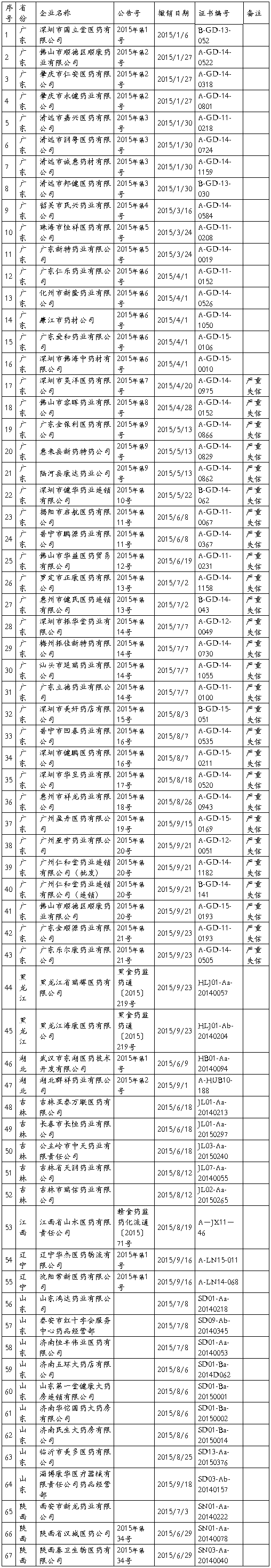
三、被收回GSP证书的药品批发企业汇总
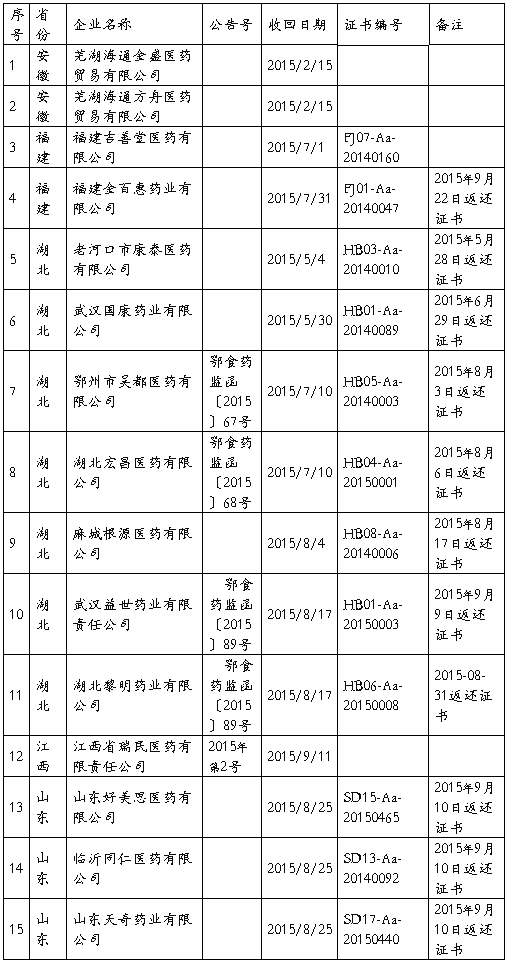
20##年10月13日,陕西省食品药品监督管理局发布通知,经省局跟踪检查或飞行检查,陕西华龙制药有限公司等严重违反《药品生产质量管理规范》规定,依据《药品生产质量管理规范认证管理办法》第三十三条规定,我局依法收回其《药品GMP证书》。
据统计,20##年以来,陕西省已收回4家药品生产企业的GMP证书,分别是:

此外,另有2家企业因兼并重组有关事宜,被陕西省局依法注销原《药品生产许可证》。

一、广东省
广东省食品药品监督管理局撤销GSP认证证书公告(20##年第23号)粤食药监药通〔20##〕134号
广东国安堂大药房有限公司等3家药品经营企业严重违反《药品经营质量管理规范》规定,我局依据《药品经营质量管理规范认证管理办法》第四十五条,依法撤销其《药品经营质量管理规范认证证书》,并根据《广东省食品药品监督管理局药品生产经营单位信用分类管理的实施办法》(粤食药监法〔2014〕109号)规定,评定其信用等级为“严重失信”,现予以公布。
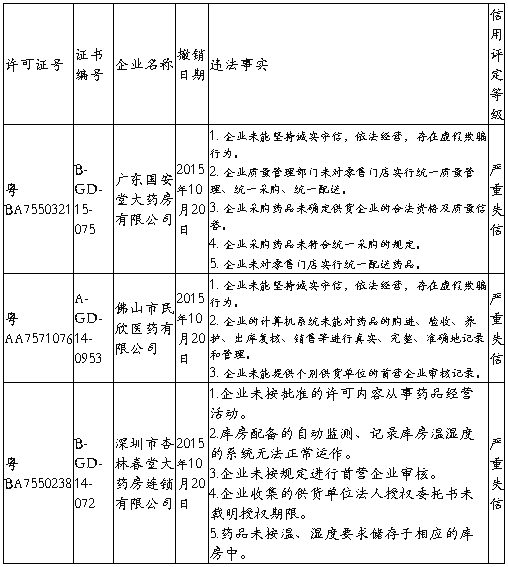
 二、河北省
二、河北省
关于撤销GSP认证证书公告20##年第187号
经飞行检查发现,河北美康太平医药贸易有限公司、唐山高孚医药有限公司严重违反《药品经营质量管理规范》规定,依据《药品医疗器械飞行检查办法》第二十五条、《药品经营质量管理规范认证管理办法》第四十五条规定,我局依法撤销以上两家企业的《药品经营质量管理规范认证证书》,现予以公布。

三、重庆市
关于撤销重庆棠仁阁医药有限公司药品经营质量规范认证证书的公告渝食药监公告〔20##〕25号
重庆棠仁阁医药有限公司严重违反《药品经营质量管理规范》,依据《药品经营质量管理规范认证管理办法》(国食药监市〔2003〕25号)第四十五条规定,我局依法撤销其《药品经营质量管理规范认证证书》,现予以公布。

第二篇:西安国家飞行检查检查点总结
西安国家飞行检查检查点总结 检查企业:
陕西玉龙医药有限公司; 陕西恒生医药有限公司;
西安华协医药有限责任公司;
一、 检查时间:
两天
二、 检查安排:
第一天:客户资质、首营资料、进销存记录、账货相符等。 第二天:冷链专项。
三、 检查概述:
1、 检查组组成:
国家局10人,省、市、区分局陪同8-12人。
2、 检查形式:
进库立刻分散,各人查各人的内容,最后做汇总简报。
3、 检查手段:
手机APP对货物进行扫码。
让企业根据规程进行现场演练操作。
4、 取证办法:
记录问题,手机拍照取证,手机拍照取证时要拍证据
上的企业名称或同时拍企业人员照片。
四、 检查重点:
第一天就不详细说了,就是10个人拿各种资料,然后进会议室后关门核对所有资料。
第二天冷链专项。
1、 检查流程:
A、 进库后让企业提供冷链相关操作规程、验证报
告和企业花名册,根据报告,让验证相关人员(如养护员)进行现场操作,核对操作规程与现场操作是否一致,同时检查操作规程是否符合GSP要求。过程中其他人不得提醒和提供帮助。
B、 要求打印一段时间(要求半年,货量大也可减
少)进销存系统内所有冷链单据,同时在监控系统中调出这段时间的温湿度记录,一条一条对。
C、 报告检查:
a. 查询年度验证计划(必查项);
b. 根据年度验证计划核对本次验证时间及验证项目;
c. 查参与人员签字;
d. 要培训记录及培训内容(要纸质的!);
e. 对参加过培训的人员提问,不许其他人帮忙,主要问题如下:
1) 规范要求的布点原则是什么?
2) 你们企业布点原则是什么?
3) 验证项目你们这次都做了哪些?
4) 项目怎么做的你大概给我描述一下。
5) 根据岗位不同根据操作规程提出一些
问题,主要是跟冷链相关的,比如开门
多长时间,冷链运输最长时间是多少,
路上车坏了怎么办等。
f. 核对报告所使用的校准证书,一张一张核对。 g. 根据报告的结论核对企业操作规程。
2、 检查重点及与我们相关:
A中检查重点是操作规程,与我们相关的就是验证后我们给客户的报告结论,建议根据各地实际情况,将报告整理后给客户一套验证结论。需要注意的是检查员提出“周转箱”的概念,在冷库到冷藏车的运输过程中,一定要有中转的东西,如经过预冷的大泡沫箱等。问过检查组组长整件货怎么办,对方回答是车屁股怼进冷库…….
B中检查重点是“不缺”,既不缺单据,也不缺记录。与我们相关的是在途超标,要有处理痕迹及处理结果,
这点只有我们能做到,别家只能手填。
C中的签字,只有我们的报告有,之前别的第三方的报告都只有一个人的签字,没有参与验证人员的签字。 D中培训过程是必须的,但是要求培训内容要企业质量负责人和验证的第三方共同制定,要有纸质的培训资料存根。这点别的第三方根本不做培训,算一大缺失。
E中提问内容要根据培训来做,西安公司现在的做法是三次培训,通过这次检查感觉效果还不错。首次培训把布点要讲,每个验证步骤要讲,提前跟质量负责人讲清楚,要求参培人员记笔记。验证期间我们要求企业跟一个质管部的人,再跟一个跟验证相关的人员,边做边讲。第三次培训是结论培训,提前跟质管部主管讨论过后,制定企业的操作规程,然后拿操作规程混着我们的验证结论一起培训,我这边做结论培训的时候,企业基本都是质管部和库房全员参加,有几家分管质量的副总也有参加。
F中报告咱们跟志翔的问题不大,检查组认为龙邦的验证报告问题比较大。
3、 本次检查起到作用的文件:
这部分文件我另发附件了,希望能帮到别的分公司。
1) 年度验证计划示例;
年度验证计划示例是我跟用户一起设计的,
西安现在我这边的客户基本都是拿这个范本改的,希望大家帮我完善。
2) 结论总结与操作规程示例。
这个总结就是把报告最后的结论单独拿出
来了,现在我让客户根据企业实际情况和保温箱的格式去出操作规程,效果还不错。
以上是总结的全部内容,水平有限望大家谅解,感谢济南仁硕电子科技有限公司的温湿度监控系统。
