二甲苯和无水乙醇的蒸馏实验
药品:二甲苯、无水乙醇。
仪器:蒸馏烧瓶、蒸馏头、温度计、冷凝管、尾接管、锥形瓶等。 实验步骤:
1、连接好蒸馏所需要的仪器。
2、用50mL量筒分别量取40mL二甲苯和40mL无水乙醇,并转移到蒸馏烧瓶中。加入磁砖子,设置加热器的温度加热。记录第一种馏分的温度范围和体积。
3、待第一种馏分蒸馏完全后,更换接收瓶,收集第二种馏分,记录第二组馏分的温度范围。
实验现象:
刚刚加热时,温度计的读数几乎不变。经过一段时间后,蒸馏烧瓶壁有液滴出现。温度迅速上升,当接收到第一滴馏分时,温度计的读数为74℃。之后温度有所上升,一直上升到78℃不再变化。收集2h多后,蒸汽量明显减少,馏分馏出速度下降,温度计的读数开始缓慢降低。当温度计的读数低于72℃时,不再馏出馏分。温度计的读数下降速度变快,当降低到44℃时,不再下降。经过一段时间后,蒸馏瓶壁有液滴出现,蒸馏头中蒸汽上升,温度计的读数迅速上升,当温度计的读数上升到接近70℃时,仍会有少量的馏分馏出。但此时当温度计的读数继续迅速上升,当上升到124℃时,馏出第一滴馏分,但此时温度计的读数还在上升。当上升到132℃,温度计的读数稳定,馏分馏出速度也很稳定,但温度计的读数会有小幅度的上升,上升到134℃保持稳定。20多分钟后,由于蒸馏烧瓶中液体含量较少,所以停止了实验。
实验结果:
第一种馏分的温度范围为74~78℃,馏出体积为42mL。
第二组馏分的温度范围为132~134℃。
现象分析:
蒸馏第一种馏分时,后期温度计的读数会降低是因为随着时间的延长,蒸馏瓶中第一种馏分的含量在降低,蒸汽量减少。第一种馏分的温度范围接近查资料所得的无水乙醇的沸点78.3℃,所以第一种馏分是无水乙醇。馏出体积大于加入乙醇的体积,是因为蒸馏时,乙醇蒸汽带出了少量的二甲苯。温度持续降低是因为烧瓶中没有蒸汽。当温度再次上升到接近70℃时,出现了馏分,是因为蒸馏烧瓶中温度很高,但无水乙醇并没有蒸馏完全,所以当二甲苯变成蒸汽上升时,带有少量的无水乙醇,所以此时馏出了少量的无水乙醇。
实验结论:
二甲苯和无水乙醇没有共沸点。
第二篇:实验一 蒸馏工业乙醇
实验二、乙醇的蒸馏
一、实验目的
1.掌握常压蒸馏的操作方法。
2.了解通过蒸馏分离液体混合物的原理。
3.掌握通过乙醇密度查找相对应浓度的方法。
二、实验原理
液体化合物的沸点,是它的重要物理常数之一。在使用、分离和纯化过程中,具有很重要的意义。
液体化合物的蒸气压随温度升高而增加,当液体的蒸气压力增加到与大气压力相等时,液体即开始沸腾,液体在101.33 KPa(1 atm)的沸腾温度即为该化合物的沸点。液体化合物的沸点随外界压力而改变,外界压力增大,沸点升高;外界压力减小,沸点降低。沸点随外压而变化有如下经验规律:在101.33 KPa(1 atm)附近,当压力每下降1.33 KPa(10 mmHg)时,多数液体的沸点约下降0.5 ℃。在较低压力时,压力每降低一半,沸点下降约10 ℃。
在一定压力下,纯净化合物的沸点是固定的,而且沸程很短,一般为l℃左右。但具有恒定沸点的液体不一定是纯粹的化合物,如两个或两个以上的化合物形成的共沸混合物也具有一定的沸点。不纯液体有机物的沸点,取决于杂质的物理性质。如杂质是不挥发的,则不纯液体的沸点比纯液体的高,若杂质是挥发性的,则蒸馏时液体的沸点会逐渐上升(恒沸混合物例外),故沸点的测定也可用来鉴定有机物或判断其纯度。
由于物质的沸点随外界大气压的改变而变化,因此,讨论或报道一个化合物的沸点时,一定要注明测定沸点时外界的大气压,以便与其文献值相比较。
沸点的测定分为常量法和微量法。常量法装置及操作与一般蒸馏相同。
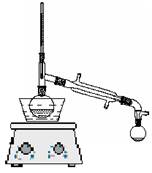
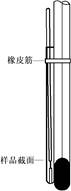
图3.2 常压蒸馏装置 图3.3 微量法测定沸点装置
微量法测定沸点可用图3.3所示装置。取一支长约8 cm、直径为4~5 mm薄壁玻璃管制成沸点管,在其中加入待测液体有机化合物样品4~5滴,再在管中插入一支上端密封开口向下的毛细管(要全部没入待测液体中)。用橡皮筋将此沸点测定管固定在温度计的一侧,使待测液面与温度计水银球上限平齐。然后将温度计连同测定管一起置于带有搅拌的盛有热浴液的小烧杯中,在小烧杯加热时由于气体膨胀,毛细管口会有小气泡慢慢逸出,当接近沸点时气泡增加,到达液体沸点时有一连串气泡快速逸出,此时停止加热,温度逐渐下降,气泡逸出的速度也逐渐减慢,当等到毛细管末端不再有气泡逸出,待测液体刚要进入毛细管的瞬间(最后一个气泡有开始缩回毛细管内的倾向时),说明毛细管内蒸气压与外界压力相同。记下温度计的温度,即为该化合物的沸点。当温度下降5~10℃时,重新换一支毛细管,缓慢加热,进行平行测定。
每支毛细管只可用于一次测定,一个样品测定需要重复2~3次,测得平行数据差应不超过1℃。
三、实验仪器及试剂
仪器:100 mL单口圆底烧瓶; 蒸馏头; 温度计;100mL单口圆底烧瓶或锥形瓶×1;50mL单口圆底烧瓶或锥形瓶×1;直形冷凝管;接液管;可控温电热包;控温电磁搅拌器 比重计;
试剂:70-75% 工业乙醇
四、实验操作
按图3.2安装仪器:组装仪器一般按照由下至上、由左向右的顺序进行安装;铁架台前端要留出足够的空间以便实验仪器的组装;用于固定铁夹的S型夹(俗称S夹),在安装时一般要将开口留在上边或右边,用于固定铁夹的旋钮在右边,方便操作;铁夹的开口要有胶衬(若无,应更换,或手工缠上细棉绳或胶布)以增大对仪器的摩擦力。依次安装仪器架、可控温电热包、100 mL单口圆底烧瓶、蒸馏头、直形冷凝管(注意磨口旋紧,以防漏气)、接液管和50 mL圆底烧瓶或锥形瓶;直形冷凝管远离蒸馏头的口为入水口,应保持与桌面垂直,另一端为出水口。在直形冷凝管入水口接胶管(称为进水管),另一端与水龙头相连;出水口接胶管(称为出水管),另一端放在水槽中。冷凝管入水口和出水口连接胶管时,玻璃管口上涂水润滑,小心安装胶管并旋转套到出水口和进水口上(可先在水池上方安装好胶管,擦净水滴后安装到蒸馏装置上,注意不要将水滴溅到电热套里)。
缓缓通入冷凝水后(从节约用水和安全考虑,出水管口有细小水流流出即可),经老师检查蒸馏装置合格后,量取50 mL 75 %工业乙醇,用长颈漏斗漏斗通过蒸馏头向100 mL圆底烧瓶中将乙醇小心加入(让漏斗下端伸入到蒸馏头支管的下方,以防液体未经蒸馏而流出),加完乙醇后加2-3粒沸石。装好温度计。开动电磁搅拌用可控温电热包加热,在100 V加热至70 ℃时,调节电热包的电流,此时蒸汽前沿逐渐上升,待蒸汽达到温度计时,温度计读数急剧上升,再继续调节电热包的电流约在95 V,使水银球上的液滴和蒸汽达到平衡,收集前馏分(如果没有前馏分就取前4滴馏分作为前馏分),量取前馏分体积,记录下来。当温度计上升至77 ℃时,将原来的接收瓶(50 mL)换成已称重的干燥的50 mL圆底烧瓶为接收器接收主馏分,保持2滴/s的速度,蒸馏至81.5℃,收集4℃馏程的馏分。
当瓶内剩下约5 mL液体以下时,若维持原来的加热速度,温度计读数经常会突然下降,此时即可停止蒸馏(不要将瓶内液体蒸干,养成至少留下1~2 mL的习惯,以防有时会出现危险)。关闭加热装置,取下主馏分接收瓶,按增重法称量主馏分的重量及其体积,分别记录下来。撤去加热套,待蒸馏瓶冷却到室温,取下蒸馏瓶,量取残液体积,记录下来。
利用分别量取的体积前馏分、主馏分和残液体积,计算液体回收率。
采用比重计测量馏出液的密度,并查手册进行换算,找出乙醇溶液的相应浓度,计算蒸馏收率。
五、实验记录
1.收集的馏分的起始和终点温度,主馏分溜出速度;
2.收集的各馏分的重量或体积。
六、注意事项
1.一定要加沸石;
2、仪器气体部分要严密;
3、馏出速度不宜太快;
4、不要蒸干,留下2~5 mL;
5、注意电热套使用安全,防止烫伤,防止药品掉入及H2O、液体滴入;
6、注意玻璃仪器安装和使用安全,防止割伤和挫伤。
七、思考与讨论
1.什么叫沸点?液体的沸点和大气压有什么关系?
2.蒸馏时蒸馏瓶内所装液体应为蒸馏瓶容积的多少为宜?
3.蒸馏时为什么要加入沸石?如果蒸馏前忘记加沸石,应怎么办?
4.蒸馏时为什么要控制馏出液的速度?
表3.3 乙醇水溶液的密度(20℃)
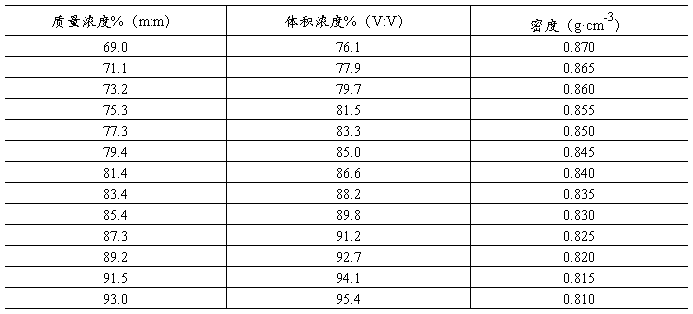
(续表)