 免疫学实验设计
免疫学实验设计

题目:StreamlineDireetHST分离卵黄抗体
班级:20##级临床医学本科(12)班
姓名:
StreamlineDireetHST分离卵黄抗体
班级:20##级临床医学本科(12)班
作者及学号:
一、实验背景
1、卵黄抗体即卵黄免疫球蛋白(Egg Yolk Immunoglobulin,lgY),目前研究较多的是鸡卵黄抗体。母鸡接受免疫后,在卵黄成熟期,血液中的免疫球蛋白IgG选择性的转移到卵黄中形成IgY。IgY是一种7S免疫球蛋白,分子量180kD,由两条重链(分子量22~30kD)组成,等电点接近5.2。IgY的结构虽与IgG相似,但其Fc段氨基酸组成与IgG相差很大,不结合类风湿因子,不与蛋白A、G以及哺乳动物Fc受体和补体结合。在免疫检测中,可代替哺乳动物来源的抗体,提高监测的特异性及敏感性。已经证明特异性IgY对人及动物的许多疾病具有一定的预防和治疗作用,与其他用于被动治疗的免疫球蛋白相比,IgY具有价廉易得、稳定性好、可口服等优点,在疾病的免疫检测和防治方面具有良好的前景。
IgY具有以下优点:
(1) 由于鸡与哺乳动物的种系关系较远,可产生针对哺乳动物保守蛋白的抗体(在哺乳动物体内难以产生),用于免疫学测定“同时IgY不与类风湿因子(RF)及哺乳动物补体结合,减少了免疫检测的干扰,提高准确性”。
(2) 经特定抗原免疫后,母鸡产生对抗原的持久性应答,可不断获得特异性的多克隆抗体,其均来源于同一个体,抗体均一性好。
(3)卵黄中的IgY含量明显高于鸡血清中lgG的含量,约为巧一25mg/mL卵黄在相同的免疫时间内,由一只鸡所生鸡蛋中提取的抗体量是由一只兔的血清制备的120倍。
(4) IgY还可抵抗幼龄动物的胃酸屏障作用,并可抗肠道中胰蛋白酶和胰凝乳蛋白酶的消化。
鸡蛋提供了廉价易得的IgY来源,从一枚鸡蛋中可获得100~250 mg IgY。如何将大量的卵黄抗体提取出来,是决定IgY能否被广泛应用的一个重要前提。鸡卵黄中含水48%、蛋白质17.8%、脂肪30.5%,其中几乎所有的脂肪都与蛋白质结合形成脂蛋白,IgY是水溶性的蛋白。从卵黄中获得卵黄抗体的过程包括IgY分离、提取和纯化高含量的脂肪及脂蛋白。
2、StreamlineDireetHST是一种新型吸附剂,主要为阳离子离子交换吸附,同时伴有疏水作用,可以用来处理高粘度的料液。
已有实验成功实现了StreamlineDireetHST对模型蛋白的静态吸附。以牛血清白蛋白(BSA)和牛血红蛋白为模型蛋白,考察了pH和盐浓度对streamlineDireetHsT吸附蛋白质的影响。结果表明,streamlineDireetHsT对蛋白质的吸附随pH的变化而变化,存在最适pH使得吸附容量最大,蛋白质分子体积的变化在一定程度上会影响吸附容量。当蛋白质与吸附剂存在静电吸引作用时,吸附过程由静电相互作用主导,吸附等温线符合Langmuir吸附方程;当存在静电排斥作用时,吸附等温线则呈现典型的多分子层吸附模式。
StreamlineDirectHST吸附剂的吸附容量大,可以在很高的料液流速下高效吸附蛋白质。料液的盐浓度对于吸附没有大的影响,对于高粘度料液不需稀释可以直接进样,所以料液可以省去很多处理步骤,节约成本,可以采用提高离子强度或是改变pH来洗脱蛋白质。
既然IgY是一种蛋白质,因此,可以设计一个StreamlineDireetHST分离卵黄抗体IgY。
二、实验原理
阳离子交换型混合模式吸附剂streamlineDirectHST对蛋白质的吸附受pH和盐浓度的共同影响。streamlineDirectHsT对蛋白质的吸附随pH的变化而变化,存在最适pH使得吸附容量最大,蛋白质分子体积的变化在一定程度上会影响吸附容量。当蛋白质与吸附剂存在静电吸引作用时,吸附等温线符合Langmuir吸附方程;当存在静电排斥作用时,吸附等温线则呈现典型的多分子层吸附模式。
卵黄抗体在pH4一9之间性质较稳定,所以本实验采用pH4一9的缓冲液进行层析分离。
三、实验目的
1、了解streamlineDirectHST分离蛋白的原理。
2、探索streamlineDirectHST对卵黄抗体分离的可行性。
四、材料与方法
1、 试剂与仪器
试剂:StreamlineDireetHST吸附剂,磷酸氢钠和磷酸二氢钠。
仪器:AKTA explorer 100层析系统,Ultrospec 3300 pro 分光光度计,台式PH/ISH测试仪。
2、 方法
(1) 卵黄水溶性组分(WSF)的提取
采用水稀释法除去卵黄中的大部分脂类。具体方法如下:取购自农贸市场的新鲜鸡蛋一只,打一小孔将蛋清倒出,将孔扩大并用蒸馏水冲洗卵黄1一2次。将卵黄倒至滤纸上吸干水分,刺破卵黄膜,使卵黄流出。将收集到的卵黄用蒸馏水稀释六倍,并用0.1M的HCI溶液调节pH至5.2,放入4摄氏度冰箱静置过夜。将卵黄溶液800Orpm离心30分钟,上清液中含有卵黄水溶性组分(包括卵黄抗体),沉淀弃去。
(2) StreamlineDireetHST分离IgY
取预处理好的卵黄稀释液的上清液,用0.2um滤膜过滤,作为进样样品,每次进样量为2ml。层析柱(内径1cm)中填充5ml Streamline Direct HST。使用AKTA explorer 100蛋白质分离纯化系统进行层析分离实验,改变平衡液与洗脱液的pH和盐浓度进行层析分离,收集各流出组分,并作lgy电泳分析。
(3) SDS一聚丙烯酞胺凝胶电泳分离
配制30%凝胶贮液、分离胶缓冲液、浓缩胶缓冲液、10%SDS、1%TEMED、10%AP、电极缓冲液与2x非还原态染色液。
制板:采用8%的分离胶和3%的浓缩胶。取待电泳的样品,与等体积的2x非还原态染色液混合。上样前沸水浴中3一5分钟。层析料液样品上样量为5ul,穿透液与洗脱液样品上样量为15ul。
五、实验预期结果与讨论
1、实验结果
StreamlineDireetHST成功分离了卵黄抗体
2、讨论
streamlineDireetHsT是阳离子交换型混合模式吸附剂,而卵黄抗体在pH5.0左右呈中性,净电荷为零。理论上分析,选择上样平衡液pH应该小于7.0,使IgY带正电荷,而与吸附剂产生静电吸附作用。根据此技术在蛋白质分离中的经验,在pH<4时,streamlineDirectHsT的梭基基团将渐渐趋于不解离,对蛋白质的吸附容量会减少,同时考虑到IgY在pH<3时活性将急剧降低因此选择上样平衡液的pH在4.0一6.0之间。
洗脱时改变缓冲液的pH使蛋白质带负电荷与吸附剂产生静电排斥作用。IgY等电点接近7,因此使用中性或碱性缓冲液使卵黄抗体带负电荷,与streamhneDirectHsT发生静电排斥,洗脱蛋白。IgY在pH>ll时活性开始下降,因此为保持较高的蛋白质活性,实验中洗脱液均使用pH7一10的缓冲液。
六、参考文献
1、《混合模式层析及其用于抗体分离纯化的研究》浙江大学 何瑜芳
2、《卵黄抗体对肠道感染小鼠粘膜的调节作用》大连理工大学 宗颖
3、《家禽卵黄抗体作用机理及应用现状分析》 燕海峰;邓源;朱立军;肖兵南
4、《单个B细胞抗体制备及应用》 生物工程学报 迟向阳;于长明;陈薇
第二篇:20xx级临本9班免疫试验设计
补体结合试验
一 实验目的
掌握用免疫溶血机制做指示系统,来检测另一反应系统抗原或抗体的试验的原理及操作。
二 实验原理
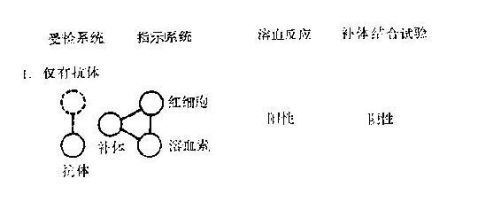
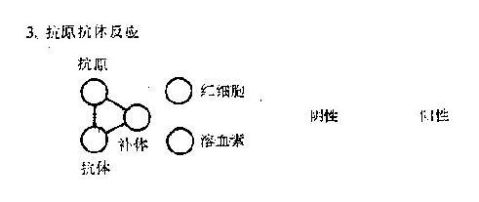
该试验中有5种成分参与反应,分属于3个系统:①反应系统,即已知的抗原(或抗体)与待测的抗体(或抗原);②补体系统;③指示系统,即绵羊红细胞与相应溶血素,试验时常将其预先结合在一起,形成致敏红细胞。反应系统与指示系统争夺补体系统,先加入反应系统给其以优先结合补体的机会。
如果反应系统中存在待测的抗体(或抗原),则抗原抗体发生反应后可结合补体;再加入指示系统时,由于反应液中已没有游离的补体而不出现溶血,是为补体结合试验阳性。如果反应系统中不存在的待检的抗体(或抗原),则在液体中仍有游离的补体存在,当加入指示系统时会出现溶血,是为补体结合试验阴性(图1)。因此补体结合试验可用已知抗原来检测相应抗体,或用已知抗体来检测相应抗原。
三 实验材料
待测血清(破坏补体和除去一些非特异因素)、抗原、抗体、溶血素、羊红细胞、补体、试管、微量加样枪。
四 试验方法
1.设定阳性对照组、阴性对照组和待测组。
2.向三组试管中先分别依次加入0.2ml补体、0.1ml抗原。
3.添加0.1ml抗体于阳性对照管,加0.1ml血清于待测组。
4.分别向三组试管添加0.1ml溶血素,0.2ml羊红细胞。
5.混匀,置37℃30min后观察结果。
五 预期结果
阳性对照管不发生溶血,阴性对照管发生溶血。若待测组发生溶血,则不含与相应抗原对应的抗体;若不发生溶血,则含与相应抗原对应的抗体。
六 讨论
补体的生物学意义。
设计者:李媛媛5110001386 李兆玮5110001387 李茜 5110001384 李婷婷5110001385 李磊 5110001413 贾伟 5110001411
