综合性实验报告
胡萝卜肉质根愈伤组织诱导
及继代增殖培养
一、实验原理及目的
(一)实验目的
1、通过MS培养基母液的配制和保存,掌握配制于保存培养基母液的基本技能。
2、通过MS固体培养基的配制,掌握培养基的制备基本技能。
3、学会和掌握诱导愈伤组织的基本技术。
4、初步掌握组织培养的无菌操作技术。
5、初步掌握外植体的消毒技术。
6、掌握组培室常用的化学试剂。
7、学会和掌握愈伤组织继代培养的基本操作技术。
(二)实验原理
1、配制培养基时,为了使用方便和用量准确,通常采用母液法进行配制,即将所选培养基配方中各试剂的用量,扩大若干倍后再准确称量,分别先配制成一系列母液置于冰箱中保存,使用时按比例吸取母液进行稀释配制即可。
2、在自然情况下,根主要为植物吸收和固定的重要器官,同时,有些植物的根亦具有繁殖的功能。植物根生长快、代谢能力强、变异小,使得其在研究根的营养吸收、生长和代谢的变化规律、器官分化、形态建成规律等方面具有重大的理论与实践意义。
依据细胞全能性原理,即指任何具有完整细胞核的细胞(动物、植物等),都拥有形成一个完整个体所必需的全部遗传信息(DNA)。就胡萝卜根来说,其肉质根细胞同样具有形成完整再生植株的能力。这种由单个根衍生而来并经继代培养而保存的,在遗传上具有一致的根的培养物,称为离体根无性系。利用这些离体根的无性系可以进行器官再生体系、苗木无性系快速繁殖和其他方面的实验研究。
3、愈伤组织(callus)原指植物体的局部受到创伤刺激后,在伤口表面新生的组织。它由活的薄壁细胞组成,可起源于植物体任何器官内各种组织的活细胞。在植物体的创伤部分,愈伤组织可帮助伤口愈合;在嫁接中,可促使砧木于接穗愈合,并由新生的维管组织使砧木与接穗沟通。在植物器官、组织、细胞离体培养时,条件适宜也可以长出愈伤组织。其发生过程是:外植体的活细胞经诱导,恢复其潜在的全能性,转变为分生细胞,继而其衍生的细胞分化为薄壁细胞组织而形成愈伤组织。
愈伤组织诱导的成败关键主要不是外植体的来源种类,而是培养条件,其中激素的种类和浓度最为重要。诱导愈伤组织常用的生长素是2,4-D,IAA和NAA,常用的细胞分裂素是KT和6-BA。
愈伤组织形成的过程分为3个时期:诱导期、分裂期和分化期(形成期),愈伤组织的生长是发生在不与琼脂培养基接触的表面。
4、调节培养基的酸碱性至PH=5.8左右。由于培养基的PH值直接影响到培养物对离子的吸收,因而过酸或过碱都会对植物材料的生长有很大的影响。此外,PH还影响到琼脂培养基的凝固情况。所以,当培养基配制好后应立即进行PH的调整。培养基若偏酸时用氢氧化钠(1mol/L)来调节,若过碱就用盐酸(1mol/L)来调节。当PH值高于6.0时,培养基将会变硬;当PH值低于5.0时,琼脂不能很好地凝固。
5、植物组织培养的优点:
①研究材料来源单一,无性系遗传背景一致;
②经济、方便、效率高;
③条件可控、误差小;
④生长快、周期短、重复性强;
⑤可全年试验或生长。
6、继代培养是指愈伤组织在培养基上生长一段时间后,营养枯竭,水分散失,并已经积累了一些代谢产物,此时需要将这些组织转移到新的培养基上,这种转移称为继代培养。实际上就是对来自于外植体所增殖的培养物(包括细胞、组织或其切段)通过更换新鲜培养基及不断切割或分立,进行连续多代的培养。
将诱导产生的芽、苗、愈伤组织、原球茎或胚状体等培养物重新分割,接种到新鲜培养基上进一步扩大培养的过程称为继代培养,也称为增殖培养。该过程是植物组织培养中决定繁殖速度快慢、繁殖系数高低的关键阶段。继代使用的培养基对于一种植物来说,每次几乎完全相同。由于培养物在适宜的环境条件、充足的营养供应和生长调节剂作用下,排除了其他生物的竞争,繁殖速度大大加快。
二、实验所需仪器设备及其原理
(一)冰箱
用于长期贮存培养基母液、生化试剂及低温处理材料。
(二)培养箱
用于少量植物材料的培养。有条件的话,还可采用全自动的调温、调湿人工气候箱来进行植物组织培养和试管苗快繁。
(三)超净工作台
超净工作台是为植物组织培养提供无菌操作环境,是最常用、最普及的无菌操作装置,和无菌室相比,超净工作台既方便又舒适,无菌效果又好。
超净工作台一般由鼓风机、过滤器、操作台、紫外灯和照明灯等部分组成。它是将空气过滤后形成无菌的风,创造出一个无菌环境。根据风幕形成的方式,超净工作台可分为水平式和垂直式两种。在一般的植物组织培养中,两种都可以采用,而进行植物的遗传转化操作和农杆菌、大肠杆菌的接种时,最好采用垂直风幕式的超净工作台,这样可以避免细菌在空气中的扩散。
(四)高压蒸汽灭菌锅
高压蒸汽灭菌锅主要用于培养基、蒸馏水和各种器械的灭菌消毒。高压灭菌锅有大型、中型和小型三种。实验室最常用的是中型立式全自动灭菌锅和小型便携式美景,大型卧底式高压灭菌锅在大型工厂化植物组织培养上使用。
(五)天平
较常用的为普通天平(1/100g、1/10g),在微量元素、植物激素等的称量时,需要用分析天平(1/10000g)。
(六)蒸馏水制备装置
有蒸馏型和离子交换型两种。需要时,还可以进行重蒸馏来获得纯度更高的蒸馏水。
三、培养基及其机制
(一)培养基
是供微生物、植物和动物组织生长和维持用的人工培植的养料,一般含有碳水化合物、含氮物质、无机盐(包括微量元素)以及维生素和水等。
(二)植物组织培养所用培养基——MS培养基
MS培养基是Murashige和Skoog于1962年为烟草细胞设计的,其特点是:无机盐和离子浓度高,是较稳定的离子平衡溶液,它的硝酸盐含量高,其养分的数量和比例合适,能满足植物细胞的营养和生理需要,因而使用范围较广,多数植物组织培养快速繁殖用它作为培养基的基本培养基。
MS培养基是目前使用最普遍的培养基。其具有较高的无机盐浓度,能够保证组织生长所需的矿质营养,还能加速愈伤组织的生长,由于配方中的离子浓度较高,在配制、贮存和消毒等过程中,即使有些 成分略有出入,也不会打破离子间的平衡。MS固体培养基可用于诱导愈伤组织,也可用于胚、茎段、茎尖及花药的培养,其液体培养基用于细胞悬浮培养时能获得明显的成功。MS培养基的无机养分的数量和比例比较合适,足以满足植物细胞在营养上和生理上的需要。因此,一般情况下,不再用添加氨基酸、酪蛋白水解物、酵母提取物及椰子汁等有机附加成分。和其它培养基基本成分相比,MS培养基中的系哦啊酸盐、钾和铵的含量高,这是它的显著特点。
1.配制MS母液培养基
(1)所需仪器
电子天平、烧杯、容量瓶、细口瓶、药勺、玻璃棒、电炉、量筒、称量纸、PH试纸、冰箱
(2)所需药品
NH4NO3、KNO3、CaCl2·2H2O、MgSO4·7H2O、KH2PO4、H3BO3、MnSO4·4H2O、ZnSO4·7H2O、Na2MoO4·2H2O、KI、CuSO4·5H2O、CoCl2·6H2O、FeSO4·7H2O、Na2-EDTA·2H2O、肌醇、烟酸、盐酸吡哆醇(维生素B6)、盐酸硫胺素(维生素B1)、甘氨酸、蒸馏水.
①大量元素的配制(CaCl2·2H2O要在最后单独加入)
用量=放大倍数×体积×培养基中的浓度 n=20 v=1L
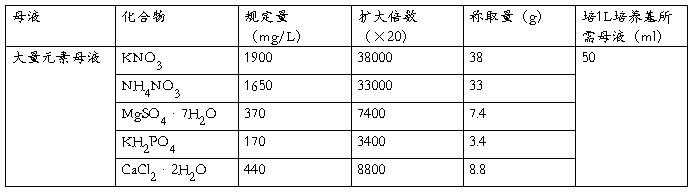
依次称取,分别溶解,依次混合,定容,倒入母液瓶中,贴标签,放入4℃冰箱。
②微量元素的配制(Fe单独配制)
n=200 v=1L MnSO4·4H2O:22.3g或MnSO4·H2O:16.9g
③铁盐母液配制
n=200 配500ml
螯合态的铁,混合煮沸,PH=5.8~6.2(用NaOH溶液调其PH)
④有机物的配制(单一母液)
肌醇(10mg/ml 配250ml) V B1(1mg/ml 配250ml)
V B6(1mg/ml 配250ml) 烟酸(1mg/ml 配250ml)
甘氨酸(2mg/ml 配250ml)
⑤生长调节物配制
6-BA(1mg/ml 配100ml)
2,4-D(1mg/ml 配100ml)
NAA(1mg/ml 配100ml)
注:6-BA先用少量1mol/L HCl溶解,2,4-D和NAA先用少量mol/LnaOH或95﹪酒精溶解。
2.配制胡萝卜愈伤组织诱导培养基(MS固体培养基)
(1)配方:
MS基本培养基+2mg/L NAA+0.1 mg/L6-BA+200 mg/L水解酪蛋白+3﹪蔗糖+0.7﹪琼脂粉
即:大量元素:50ml 微量元素:5 ml 有机物成分:5 ml 铁盐:5 ml
2mg/L NAA:2mg(ml) 0.1mg/L 6-BA:0.1mg(ml) 200mg/L水解酪蛋白:200mg
蔗糖:30g 琼脂:7g
注:由于配制减半,因此上述试剂均减半。
(2)要求:每小组配制500ml,分装为20瓶,每瓶25ml。
(3)步骤:
①琼脂溶解(3.5g+350ml蒸馏水,加热煮沸2min以上);
②把蔗糖加入琼脂溶液中(15g蔗糖);
③把CH加入琼脂和蔗糖溶液中;
④依次量取MS培养基母液及所需生长调剂物质母液于烧杯中,最后加入到相应的容器中;
⑤PH调整为6.0~6.2,并定容到500ml;
⑥培养基分装、封口;
⑦灭菌(121℃ 1.1kg/cm2 ,15min);
⑧保存。
3.继代培养基的配制
MS基本培养基+6-BA+ NAA+2,4-D+C+CH
蔗糖15g;琼脂3g;大量元素2.5ml;微量元素2.5ml;铁盐0.5ml;肌醇5ml;V B1 0.5ml;
V B6 0.25ml;烟酸0.25ml;甘氨酸0.5ml;CH 0.1g。
制500ml,分为22瓶,PH为5.8。
四、外植体消毒及无菌操作技术
(一)外植体消毒
在离体根培养中,首先芽解决外植体消毒问题,因为在自然条件下,根生长在土壤中,要进行彻底灭菌、消毒。为了消灭这种污染源,在把植物组织接种到培养基上之前必须要进行彻底的表面消毒;内部已受到真菌或细菌侵染的组织在组织培养研究中一般都淘汰不用。
胡萝卜的肉质根,其硬度较大,容易操作,可直接用灭菌剂进行处理。
①用自来水将胡萝卜冲洗干净,用解剖刀将其切成几个小段;
②用70﹪~75﹪的酒精浸泡胡萝卜2min;
③放入0.1﹪HgCl2中浸泡10min;
④用无菌水洗4次;
⑤备用:为胡萝卜愈伤组织的诱导作准备。
(二)无菌操作技术
无菌操作技术室用于防止微生物进入实验室区内的操作技术。
要求:①在进行无菌操作前将界面上的细菌和病毒等微生物杀灭;
②操作过程中是界面与外界隔离,避免微生物的侵入。
目前,多数实验室都使用各种类型的超净工作台进行无菌操作。
步骤:
①在实验之前30min将超净工作台的紫外灯打开,进行灭菌。工作人员要避免紫外灯的照射,做实验时将紫外灯关闭。
②用酒精喷壶或酒精棉将超净工作台进行消毒(酒精浓度为70﹪)。
③实验操作前,工作人员的手和小臂用70﹪的酒精消毒。
④使用的镊子、解剖刀等用90﹪的酒精浸泡,之后放在酒精灯上火烧灭菌,再放在灭菌支架上冷却后使用。
⑤在植入或移植材料的前后,培养瓶的瓶口需在酒精灯上火烧灭菌。
(三)实验操作的注意事项
1.进行胡萝卜愈伤组织诱导,首先要在无菌的滤纸上将已消毒的外植体的表面轻轻切去;
2.移入培养基时,打开封口,封口纸要小心摆正,不能乱丢乱放;
3.镊子用手拿住上端,不能去拿下端;
4.整个操作过程要尽量在超净工作台的无菌范围内进行;
5.禁止操作时正面大声讲话。
五、实验结果及讨论
(一)实验结果
1.胡萝卜肉质根愈伤组织诱导结果:

2.胡萝卜愈伤组织继代增殖培养结果
这次试验总的接种瓶数为2瓶,无污染瓶;但是愈伤组织没有进行进一步的生长,增殖不是很好,呈现暗色。
(二)对试验结果的分析
1.胡萝卜肉质根愈伤组织的诱导
(1)其中一瓶接种瓶受污染,可能是由于在使用解剖刀切胡萝卜时,拿镊子的部位靠下后导致污染了细菌;也可能操作时没有在超净工作台的无菌范围内;也可能由于材料本身内部已经收到了污染,或是在切离胡萝卜表面时,没有彻底将材料表面切干净,导致接种后受污染;也有可能所使用的工具消毒不够彻底,或是操作不规范,如接种掀开培养瓶封口膜时手指碰到了封口膜里面,或是封口膜没有绑紧,导致了微生物的进入。
(2)已接种好的材料,愈伤组织发生不好的或是没有发生的。可能是由于:
①在配制培养基时,缺乏某种物质或没有将培养基混合均匀;
②在分装培养基时,没有进行均匀倾倒;
③所使用材料没有将其表面切除,因其结构被HgCl2破坏而无法使组织材料愈伤组织化。
2.愈伤组织的继代增殖培养
(1)培养瓶没有被污染,但是愈伤组织仅在培养基上发育了一段时间后就终止其生长,其原因有:
①培养基的配制有问题,可能培养基配制时某类激素用量较少或无;
②接种时,切其愈伤组织时把本体胡萝卜切了进去。
(三)实验讨论
1.调节培养基PH时,理论上应调至5.8为宜,但因其培养基经高温高压灭菌后,蔗糖会分解,PH值会有所下降,因此PH值调至6.0可减小误差。
2.植物组织培养实验中,必须的前提是:无菌操作,胡萝卜肉质根(外植体)经HgCl2 和酒精消毒后,即认为是消毒干净,在此后的操作中,要注意对其用具彻底消毒,操作过程中动作要规范实施。
3.废液进行回收处理,酒精、HgCl2浸泡完材料后,应统一倒入指定容器。
4.切胡萝卜时,下方要垫上无菌滤纸。
5.接种时,动作要轻,力度要适中,不要把接种的材料切块压入到培养基里面,以致破坏培养基;切块大小要适中,不宜太大,也不宜太小。
6.MS培养基的特点:
①无机盐浓度高;
②高含量的氮、钾,尤其是硝酸盐;
③有一定数量的铵盐,营养丰富;
④不需要添加更多的有机附加物。
7.植物组织培养所需的环境条件:
与自然条件一样,组织培养中的材料的生长要受到温度、光照、湿度等各种物理条件,不同气体、培养基的组成、PH值和渗透压等各种化学条件,以及外植体部位、大小、细胞密度等各种生物条件等环境条件的影响。实验中要注意考虑这些条件的影响,并采取适当的措施控制好培养条件。
8.植物组织培养所需的营养成分:
植物体内至少含有几十种化学元素,其中大部分元素在植物体的内部起到了一定的生理作用:
①组成各种化合物,参与集体的建设,成为结构物质;
②构成一些特殊的生理活性物质,参与活跃的新陈代谢;
③元素之间相互协调,以维持离子浓度平衡、胶体稳定、电荷平衡等电化学方面的作用;
④发育方面:特定的元素影响植物的形态发生和组织、器官建成。
(四)实验总结
本次试验有成功之处,也有不足的地方。成功是我经过此次试验,学到了很多关于植物组织培养的实际操作的知识内容,并且这些东西,只有自己亲身尝试,才能体会明白。
植物组织培养实验,最重要的就是在无菌条件下对无菌的材料进行处理,因此,无菌操作技术是实验失败与否的关键;进行实验前期,我们要做好充分的准备,培养基的配制、材料的选用、植物组织培养理论知识,及操作的方法与步骤要进行预先准备,如果有一步骤出差错,尤其是培养基配制,即使后面的过程做得再好,结果也等于“0”。
实验的细节要把握好,才能取得实验的成功。此次试验,让我深深体会到了严谨的科学态度的重要性。
实验失败是由于操作不当、培养基配制出错等原因造成的,我们在实验时必须按照步骤严格进行,否则再怎么努力,也是白做。
此次试验以小组为单位,我们分工合作,各自负责好自己分好的部分工作,合作也是实验要求的基本内容,有了合作,才有了我们的成果,不管好与否,至少我们努力过。
第二篇:组培实验报告:胡萝卜愈伤组织诱导培养

本科学生综合性实验报告
学号 姓名
学院 专业、班级
实验课程名称 植物组织培养实验
教师及职称
开课学期 20## 至 2014 学年 第二 学期
填报时间 20## 年 06 月 20 日
云南师范大学教务处编印
一、实验设计方案
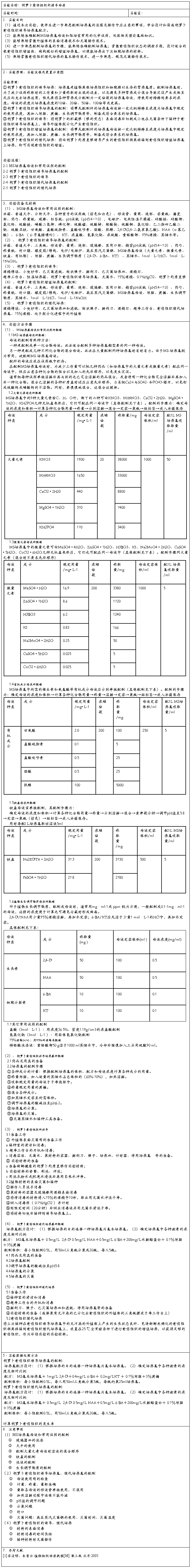
二、实验报告

