风险管理报告
1 验证报告起草

2 验证组成员:
3 验证报告批准:
批准人: 日期:
目 录
第一章 综述............................................................................................................... 2
第二章 风险管理评审的输入....................................................................................... 5
第三章 风险管理评审................................................................................................. 5
第四章 风险管理评审结论.......................................................................................... 6
附录1.............................................................................................................................. 7
附录2............................................................................................................................. 11
附录3............................................................................................................................ 13
第一章 综述
1.产品简介
1)产品概况:
2)预期用途:
3)适用环境:
4)产品的负载的要求:
5)产品使用方法:
请参考使用说明书
2.风险管理计划及实施情况简述
于20##年开始策划立项的同时,我们针对该产品进行风险管理活动的策划,制定了风险管
理计划。
该风险管理计划确定了的风险可接受准测,对初步阶段的风险管理活动,风险管理活动有关
人的职责和权限以及生产和和产后信息的获得方法的评审要求进行了安排。
公司组成了风险管理小组,确定了该项目的风险管理负责人,确保该项目的风险管理活动按
照风险管理计划有效的执行。
3.此次风险管理评审目的
本报告是对XX产品在设计开发输入阶段的风险管理情况进行总体评价,并对所有的可能危害及每一
个危害产生的原因进行判定,对于每种危害可能产生损害的严重度和危害的发生概率进行了评估。在某一风险水平不可接受时,采取了降低风险的控制措施,同时,对采取风险控制措施后的剩余风险进行了可接受性评价,证实对产品的风险已进行了管理,并且控制在可接受范围内。
4、风险管理人员及其职责分工
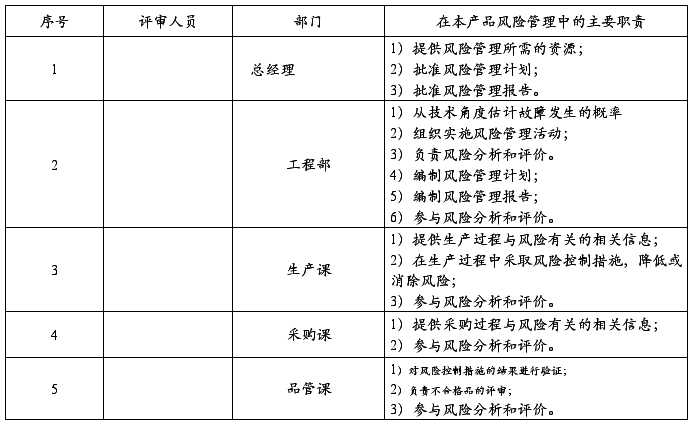
第二章 风险管理评审的输入
1. 产品的相关法律法规要求:
2.风险管理计划(包含风险可接受准则)文件编号:(详见附录1)
3.风险管理文档
(1)《安全性特征问题清单》 文件编号: (详见附录2)
(2)《初始危害判断及初始风险控制方案分析》 文件编号: (详见附录3)
4、相关文件和记录
《风险分析控制程序》 文件编号: 版本号:A
产品设计开发文档 (主要包括设计图纸、工艺等 )
第三章 风险管理评审
1、风险管理计划完成情况
评审小组对风险管理计划的合理性进行了检查,通过对相关风险管理文档的检查,认为自粘电极胶系列风险管理计划能够有效控制产品最终风险。
2、风险可接受评审
针对产品系列在设计方案每一个危害的判断,在充分收集资料数据,采取降低风险措施后,产品接受的程度,采取风险控制措施后,没有新的风险产生,经评审小组确认:产品设计阶段剩余风险控制方案可接受。具体评价方面:
1)单个风险控制是否有相互矛盾的要求?
结论:尚未发现现有控制措施有相互矛盾的情况。
2)总结论:风险管理评审小组在分析以上方面,一致评价,本产品的设计输入风险可接受。
3、评审通过的风险管理文档
本次评审后确定的风险管理文档:
1)《风险分析控制程序》 文件编号: (详见附件)
2)《风险管理计划》 文件编号: (详见附录1)
3)《安全性特征问题清单》 文件编号: (详见附录2)
4)《初始危害判断及初始风险控制方案分析》 文件编号:(详见附录3)
5)《风险评价风险控制措施及剩余风险评价记录表》文件编号:(详见附录4)
第四章 风险管理评审结论
1、风险管理评审小组经过对试生产的产品的评审,以及以检查风险管理文档的方式对风险管理过程的评审,认为:
- 风险管理计划已被适当地实施;
- 综合剩余风险是可接受的;
- 已有适当方法获得相关生产和生产后信息;
-全部剩余风险处于风险可接受准则的可接受范围内,且受益超过风险。
同意批准。
小组签名:
批准:
1.计划范围:
本计划适用于本公司范围内医疗器械类产品的设计和开发过程、产品实现过程、产品销售服务过程以及产品报废处置过程的风险管理活动。
2.职责和权限的分配:(职责和权限的分配)
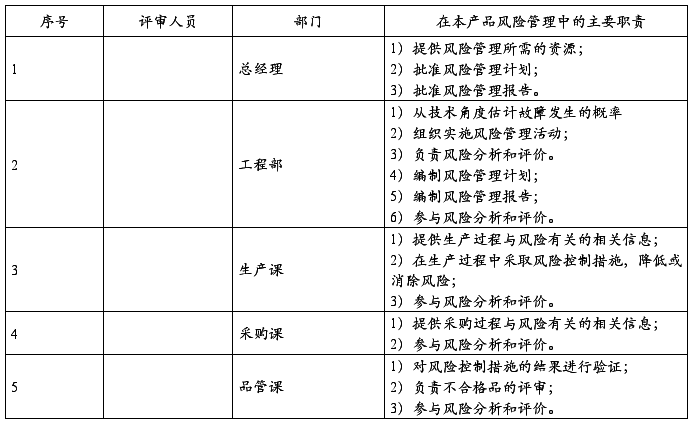
3.风险管理活动评审的要求:
(1)在设计和开发阶段看风险管理是否覆盖所有安全要素;
(2)规定一个风险可接受准则的方针并形成文件;
(3)定期或不定期评审风险管理过程,以确保风险管理过程的持续适宜性和有效性。
4.风险可接受性准则

5.风险管理活动计划
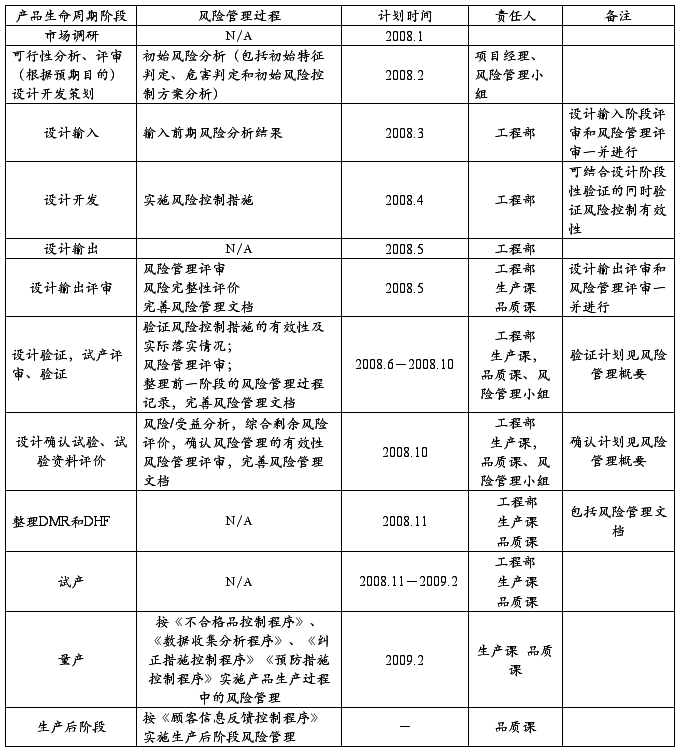
6. 风险管理过程:
风险管理过程包括:
第1步:产品用途和定量定性特征的描述
第2步:已知或可预见危害的判定
每项损害严重度的估计
每项损害潜在原因的判定
每项原因发生概率的估计
第3步:风险估计(采取控制措施前)
第4步:风险评估
第5、6步:采取风险控制措施
第7步:剩余风险评估
第8步:风险/收益分析及准则
第9步:产生的其他危害
第10步:风险评价的完整性
第11步:全部剩余风险的评价
第12步:风险管理结果
7. 风险管理审核要求:
严格按照风险管理计划进行各阶段的审核,确保计划得到有效地执行,保证各个步骤的正确运行,并且得到相应的结果以及记录归档。
附录2 《安全性特征问题清单》
公司以ISO 14971-2007医疗器械 - 医疗器械的风险管理中的应用为基础,同时依标准YY/T0316:2008附录C的资料对医疗器械预期用途和与安全有关的特征进行了判定,通过对涉及医疗器械的生产、预期使用者、预期用途、合理可预见的误用和最终处置等提出了一系列问题的方法,逐步了解该产品的安全性特征,为进一步的风险分析打下基础。
表1
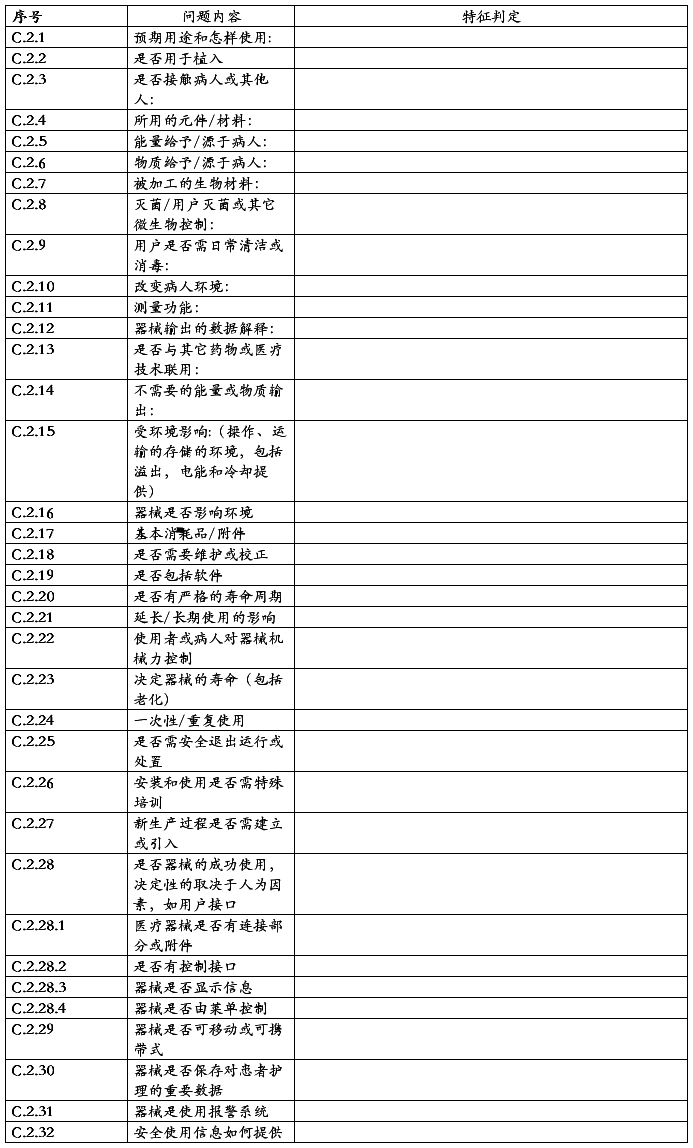
附录3
风险控制方案分析
1. 风险评价、风险控制措施及剩余风险评价记录表:
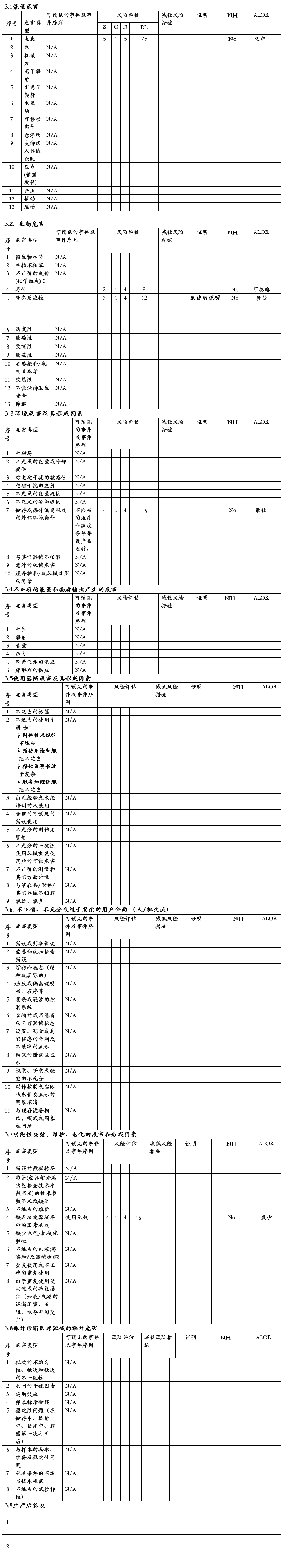
第二篇:公司风险管理报告
司风险管理报告
2、职责与权限的分配
2 1总经理为风险管理提供适当的资源,对风险管理工作负领导责任。保证给风险管理、实施和评定工作分配的人员是经过培训合格的,保证风险管理工作执行者具有相适应的知识和经验。
2 2技术部负责产品设计和开发过程中的风险管理活动,形成风险分析、风险评价、风险控制、综合剩余风险分析评价的有关记录,并编制风险管理报告。 2 3质量部、、销售部、生产部等相关部门负责从产品实现的角度分析所有已知的和可预见的危害以及生产和生产后信息的收集并及时反馈给技术部进行风险评价,必要时进行新一轮风险管理活动。
2 4技术部和评审组成员定期对风险管理活动的结果进行评审,并对其正确性和有效性负责。
2 5办公室负责对所有风险管理文档的整理工作。
3、风险分析
附录E 1的资料对所有已知和可预见的危害事件序列进行分类,组织各部门进行风险评价和风险控制措施的分析与实施并编制成相应的表格。
3 1参加风险分析的部门包括生产部、质量部、技术部、、销售部等,技术部主要分析设计开发阶段已知和可预见的危害事件序列,生产部主要分析产品生产阶段的已知和可预见的危害事件序列,和销售部主要分析产品生产后已知和可预见的危害事件序列,技术部负责收集各部门分析的结果并按照16号令的要求和YY/T0316:2008附录E 1的资料对所有已知和可预见的危害事件序列进行分类,组织各部门进行风险评价和风险控制措施的分析与实施并编制成相应的表格。
3 2风险分析内容包括:
3 3在产品设计开发初始阶段由于对产品设计细节了解较少,采用PHA(初步危害分析)技术对产品进行
3 4在设计开发成熟阶段采用失效模式和效应分析(FMEA)及失效模式、效应和危害分析(FMECA)对产品进行危害、危害处境及可能导致的损害进行分析。 3 5在试生产或生产阶段采用危害分析和关键控制点(HACCP)进行风险管理的优化。
3 6质量部、生产部负责配合技术部对产品所有已知和可预见的危害进行分析,预期1个月,保存好相关记录。
4、风险评价
4 1生产部、质量部、、销售部负责配合技术部对经风险分析判断出的危害进行发生概率与损害严重度的分析,最后根据本计划确定的风险可接受准则判断风险的可接受性,预期2个月,保存好评价记录。
4 2以下是为本次风险管理确定的风险可接受准则,其中损害的严重度采用定性分析,损害发生的概率采用半定量分析,风险可接受性准则以4Ⅹ6三分区矩阵图表示。
4 2 1损害的严重度水平
4 2 2损害发生的概率等级
4 2 3风险评价准则
4 3在经过风险分析和风险评价过程判断出的产品所有的风险均应采取合理可行的措施降至可接受区,当风险被判断为不可接受时,应应收集相关资料和文
献对风险进行风险/受益分析,如果受益大于风险,则该风险还是可接受的,如果风险大于受益则设计应放弃。
4 4对损害概率不能加以估计的危害处境,应编写一个危害的可能后果清单以用于风险评价和风险控制,各部门应配合技术部采取合理可行降低法将风险降低到合理可行的最低水平,对于无法降低的风险进行风险/受益分析,如果受益大于风险,则该危害可接受,如果风险大于受益,则风险不可接受。 4 6受益必须大于风险才能判断为可接受。
5、风险控制
5 1对于经判断为可接受的风险还应当采取可行的措施将风险降到最低。 5 2对于经判断为不可接受的风险,各部门应配合技术部在设计开发阶段从以下几个方面进行风险控制方案分析,识别一个或多个风险控制措施,以把风险降低到可接受水平。
附文件中给出警告、使用说明;
5 3在产品试生产或生产阶段,对产品制造过程进行控制,如运用HACCP技术。(危害分析和关键控制点)
5 4如果经方案分析确定所需的风险降低是不可行的,则各部门应收集相关资料对剩余风险进行风险/受益分析,若经评审所收集的资料和文献不支持受益大于风险,则设计应放弃。
5 5各部门应确保经判定的危害处境产生的一个或多个风险得到了考虑,保证风险控制的完整性。
第4条的风险可接受准则进行评价,对判断为不可接受的应采取进一步的风险控制措施,如果控制措施不可行,则应收集和评审相关的资料和文献对剩余风险进行风险/受益分析,若受益大于风险,则剩余风险依然是可接收到,如果风险大于受益,则为不可接受。对于判断为可接受的剩余风险,、销售部应配合技术部决定那些剩余风险应予以公开,依据YY/T0316:2008附件J的指南公开哪些剩余风险。同时对控制措施的实施是否会引起的一个或多个新的风险或对采取措施之前评价的风险是否有影响进行分析,必要时进行再次风险分析、风险评价和风险控制,所采取活动的结果应进行记录并保持,此过程预期30个月。
5 6在风险控制方案实施中或实施后,应对实施效果进行验证,以确定控制措施的适应性和有效性,对任何剩余风险都应采取本计划中第4条的风险可接受准则进行评价,对判断为不可接受的应采取进一步的风险控制措施,如果控制措施不可行,则应收集和评审相关的资料和文献对剩余风险进行风险/受益分析,若受益大于风险,则剩余风险依然是可接收到,如果风险大于受益,则为不可接受。对于判断为可接受的剩余风险,、销售部应配合技术部决定那些剩余风险应予以公开,依据YY/T0316:2008附件J的指南公开哪些剩余风险。同时对控制措施的实施是否会引起的一个或多个新的风险或对采取措施之前评价的风险是否有影响进行分析,必要时进行再次风险分析、风险评价和风险控制,所采取活动的结果应进行记录并保持,此过程预期30个月。
6、风险管理活动的验证要求
6 1风险管理计划是否已适当实施的验证
6 2风险管理活动效果的验证
7、风险管理活动评审的要求
7 1评审组成员及其职责如下:
7 2评审组成员应对评审结果的正确性和有效性负责。
7 3各部门应配合评审组成员利用《质量信息反馈控制程序》及《忠告性通知和事故报告程序》对与产品安全性有关的信息进行评审,为综合剩余风险的评价提供依据。
7 4依据以下和安全性有关的信息在产品的设计开发、试制及产品生产与售后阶段进行评审:
7 5应对产品生产和生产后信息的获取方式进行评审
8、综合剩余风险分析
第4条的准则判断是可接受的,如果判断为不可接受,则各部门应收集和评审有关资料和文献,以便决定预期用途的医疗受益是否超过综合剩余风险,如果上述证据支持医疗受益超过综合剩余风险的结论,则综合剩余风险是可接受的,否则综合剩余风险任然是不可接受的。
8 1在所有风险控制措施已经实施并验证后,各部门应考虑是否所有由该产品造成的综合剩余风险依据本计划中第4条的准则判断是可接受的,如果判断为不可接受,则各部门应收集和评审有关资料和文献,以便决定预期用途的医疗受益是否超过综合剩余风险,如果上述证据支持医疗受益超过综合剩余风险的结论,则综合剩余风险是可接受的,否则综合剩余风险任然是不可接受的。 8 2各部门可以参考一下的一些方法评价综合剩余风险
附录J予以公布,应保持综合剩余风险的评价结果记录,此过程预期3个月。 8 3各部门应决定哪些综合剩余风险应依据YY/T0316
9、风险管理报告
第7条,评审的结果最终以风险管理报告的方式给出,此项评审活动预期1个月。
1、产品描述
概 述
3、风险分析人员
附录E 1的资料对所有已知和可预见的危害事件序列进行分类,组织个部门进行风险评价和风险控制措施的分析与实施并编制成相应的表格。
4、医疗器械预期用途和与安全性有关特征的判断
附录C的资料,根据各自有关的专业和经验对预期用途和与安全性有关的特征进行了判断,同时对已知和可预见的危害进行了分析,记录如下表: 2 1 医疗器械的预期用途是什么和怎样使用医疗器械?
2 2 医疗器械是否预期植入?
2 3 医疗器械是否预期和患者或其他人员接触?
2 4 在医疗器械中利用何种材料或组分,或与医疗器械共同使用或与其接触? 2 5 是否有能量给予患者或从患者身上获取?
2 6 是否有物质提供给患者或从患者身上提取?
2 7 医疗器械是否处理生物材料用于随后的再次使用、输液/血或移植? 2 8 医疗器械是否以无菌形式提供或预期由使用者灭菌,或用其他微生物学控制灭菌?
2 9 医疗器械是否预期由用户进行常规清洁和消毒?
2 10 医疗器械是否预期改善患者的环境?
2 11 医疗器械是否预期和其它医疗器械、医药或其它医疗技术联合使用? 2 12 是否有不希望的能量或物质输出?
2 13 医疗器械是否对环境影响敏感?
2 14 医疗器械是否影响环境?
附件?
2 15 医疗器械是否有基本的消耗品或附件?
2 16 医疗器械是否有储存寿命期限?
2 17 是否有延时和长期使用效应?
2 18 医疗器械承受何种机械力?
2 19 什么决定医疗器械的寿命?
2 2 20 医疗器械是否预期一次性使用?
2 21 医疗器械是否需要安全的推出运行或处置?
2 22 医疗器械的安装和使用是否要求专门的培训或专门的技能?
2 23 如何提供安全使用信息?
2 24 是否需要建立或引入新的制造过程?
2 25 医疗器械的成功使用,是否关键取决于人为因素,例如用户界面? 2 25 1 用户界面设计特性是否可能促成使用错误?
2 25 2 医疗器械是否在因分散注意力而导致使用错误的环境中使用? 2 25 3 医疗器械是否有连接部分或附件?
2 25 4 医疗器械是否有控制接口?
2 25 5 医疗器械是否显示信息?
2 25 6 医疗器械是否由菜单控制?
2 25 7 医疗器械是否由具有特殊需要的人使用?
2 26 医疗器械可能以什么方式被故意地误用?
2 27 医疗器械是否预期为移动式或便携式?
2 28 医疗器械的使用是否依赖于基本性能?
2 29 医疗器械是否通过第三方权威部门检测?
2 30 医疗器械是否有明确的标识或信息显示在何种状态下禁止使用?
5、危害的判定
附录E 1危害示例进行了分类,同时对可能发生的损害和初步控制措施进行了分析,记录如下表:
序文件要求控制
1、洁净区尘埃粒子超标、温度、湿度不符合要求等
2、仓库环境不符合要求等
1、没有注意说明书上注意事项及图示而使产品不能预期使用(正常状态)
2、某些部件缩水程度不同、组装不到位或者漏检
3、产品基本性能如滑动性、密合性、针尖锋利度等不符合标准要求 3 1损害发生概率的分析
附录D 3 2对上一步分析得到的每一项危害处境引起的损害发生概率进行估计,然后依据风险管理计划第4条4 2 2的损害发生概率等级的准则,对估计的每一项损害概率划分等级,具体记录如下表:
1、洁净区尘埃粒子超标、温度、湿度不符合要求等。
2、仓库环境不符合要求等。
1、没有注意说明书上注意事项及图示而使产品不能预期使用。(正常状态)
2、某些部件缩水程度不同、组装不到位或者漏检。
3、产品基本性能如滑动性、密合性、针尖锋利度等不符合标准要求。
3 2 损害发生严重度的分析
附录D和风险管理计划中规定的损害严重度准则对每一项危害处境可能引起的损害严重度进行等级划分,具体记录如下表:
3 3 风险可接受性判断
3 1风险控制方案分析
1、洁净区尘埃粒子超标、温度、湿度不符合要求等
2、仓库环境不符合要求等
1、没有注意说明书上注意事项及图示而使产品不能预期使用(正常状态)
2、某些部件缩水程度不同、组装不到位或者漏检
3、产品基本性能如滑动性、密合性、针尖锋利度等不符合标准要求
3 3.设计开发过程中,运用FMEA、FMECA,对于与产品安全性相关的失效模式,按风险管理流程,进行风险分析、风险评价和风险控制,
9 8 按照采购控制程序对供方进行严格评审并按程序要求控制原材料的采购 9 8 按照设计的参数进行验证并最后确认,作为关键控制点进行控制
1、刻度不准确无法正确用药
2、标识不清晰无法正确操作
1、零位线偏低或偏高
2、印刷网版上有异物或产品上有硅油
3、机台运行不正常
9 8 制定相应的工序检验规程并按要求检验,印刷设备按要求进行验证确认并按照维护保养计划定期维护保养
1、密封圈安装不合格
2、自动回缩装置安装不到位、漏检
9 8 在组装设备自检程序里输入设计的安装质量要求,并对设备进行安装、运行、性能验证,并有质量部对产品进行抽查
8 8 按照设计的参数进行验证,最后确定上下限并形成工艺流程图,严格按要求操作
序文件要求和工艺流程图,并对相关计算机软件进行验证
9 8 按照设计的参数范围和临界条件进行灭菌验证,并制定相应的程序文件要求和工艺流程图,并对相关计算机软件进行验证
3 4风险控制措施实施效果的验证
3、综合剩余风险评价
