化工专业实验报告
实验名称: 固定床乙醇脱水反应实验研究
实验人员: 同组人:
实验地点:天大化工技术实验中心630室
实验时间: 年 月 日
班级/学号: 级 班
学号: 实验组号:
指导教师:
实验成绩:
乙醇脱水反应研究实验
一、实验目的
1. 掌握乙醇脱水实验的反应过程和反应机理、特点,了解针对不同目的产物的反应条件对正、副反应的影响规律和生成的过程;
2. 学习气固相管式催化反应器的构造、原理和使用方法,学习反应器正常操作和安装,掌握催化剂评价的一般方法和获得适宜工艺条件的研究步骤和方法;
3. 学习动态控制仪表的使用,如何设定温度和加热电流大小,怎样控制床层温度分布;
4. 学习气体在线分析的方法和定性、定量分析,学习如何手动进样分析液体成分。了解气相色谱的原理和构造,掌握色谱的正常使用和分析条件选择;
5. 学习微量泵和蠕动泵的原理和使用方法,学会使用湿式流量计测量流体流量。
二、实验仪器和药品
乙醇脱水气固反应器,气相色谱及计算机数据采集和处理系统,精密微量液体泵,蠕动泵。ZSM-5型分子筛乙醇脱水催化剂,分析纯乙醇,蒸馏水。
三、实验原理
乙醇脱水生成乙烯和乙醚,是一个吸热、分子数增多的可逆反应。提高反应温度、降低反应压力,都能提高反应转化率。乙醇脱水可生成乙烯和乙醚,但高温有利于乙烯的生在,较低温度时主要生成乙醚,有人解释这大概是因为反应过程中生成的碳正离子比较活泼,尤其在高温,它的存在寿命更短,来不及与乙醇相遇时已经失去质子变成乙烯.而在较低温度时,碳正离子存在时间长些,与乙醇分子相遇的机率增多,生成乙醚。有人认为在生成产物的决定步骤中,生成乙烯要断裂C—H 键,需要的活化能较高,所以要在高温才有和于乙烯的生成。
乙醇在催化剂存在下受热发生脱水反应,既可分子内脱水生成乙烯,也可分子间脱水生成乙醚。现有的研究报道认为,乙醇分子内脱水可看成单分子的消去反应,分子间脱水一般认为是双分子的亲核取代反应,这也是两种相互竞争的反应过程,具体反应式如下:
C2H5OH → C2H4 + H2O (1)
C2H5OH → C2H5OC2H5 +H2O (2)
目前,在工业生产方面,乙醚绝大多数是由乙醇在浓硫酸液相作用下直接脱水制得。但生产设备会受到严重腐蚀,而且排出的废酸会造成严重的环境污染。因此,研究开发可以取代硫酸的新型催化体系已成为当代化工生产中普遍关注的问题。目前,在这方面的探索性研究已逐渐引起人们的注意,大多致力于固体酸催化剂的开发,主要集中在分子筛上,特别是ZSM-5分子筛。
本实验采用ZSM-5分子筛为催化剂,在固定床反应器中进行乙醇脱水反应研究,反应产物随着反应温度的不同,可以生成乙烯和乙醚。温度越高,越容易生成乙烯,温度越低越容易生成乙醚。实验中,通过改变反应温度和反应的进料速度,可以得到不同反应条件下的实验数据,通过对气体和液体产物的分析,可以得到反应的最佳工艺条件和动力学方程。
反应机理如下:
主反应:C2H5OH → C2H4 + H2O
副反应:C2H5OH → C2H5OC2H5 +H2O
在实验中,由于两个反应生成的产物乙醚和水留在了液体冷凝剂中,而气体产物乙烯是挥发气体,进入尾气湿式流量计计量总体积后排出。
对于不同的反应温度,通过计算不同的转化率和反应速率,可以得到不同反应温度下的反应速率常数,并得到温度的关联式。
四、实验流程图
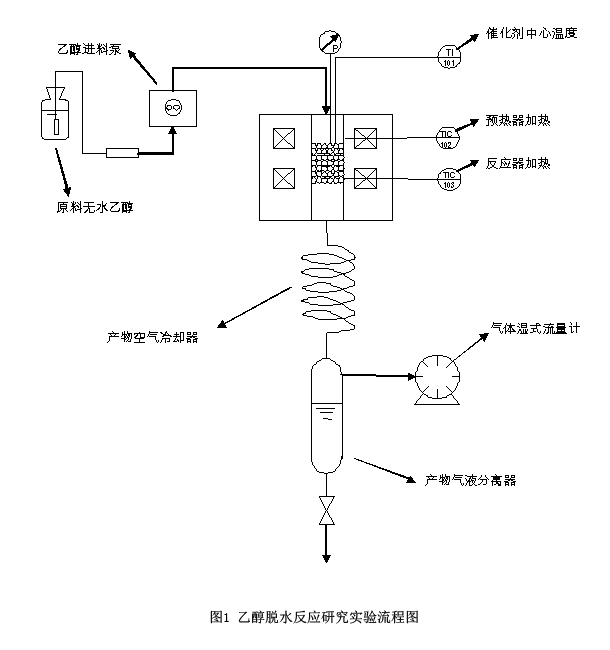
五、实验步骤
1. 按照实验要求,将反应器加热温度设定为270℃。在温度达到设定值后,继续稳定10分钟;
2. 设置乙醇的加料速度为0.4ml/min,开始加入乙醇;
3. 反应进行15分钟后,正式开始实验。打开气液分离器旋塞,放出液体倒入回收瓶,记录湿式流量计读数,而后关闭旋塞。每隔10min记录反应温度、预热温度和炉内温度等实验条件;
4. 每个加料速度下反应30分钟。反应终止后,打开旋塞,用洗净的三角锥瓶接收液体产物,并用天平对液体产物准确称重(注意接收液体产物前应先称出锥形瓶的重量),并且记下此刻湿式流量计的读数;
5. 改变加料速率,每次提高0.4ml/min,重复上述实验步骤。
六、实验数据记录与处理
表1 实验过程记录
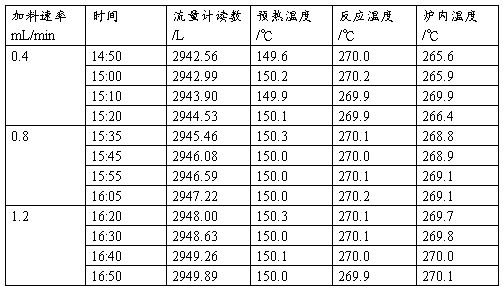
表2 色谱分析条件
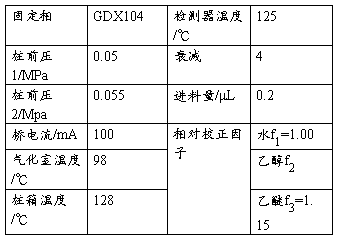
表3 标准液色谱分析结果
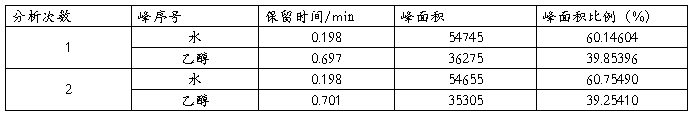
备注:配置样品用水17.57g,乙醇15.18g.
表4 液相产品色谱分析结果

备注:0.4时得产品(63.09-57.57)g ,0.8时得产品(65.20-49.19)g ,1.2时得产品(79.64-53.02)g .
表5 进料流量变化与转化率、收率、选择性关系表

计算过程举例:
1.计算乙醇相对校正因子:
f2= 
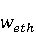 =
=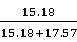 =0.4635
=0.4635
f2,1= 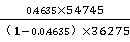 = 1.304
= 1.304
f2,2 =1.337
则得f2=1.320
2.色谱定量数据处理:
以进料量为0.4mL/min时乙醇为例,其质量百分含量为
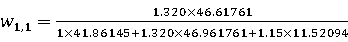 =0.5275
=0.5275
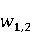 =0.5307
=0.5307
则有 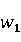 =0.5291
=0.5291
3.转化率、选择性和收率计算:
以进料量为0.4 mL/min时的数据为例,已知
表6. 20℃各物质物性参数

进料质量流率为
Q=0.789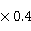 =0.316g/min
=0.316g/min
30min内进料的物质的量为
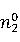 =0.316
=0.316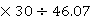 =0.20577mol
=0.20577mol
湿式流量计测得产品的体积为
V=2944.53-2942.56=1.97L
假设实验条件是标况,则乙烯的物质的量为
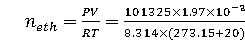 =0.081900mol
=0.081900mol
由色谱定量结果可得乙醇物质的量
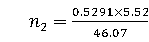 =0.06340mol
=0.06340mol
乙醚的物质的量
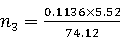 =0.00846
=0.00846
乙醇的转化率
X=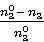 =0.69189
=0.69189
乙烯的收率
Yeth =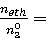 0.39802
0.39802
乙烯的选择性
S= =0.57526
=0.57526
同理得乙醚收率0.04111,选择性0.05942.
七、实验结果分析
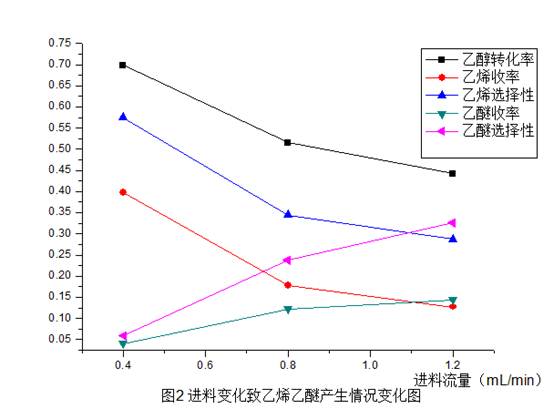
随进料量增加,乙醇转化率和乙烯收率、选择性下降;乙醚收率及选择性上升。
说明反应存在单分子和双分子过程的竞争。在进料流率较低的情况下,乙醇分压较低,容易发生单分子反应,此时以主反应即乙醇脱水反应为主。随着进料流量的增加,反应器内乙醇分压上升,此时乙醇分子间反应加剧,导致乙烯收率和选择性下降,乙醚含量和选择性上升。
由于催化剂催化能力的限制,催化剂不能完全催化进料的转化,导致随进料量增加,乙醇转化率不断降低。
八、问答题
1. 改变哪些实验条件,可以提高乙醇的反应转化率?
乙醇反应转化率的提高和空速、反应温度、进料乙醇浓度等因素有关。空速直接关系到反应停留时间长短。反应停留时间越长,反应越彻底,乙醇的转化率也就越高。反应温度关系到反应常数,反应温度越高,反应常数越大,因而反应速率提高,转化率也就跟着提升。而进料乙醇的浓度越高,从气体反应的碰撞理论上来看,反应器内分子碰撞次数也随之提高,因而反应速率提高,转化率提高。
2. 怎样使反应的平衡向有利于产物乙烯生产的方向发展?
可以降低乙醇的进料速率,并通过增加反应器长度增加空时。
乙醇脱水制乙烯是放热反应,分子数不变,提高反应温度,降低反应压力均能提高反应转化率。
3. 结合本实验的结果,叙述怎样确定最适宜的分析条件?
多次不同条件下进行试验,分析载气流速变化、进样量大小及柱温高低对色谱峰和峰面积的影响,选择合适的色谱分析条件。
4. 怎样对液体产物进行定性分析?
可以利用相对保留值ris对液体产物进行定性分析。选择水作为基准物,液体产物各组分的相对保留值可以通过下式求出:

将实验测得的待测组分对标准物质的相对保留值与文献记载的相对保留值进行对照,即可定性。
根据气相色谱峰面积比值和所得相对校正因子,利用下面公式即可以得到液体产物的组成。

5. 怎样对整个反应过程进行物料恒算?应该注意哪些问题?
根据反应方程式,利用求出的乙烯和乙醚的质量可以算出反应所需的乙醇的总量,利用下面表达式对乙醇进行物料恒算:
液体产物中乙醇质量 + 生成反应物消耗的乙醇质量 - 乙醇进量
若上式等于零,则表明物料守恒。
要进行物料衡算应该注意下述条件:
1) 保证反应过程应达到稳态。这可以根据设备仪表的读数是否稳定在目标温度确定;
2) 确保色谱读数可靠。实验中,通过完成两次色谱测定,只有当两次色谱结果各值差距不超过2时,才能确保色谱操作可信。
3) 确保每次称量液体产品前,都要对三角锥瓶进行称重,不能以第一次结果进行测量。因为每次实验都要对容器进行彻底地清洗,凡士林不能保证每次涂抹量一样。
4) 最好保证实验的时间控制精确到秒。这是因为乙醇进量是根据流量乘以时间求出,相差几十秒对实验衡算结果影响也是不小的。
6. 实验中,那些简化的处理方法可能造成实验误差?应怎样进一步改进?
将进入湿式气体流量计的气体全部视为乙烯,此简化计算造成实验误差,尤其
在乙烯本身收率已经很高时,造成的误差很大。应测量气液分离器内的温度与压力,通过气体分压方程和安托尼方程计算乙烯、乙醇蒸气,乙醚蒸气、水蒸气各自含量,分配对应体积。
第二篇:对乙醇脱水制乙烯实验的新研究
对乙醇脱水制乙烯实验的新研究
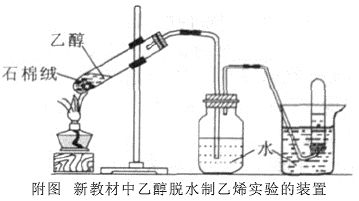
中学化学实验室中常用浓硫酸作为乙醇脱水制取乙烯的催化剂、脱水剂,但是实验中存在很多的弊端,如:炭化现象严重影响观察,反应所需要的时间长,制取的乙烯纯度不高等。苏教版全国高中化学新教材———《有机化学基础》(选修)P69页,关于乙醇脱水制取乙烯的实验中,没有采用传统的方法即以浓硫酸作为催化剂,而是选用石棉绒作为催化剂制取乙烯[1]。教材中采用试管作为反应仪器,将乙醇和石棉绒加入其中用酒精灯进行加热,并用水进行洗气来制取乙烯(见下图)。
石棉绒能否作为制取乙烯的催化剂,还需要从其反应机理来看。
乙醇脱水反应是按照E1机理进行的,具体过程如下:
在酸的作用下,乙醇分子上不容易离去的基团——C—O转变成易离去的基团,C—O键断裂脱水形成C,C的邻位碳原子上失去一个质子,一对电子转移过来中和正电荷形成双键。从反应机理上看,生成C的一步是整个反应的速控步骤,还表明醇的脱水反应是一个可逆反应。因此可以通过控制H的浓度即用较浓的酸来使反应向右进行,可以选用浓硫酸或五氧化二磷作为催化剂和脱水剂。另外,醇在350-400℃在氧化铝或者硅酸盐表面上脱水,也可形成双键[2]。如: ++++
石棉属于硅酸盐类矿物,化学成份是Mg6[Si4O10][OH]8,含有氧化镁、铝、钾、铁、
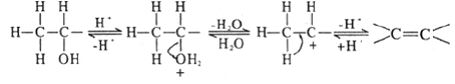
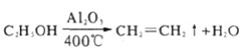
硅等成分[3]。因此从理论上看石棉绒可以作为乙醇脱水制取乙烯的催化剂,那么它在
实际操作中能否有良好的催化效果?与浓硫酸、五氧化二磷在实验室中的催化效果有什么不同?笔者对此进行了一系列的对比实验。
1实验内容
1.1催化剂的选择
采用浓硫酸作催化剂;
采用石棉绒作为催化剂,分别采用角闪石石棉和蛇纹石石棉;
采用五氧化二磷作催化剂;
采用浓硫酸和石棉绒作为混合催化剂;
采用五氧化二磷和石棉绒作为混合催化剂。
1.2实验装置
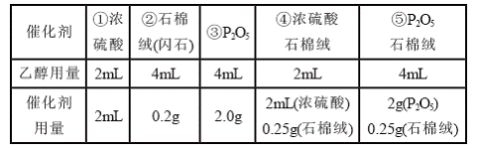
1.3实验中乙醇的具体用量及催化剂用量
乙醇的用量和催化剂用量表
1.4说明
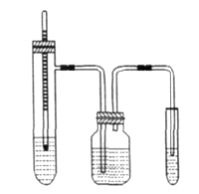
实验采用具支试管作为反应容器。为了使实验结果具有明显的对比性,实验中检验乙烯的酸性高锰酸钾采用相同的配制:在试管中加入3滴0.01mol/L的高锰酸钾稀释至5mL,再加入3滴1﹕1的盐酸,混合均匀。由于实验中浓硫酸、五氧化二磷及产生的杂质都具有酸性,因此选用KOH溶液洗气,消除杂质对检验乙烯的影响。另外,由于热的乙醇也能够使高锰酸钾褪色,为了保证实验中蒸发出的乙醇对实验结果没有影响,加做了一个空白实验,即不加入任何的催化剂采用和上述装置相同的装置进行加热,将乙醇蒸发经过盛有KOH溶液的洗气瓶,通入酸性高锰酸钾溶液中,发现高锰酸钾未褪色。
说明在实验中乙醇没有对结果造成影响。另外自然界中的石棉有两种,角闪石石棉和蛇纹石石棉,上述实验中的是角闪石石棉。为了准确,笔者将蛇纹石石棉也作为催化剂进行了部分对照实验。
2实验现象
2.1浓硫酸作为催化剂
加热到40s左右时温度迅速上升到170℃,即有大量的气泡冒出,酸性高锰酸钾溶液褪色,褪色情况较好。在反应开始后不久即开始出现炭化现象,到反应结束时溶液的炭化现象非常严重,几乎变成浓黑色。且反应完毕后试管中酸性残留气体非常多,试管难以洗涤。
2.2石棉绒(角闪石)作催化剂
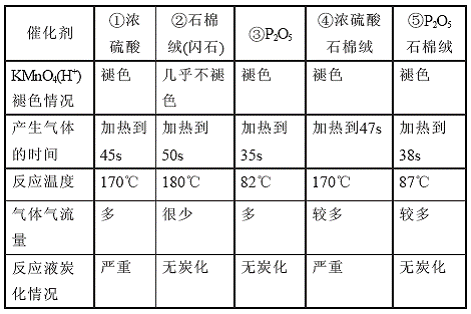
加热开始时温度升高,有少许气泡冒出,当温度上升到78℃时乙醇开始大量地蒸发,加热到50s左右时有很少量的气泡冒出,温度开始上升,但是酸性高锰酸钾几乎不褪色,褪色情况明显不如前者好,且当温度过高时,石棉绒会变焦。笔者试做的几次蛇纹石石棉的反应现象还不如角闪石石棉。
2.3五氧化二磷作催化剂
将五氧化二磷加入到盛有乙醇的试管中即有大量的白雾产生,加热后温度开始迅速上升,有少许气泡冒出,当加热到82℃时即有大量的气泡冒出,反应进行到35s时酸性高锰酸钾褪色,褪色情况相对最好。
2.4浓硫酸和石棉绒共同作为催化剂
反应现象同1中相似,但是局部炭化现象比较严重,且石棉绒会阻止部分乙烯气体的逸出,因此酸性高锰酸钾的褪色时间及褪色情况不如1。
2.5五氧化二磷和石棉绒共同作催化剂
反应现象同3,加热到87℃左右时会有大量的气体产生,石棉绒也会阻止乙烯气体的逸出,因此高锰酸钾的褪色情况及时间不如3。
3结果分析
3.1石棉绒作催化剂
石棉绒作为乙醇脱水制乙烯的催化剂在以前的中学教材及文献中并没有提及,虽然醇在硅酸盐表面上能够发生脱水反应并且不发生重排,但是所需要的温度非常高,在演示实验中乙醇往往在脱水之前就已经完全地蒸发掉,只有极少的一部分会脱水生成乙烯。笔者在进行实验时发现:该反应产生的气体的量很少,只能使高锰酸钾稍微褪色,且现象不明显,反应的重现性很差,即石棉绒对乙醇脱水制取乙烯的催化效果不佳。另外,由于石棉绒属于致癌物质,对人体的危害较大,所以很多中学实验室中并不配备石棉绒,而且石棉的种类比较多,成份不同,其催化作用也不尽相同,因此,笔者认为,乙醇脱水制乙烯实验的催化剂选用石棉绒并无什么优势,另外,在浓硫酸和五氧化二磷作催化剂时分别加入石棉绒对他们的催化效果也没有明显的促进作用,反而会使气体逸出的时间加长。
3.2浓硫酸作催化剂
浓硫酸作为一种传统的催化剂,在教材中被使用得最多,但是也存在较多的问题,主要在于反应时间长,炭化现象严重,副产物较多,试管难于清洗。对于浓硫酸作为催化剂在很多文献中都进行了大量的研究,笔者认为可以通过改变乙醇和浓硫酸的体积比消除此反应的弊端:教材上所给出的乙醇和浓硫酸的体积比为1∶3,在这个比例下乙醇易被浓硫酸炭化,副产物也较多,因此可以适当减少浓硫酸的用量,笔者用1∶1体积比进行实验,可明显减轻炭化现象。
3.3五氧化二磷作催化剂
五氧化二磷作为催化剂,其催化效果在一些文献中曾被提及。笔者在实验中也发现:采用五氧化二磷作为催化剂无炭化现象,不影响学生对实验的观察,反应时间短,所需温度不是很高,在80℃左右即可,高锰酸钾褪色情况良好。但是五氧化二磷属于强吸水剂,在具体操作中会产生白雾,存在着不便,这也是其在使用中存在的弊端。
经多次反复的对照实验验证:在乙醇脱水制取乙烯的实验中,五氧化二磷的催化效果最为理想,而石棉绒对该反应的催化效果并不理想。
参考文献:
[1]王祖浩.有机化学基础[M].南京:江苏教育出版社,2004:69.
[2]邢其毅.基础有机化学(上册)(第三版)[M].北京:高等教育出版社,2005:275.
[3]王箴.化工辞典(第四版)[M].北京:化学工业出版社,2000:837.
