ISO13485-2003内部质量体系审核计划
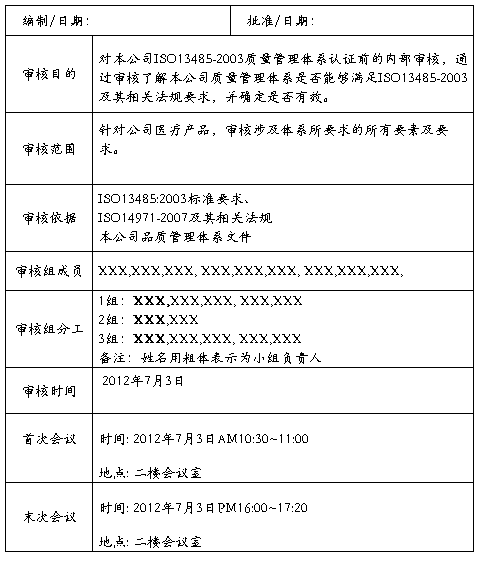
Audit Arrangements 审核安排
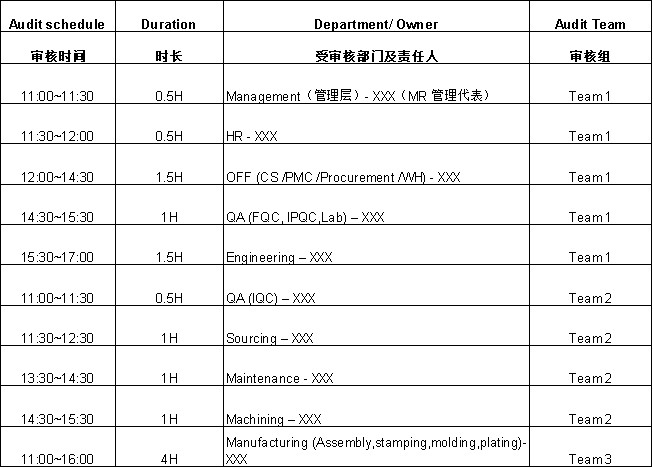
Audit Elements of Each Departments 审核要素与部门对照表

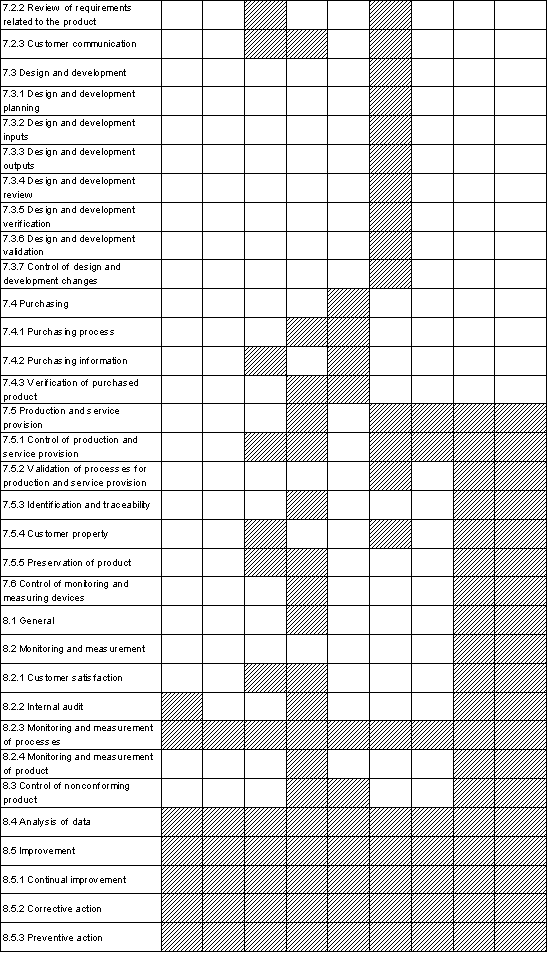
审核说明
1) 文件控制、记录控制、目标指标、职责和权限、沟通、资源提供(含培训)、过程的监视和测量、数据分析、纠正措施和预防措施等要素将贯穿所有过程的审核。
2) 在审核前,由审核组长同被审核部门沟通,已确定最终的审核时间安排。
3) 审核员不得审核本职责范围内工作.
第二篇:ISO13485 内部质量审核实施计划
内部审核实施计划
NO:

1 审核目的:
检查本公司质量管理体系是否符合ISO9001:2008 & ISO 13485:2003(YY/T 0287—2003)《医疗器械 质量管理体系 用于法规的要求》标准要求,质量体系是否有效运行。
2 审核依据:
ISO9001:2008 & ISO13485:2003(YY/T 0287—2003)标准、公司质量手册及质量管理体系文件。
3 审核覆盖产品:
轮椅、助行器、拐杖、洗澡椅。
4 审核时间:
20## 年 9月 10 日
5 现场审核期间请被审核方有关人员参加下列活动:
首、末次会议:总经理、副总经理、管理者代表及与审核有关的部门负责人、管理人员参加。
审核活动:按审核时间安排,被审核方有关人员应在本岗位上。
6 审核员分组:
审核组长:
A组 B组:
7 审核安排:
按审核时间表。
1
审核时间表
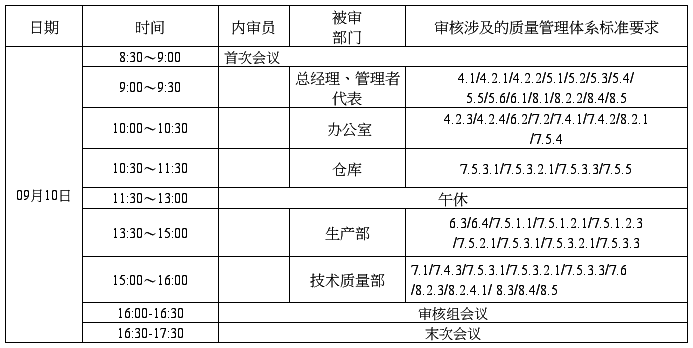
备注:
1 本次审核中,按照ISO9001:2008 & YY/T 0287标准要求进行。
2 本次审核中,每组在审核各部门时,均要审核:
文件控制(4.2.3)、质量方针(5.3)、质量目标(5.4.1)、记录控制(4.2.4)、培训(6.2)、纠正和预防措施(8.5)。
编制: 批准: 日期:
