DNA指纹图谱实验
上课地点:化学楼120 上课时间:选课时
任课教师:薛闯 办公地点:生化楼215 电话:84706308
课程要求:
预习实验内容,掌握实验目的及原理、仪器和试剂、实验步骤;
手写完成预习报告(实验名称、实验目的、实验原理、实验器材与试剂、实验方法与步骤),课堂检查预习报告情况。
自带U盘和尺子。
实验注意事项:
1、实验台上物品按实验室管理老师要求摆放整齐;
2、实验废物按实验室管理老师要求收集;
3、实验结束后,经老师检查后方可离开。
实验纪律:
1、按时上课
2、穿实验服(白大衣)
3、不许吃东西,课堂严禁大声喧哗
4、手机静音
实验成绩:
预习报告: 20分
实验操作: 40分
报告内容:结果和讨论 40分
DNA指纹图谱实验
(指导教师:薛闯)
一.实验目的 1. 掌握 DNA 指纹图谱技术的概念、原理和基本操作过程
2. 掌握琼脂糖凝胶电泳的基本操作技术,学习利用琼脂糖凝胶电泳测定 DNA 片段的长度。
3. 掌握对DNA指纹数据进行基本统计分析方法。
二 . DNA指纹图谱实验原理 1984 年英国莱斯特大学的遗传学家 Jefferys 及其合作者首次将分离的人源小卫星 DNA 用作基因探针,同人体核 DNA 的酶切片段杂交,获得了由多个位点上的等位基因组成的长度不等的杂交带图纹,这种图纹极少有两个人完全相同,故称为 "DNA指纹",意思是它同人的指纹一样是每个人所特有的。DNA指纹的图像在X光胶片中呈一系列条纹,很像商品上的条形码。由于 DNA 指纹图谱具有高度的变异性和稳定的遗传性,且仍按简单的孟德尔方式遗传,成为目前最具吸引力的遗传标记。
DNA 指纹具有下述特点:
1. 高度的特异性:研究表明,两个随机个体具有相同 DNA 图形的概率仅3×10-11 ;如果同时用两种探针进行比较,两个个体完全相同的概率小于 5×10 -19 。全世界人口约 50 亿,即 5×109 。因此,除非是同卵双生子女,否则几乎不可能有两个人的 DNA 指纹的图形完全相同。
2. 稳定的遗传性:DNA 是人的遗传物质,其特征是由父母遗传的。分析发现, DNA指纹图谱中几乎每一条带纹都能在其双亲之一的图谱中找到,这种带纹符合经典的孟德尔遗传规律,即双方的特征平均传递 50 % 给子代。
3. 体细胞稳定性:即同一个人的不同组织如血液、肌肉、毛发、精液等产生的 DNA 指纹图形完全一致。
DNA 指纹图谱法的基本操作:
从生物样品中提取 DNA
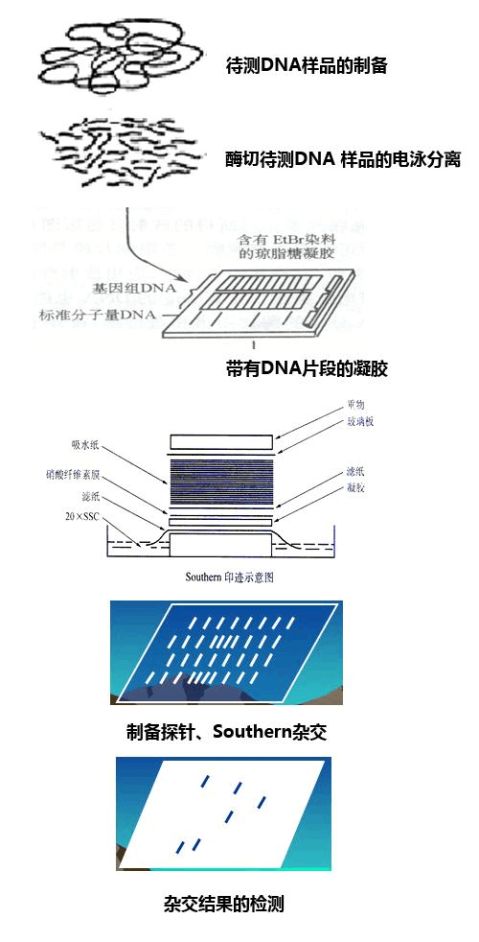
( DNA 一般都有部分的降解),可运用 PCR 技术扩增出高可变位点(如 VNTR 系统,串联重复的小卫星 DNA 等)或者完整的基因组 DNA ,然后将扩增出的 DNA 酶切成 DNA 片断,经琼脂糖凝胶电泳,按分子量大小分离后,转移至尼龙滤膜上,然后将已标记的小卫星 DNA 探针与膜上具有互补碱基序列的 DNA 片段杂交,用放射自显影便可获得 DNA 指纹图谱。
DNA 指纹图谱法的基本操作示意图
琼脂糖凝胶电泳:
琼脂糖凝胶电泳是分离,鉴定和纯化DNA 片段的常规方法。利用低浓度的荧光嵌入染料-溴化乙锭进行染色,可确定DNA 在凝胶中的位置。如有必要,
还可以从凝胶中回收DNA 条带,用于各种克隆操作。琼脂糖凝胶的分辨能力要比聚丙烯酰胺凝胶低,但其分离范围较广。用各种浓度的琼脂糖凝胶可以分离长度为200bp至近50kbp 的DNA。长度100kb 或更大的DNA,可以通过电场方向呈周期性变化的脉冲电场凝胶电泳进行分离。
在基因工程的常规操作中,琼脂糖凝胶电泳应用最为广泛。它通常采用水平电泳装置,在强度和方向恒定的电场下进行电泳。DNA 分子在凝胶缓冲液(一般为碱性)中带负电荷,在电场中由负极向正极迁移。DNA分子迁移的速率受分子大小,构象。电场强度和方向,碱基组成,温度和嵌入染料等因素的影响。
DNA指纹数据处理:
1. DNA指纹图谱的共有带率(Band-sharing,简称BS)
BS=2NAB/(NA+NB)
式中:NA指个体A的条带数,NB为个体B的条带数,NAB指个体A和个体B共有的条带数。
2. 平均等位基因频率(q)及最低平均杂合率(Ht)
q =l-(1-BS)1/2,Ht=l-q
式中BS为共有带率。
3. 两个个体具有完全相同的DNA 指纹图谱的概率(P)
两个无关个体具有完全相同的DNA 指纹图谱的概率为:
P1 =(1-2BS+2BS2 )n/BS ;
两个同胞个体具有完全相同的DNA 指纹图谱的概率为:
P2 =[1-0.5q(1-q)2(4-q)]n/BS 式中:n 为个体的平均条带数,q 为平均等位基因频率。
三 . 实验材料和试剂
1. DNA 样品:犯罪现场CS DNA 样品、嫌疑犯S1 DNA 样品、嫌疑犯S2 DNA 样品、嫌疑犯 S3 DNA 样品
2. 化学试剂和溶液
(1). TAE( 50 ×)
Tris 242g
冰醋酸 57.1ml
EDTA ( 0.5mol/L pH 8.0 ) 100ml
使用时用蒸馏水稀释 50 倍。
(2).琼脂糖 agarose (电泳级)
3. 仪器设备和消耗品
电泳仪、电泳槽、样品梳、微波炉、移液器(10 μ l)、离心管、一次性枪头,一次性手套。
四 . 实验步骤
DNA样本的琼脂糖凝胶电泳:
1. 用量筒量20ml电泳缓冲液TAE倒入烧杯中,然后用天平称量0.2g琼脂糖倒入烧杯中;
2. 用微波炉加热30秒左右使琼脂糖完全融化(当心煮沸的液体,溢出!);
3. 冷却至 65 ℃左右时用微量移液器加入10 μl GoldviewTM核酸染料,充分混匀;
4. 将制胶器置于工作台面上,将胶模和梳子分别插入制胶器内,梳子应距胶模一端约1cm,梳齿底边与胶模表面保持0.5-1mm的间隙;
5. 待琼脂糖冷却至60℃左右时,小心倒入胶模内(避免产生气泡),使凝胶缓慢展开直至在胶模表面形成一层约3mm厚的均匀胶层,室温静置30分钟;
6. 待凝固完全后,双手均匀用力轻轻拔出梳子(注意切勿使样品槽破裂),在胶模上形成相互隔开的样品槽;
7. 将凝胶连同胶模放入电泳槽平台上,倒入TAE缓冲液直至浸没过凝胶面2-3mm,小心去除样品槽中的气泡;
8. 用微量移液器缓慢地将3μL DNA样品分别加入到样品槽内,注意避免因样品过多而溢出,污染邻近样品;
9. 加样完毕后,将靠近样品槽一端连接负极,另一端连接正极,接通电源,开始电泳,在样品进胶前可用略高电压,防止样品扩散,样品进胶后,应控制电压不高于5V/cm(电压值V/电泳槽两极之间距离cm);
10. 当染料条带移动到距离凝胶前沿约1cm时,停止电泳;关闭电源,然后将胶板推至预先浸湿并铺在紫外灯观察台上的保鲜膜上,在波长254nm紫外灯下进行观察,DNA条带呈现荧光;在紫外灯下观察 DNA 的迁移位置;
11. 在电泳照片上用卡尺测量出犯罪现场DNA各片段的迁移距离(cm),以各片段分子碱基对的对数为纵坐标,它们的迁移距离为横坐标,用EXCEL软件上划出曲线,制作出DNA分子的标准曲线;并讨论实验结果。
五.作业与结果分析
1. 根据已知CS样本的DNA片段长度,计算S1,S2,S3样本的DNA片段长度。
2. 用现有的电泳图,练习计算嫌疑犯样本(S1,S2,S3)与犯罪现场CS样本图谱之间的共有带率(BS). 判断 CS 与哪一个 DNA 样品是同一个样品,找出罪犯。
3. 实验的心得体会和建议。
六. 注意事项
1.观察时应戴上防护眼镜或有机玻璃护面罩,避免紫外光对眼睛的伤害;
2.DNA存在的位置呈现荧光,肉眼可观察到清晰的条带,荧光会逐渐减弱,因此初步观察后,应立即拍照记录下电泳结果;
3.每次取DNA样品时都应换一个无菌枪头 。避免样品间污染。
4.Goldview核酸染料是一种毒性物质,使用时必须带手套 。实验结束后,含Goldview的凝胶要进行净化处理。
附件2:大连理工大学实验报告封皮范本
大连理工大学
本科实验报告
课程名称: 普通生物学实验 学院(系): 专 业: 班 级: 学 号: 学生姓名:
年 月 日
附件3:大连理工大学实验报告范本
大连理工大学实验报告
学院(系): 专业: 班级: 姓 名: 学号: 组: ___ 实验时间: 实验室: 实验台: 指导教师签字: 实验班级号: 成绩:
实验名称:DNA指纹图谱实验
一、实验目的
二、实验原理
三、实验器材与试剂
四、实验步骤与操作方法
五、实验数据记录和处理
六、实验结果与分析
七、讨论、建议、质疑
注:预习报告完成前四项即可。
第二篇:DNA指纹图谱技术

DNA指纹图谱技术在土壤微生物多样性研究中的应用
pace等于19xx年首次利用rrna基因确定环境样品中的微生物,
通过对5s rrna基因的序列分析来研究微生物的生态和进化。该方
法很快被用于微生物多样性研究领域。由于5s rrna基因相对较小,
携带信息相对较少,因而揭示微生物群落多样性的能力有限。相比
之下,随后开展的16s rrna基因序列分析为微生物多样性研究提
供了更多信息,且效率更高。目前16s rrna基因序列分析已广泛
应用于微生物多样性的研究。16s rrna基因序列分析是主要基于已
建立的微生物16s rrna基因序列数据库,用以确定细菌的系统发
育关系,并使序列探针用于识别未知菌成为可能。当然序列探针的
确定也可根据分子标记方法,如rapd方法进行。利用16s rrna基
因序列研究微生物多样性可采用不同的策略。目前一般常用以下几
种方法。
一、变性梯度凝胶电泳(dgge)和温度梯度凝胶电泳(tgge )
19xx年muyzer等将dgge技术引入环境微生物学多样性的研究。
随后该技术被广泛用于比较不同生态系统中的微生物群落的多样
性及监测特定微生物种群的动态变化,dgge和tgge的原理是根据
含有不同序列的dna片段(16s rrna基因扩增产物)在具有变性剂
梯度或温度梯度的凝胶上由于其解链行为的不同而导致迁移率的
不同,部分解链的dna片段在凝胶中的迁移速率低于完全螺旋形式
的dna分子,从而含有不同碱基序列的dna片段就得到有效分离。

结合pcr扩增标记基因或其转录物(rrna和mrna)的dgge方法能
直接显示微生物群落中优势组成成分。由于它可同时对多个样品进
行分析,使之非常适合研究微生物群落的时空变化,而且可以通过
对酶切条带进行序列分析,或通过与独特的探针杂交鉴定群落组
成,可以方便地了解环境被干扰后的微生物群落变化或某种指示微
生物的命运。oliver等用dgge方法考察了农田微生物的变化情况,
认为环境变化对农田微生物的多样性有很大影响。但是dgge/tgge
技术也存在一定的局限性。
其缺陷之一是只能分离约500 bp大小的dna片段,这限制了作为
下一步用于杂交分析的探针设计。并且研究报道有些种类细菌16s
rdna在dgge上不只显示1条带,而不同种细菌的16s rdna序列在
dgge上也可能因为具有相同的解链行为而不能被分开。即便存在以
上的一些局限性,dgge/tgge仍是分析微生物群落多样性较为敏感
的方法之一。
二、单链构象多态性(sscp)
sscp是对16s rrna基因扩增产物进行分析的另一种简便有效的方
法。该技术最初用来检测人类dna的基因多态性,lee等在19xx年
首次报道将sscp技术应用到环境样品微生物群体多样性分析。不
同碱基序列的单链dna分子构象不同,dna片段变性成单链后受到
凝胶不同分子筛作用力最终使不同dna片段得到分离。电泳结束后
可以将不同的条带切下并测序,或采用特异性探针进行杂交,进而

显示该特定微生物类群的动态变化。holly等利用sscp技术研究发
现在植物根际土壤中大量存在古菌crenarchaeot,该类微生物以往
一直被认为只存在于极端嗜热环境当中。但是sscp技术重现性较
差,易受胶浓度和电泳温度等条件的影响。另外,sscp能够有效分
离的dna序列过短,为150-400 bp。
三、随机引物扩增多态性dna(rapd )
由williams建立的rapd技术,因具有操作简便、快速和经济等
优点而得到了广泛应用。该技术以随机寡核苷酸(5-10 nt)作为
引物,扩增得到的多态性片段较短,更方便检测两个同源或异源等
位基因的有无,适用于种内和亚种更为细致的分类。张峦等在室内
培养条件下,采用rapd分子标记技术研究了重金属镉和多环芳烃
菲复合污染对土壤中微生物群落dna序列多样性的影响。结果表明,
培养15 d和30 d后,镉-菲单一和复合污染均导致土壤微生物群
落dna序列的丰度、均度和多样性指数增加。重复性不好是该技术
存在的主要问题,而dna模板的质量与数量、mgcl2和引物浓度的
变化都有可能导致得到不同的图谱。另外,从条带图谱中无法得到
任何微生物系统发育信息。
四、限制性片段长度多态性(rflp ) 和扩增核糖体dna
限制性分析rflp方法和ardra方法也常用于微生物群落的分析。
通常用引物pcr扩增得到16s rdna片段,被限制酶切割,然后再
进行电泳形成不同长度的片断进行分析。其所获得的谱带更为简

单,易于分析,不受菌株是否纯培养的限制,不受宿主的干扰,具
有特异性强,效率高的特点。广泛应用于新物种的发现、微生物分
类及鉴定、共生菌、病原菌的微生物遗传多样性的检测等。后来有
人利用ardra方法考察两种不同农田土壤的微生物群落时,发现两
者无显著差异。张于光等利用rflp方法对三江源地区不同的植物
类型的土壤中固氮微生物群组成进行了研究,发现所有土壤样品中
分别具有1-2个优势微生物种群。但是该技术所能获得的信息量相
对较少,并且难以用来评估物种的丰度和均度。
五、末端限制性片段长度多态性(t-rflp )
t-rflp是rflp/ardra方法的进一步发展,所不同的是在pcr扩增
16s rrna基因过程中,其中一个引物用荧光标记,在计算机程序自
动分析时仅分析荧光标记的末端限制片段,这样使得限制片段长度
多态性图谱更为简化,并且每个可见的条带都代表一个“核型”或
一个分类单元。此法能够得到一个群落的特征指纹图谱,可用于比
较不同群落的相似性和由于污染造成的群落结构在时间和空间上
的改变。pett等利用t-rflp技术考察氧化还原电位对土壤菌群的
影响,研究发现经过4 d的好氧/厌氧处理与未处理的土壤样品菌
群结构相似,而经过持续12 h的厌氧或好氧处理的土壤样品得到
的分子条带则明显不同,在所有样品的179种条带图谱中只有3种
是普遍存在的,同时还发现土著菌群对氧化还原电位的变化具有耐
受性。catherine等对t-rflp方法进行了完善,采用多个限制性酶

代替单一限制性酶更有利于排除选择酶的干扰,通过叠加靶基因酶
切位点,使待定鉴定种属在数据库中匹配度提高。为得到较精确的
结果,可以在产生图谱的同时,对分析样品创建克隆、测序鉴定,
但所需费用较高。
