课题4 化学式与化合价
教学目标:
1、知识与技能
(1) 了解化学式的涵义
(2) 知道一些常见的元素和根的化合价
(3) 能用化学式表示某些物质的组成,并能利用化合价推求化学式。
(4) 了解相对分子质量的涵义,并能利用相对原子质量和相对分子质量计算物质的组成。
(5) 能看懂某些商品标签或说明书上标示的物质成分和含量
2、过程与方法:
学习运用活动探究的方法,主动参与到学习中去获取知识。
3、情感态度与价值观
通过化学式的引入,对学生进行实事求是的科学态度的教育,充分培养学生的思维能力和计算能力。
重点:
一些元素和根的化合价,用化学式表示物质的组成,并利用化合价推求化学式,利用相对原子质量和相对分子质量计算物质的组成。
难点:
化学价的理解,化学式的书写,利用化合价写化学式
教法:
讲练结合
课时:三课时
第一课时
复习提问:
1、小测元素符号
2、书写物质分类表,每种物质各举两例,写出该物质的名称。
情景导入:
物质的名称很难确切表达一种物质的组成,化学式可以简单明了地表示物质分子的组成,一种纯净物只用一种化学式表示,化学式是国际通用的,它为学习和研究带来方便。
讲授新课:
一、 化学式(板书)
讲解:什么是化学式?
1、化学式:见课本第79页(板书)
2、化学式的写法、读法(板书)
(1)单质化学式的写法、读法(板书)
提问:什么是单质?(追问:单质的化学式怎样书写?)
板书:在学生板书的物质分类表各类物质的后边将名称改为化学式。
(2)化合物化学式的写法、读法(板书)
提问:什么是化合物?
讨论:化合物不是由一种元素组成而是由两种或两种以上元素组成的纯净物。书写化合物的化学式要抓住关键的两点?哪两点?
小结:书写化合物化学式的关键在抓住:元素符号排列顺序的规定;原子个数、原子个数(解码)的书写部位。
讲解:①氧化物:如:HgO、SO2、Fe3O4
写法:另一元素在前,氧元素在后
读法:氧化某 几氧化几某
②金属与非金属元素组成的化合物:如:NaCl、ZnS、KCl
写法:金属元素在左,非金属元素在右
读法:某化某
练习:课本第82页活动与探究
3、化学式的意义(板书)
提问:O2的意义?(追问:2O2的意义,再进一步追问符号O、2O表示的意义)
 小结: 表示一种物质及这种物质的组成
小结: 表示一种物质及这种物质的组成
化学式的意义: 表示这种物质的一个分子以及这种物质的分子构成(由分子构成的物质)
提问:H2O表示的意义?
小结:H2O表示:水,水是由氢氧两种元素组成;还表示一个水分子;每个水分子是由2个氢原子和1个氧原子构成。
提问:2H2O所表示的意义?
小结:由分子构成的物质化学式前面的化学计量数表示分子个
数。
 表示2个水分子
表示2个水分子
2H2O
表示每个水分子中有两个氢原子
练习:口答下列符号各表示什么意义?
H、2H、 H2 2H2
讲评并小结:元素符号前边的化学计量数表示原子个数;化学式前边的化学计量数表示分子个数(由分子
构成的物质);元素符号右下角的小数字表示构成一个分子的原子个数。构成两个氢分子的原子个数的计算:构成一个分子的原子个数与分子个数的乘积。如:两个氢分子是由4个氢原子构成。又如:两个水分子中(2H2O)中,有4个氢原子和2个氧原子。
作业:新学案
教后:
第二课时
复习提问:
1、 判断下列结构示意图是哪种原子的结构示意图
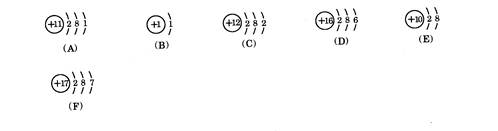
2、写出上述元素两两结合,可能形成的离子化合物与共价化合物的化学式:
小结:离子化合物的化学式:NaCl MgCl2 Na2S MgS
其原子的个数比为: 1:1 1:2 2:1 1:1
共价化合物的化学式:HCl H2O
其原子的个数比为: 1:1 2:1
引入新课:
元素相互化合时,其原子个数比都有确定的数值,如不是这个数目之比,就不能形成稳定化合物。
元素原子的最外层结构决定了原子间是按一定数目相互化合,元素的原子相互化合的数目,叫做这种元素的化合价。化合价有正负之分。
讲授新课:
一、化合价(板书)
1、概念:见课本第62页
2、 化合价的表示方法(与离子符号对比)
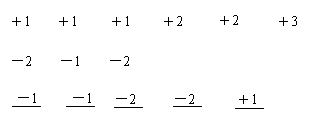
正价:H K Na Ca Cu Al
负价:O Cl S
根价:OH NO3 SO4 CO3 NH4
3、化合价实质
阅读:课文第62页,讨论后填表

二、化合价的一般夫律及常见元素的化合价(板书)
阅读:课文第80页[表4-6],根据此表总结出常见元素的化合价的一般规律。
一般规律:
化合价实质要认准;金正、非负、单质零
说明:非金属元素与氢、与金属化合显负价,与氧化合显正价
氢1(+1)、氧2(-2)应记住:正、负总价和为零;
许多元素有变价,条件不同价不同。
常见金属元素化合价顺口溜:
一价钾钠氯氢银,二价氧钙钡镁锌,三铝四硅五价磷。二三铁、二四碳,硫有负二正四六,铜汞二价最常见。正价负价
要分清,莫忘单质价为零,化合价在计算,正负和为零。
三、根据化学式会判断元素的化合价,根据元素的化合价会写化学式(板书)
1、根据化学式判断元素的化合价(板书)
判断元素化合价根据:正负总价和为零的原则。
标出下列物质中各元素的化合价
氯化锌 金属锌 氢氧化钠
解:先写出各物质的化学式
ZnCl2 Zn NaOH
然后在各化学式元素符号的正上方标出相应的的化合价(略)
注意:标化合价的方式与离子表示方式不同。
练习:课后习题2
2、已知化合物中某些元素的化合价,求另一元素的化合价
例2、试确定氯酸钾中氯元素的化合价
解:见课本第64页
练习:课后习题5、6
3、根据元素的化合价写化学式(板书)
化学式的写法:正价先,负价后。标(化合)价,
找(原子)个数
解:见课本第81页(并介绍交叉法)
注意:只有确实知道有某种化合物存在,才能根据元素的化合价写出它的化学式。切不可应用化合价任意写出实际不存在的物质的化学式。
练习:课后习题2、3、4
4、化学式的读法
化学式的读法:先写的后读,后写的先读。
氧化物:“氧化某”、“氧化亚某”“几氧化几某”
酸:“氢某酸”“某酸”
碱:“氢氧化某”、“氢氧化亚某”
盐:“某化某”、“某化亚某”“某酸某”、“某酸亚某
总结:略
作业:新学案
教后:
第三课时
复习提问:
化学式的意义如何?
引入新课:
前面学习了原子相对质量,化学式中分子的相对质量如何计算?怎样应用化学式进行计算呢?
讲授新课:
二、相对分子质量(板书)
讲解:相对分子质量概念,根据化学式的计算,利用化学式的意义引出相关的习题类型。
1、相对分子质量(板书):见课本第82页
2、根据化学式计算:(板书)——习题类型:
(1) 计算物质的相对分子质量(板书)
例1、计算N2、Fe3O4、H2SO4、Cu(OH)2的相对分子质量
解:N2的相对分子质量=14×2=28
Fe3O4的相对分子质量=56×3+16×4=98
H2SO4的相对分子质量=1×2+32+16×4=98
Cu(OH)2的相对分子质量=64+(16+1)×2=98
练习:课后习题7
(2)计算组成物质的各元素的质量比(板书)
例2:计算水中氢元素与氧元素的质量比
解:H2O中氢元素与氧元素的质量比等于
1×2∶16=1∶8
练习:课后习题8
(3)计算物质中某一元素的质量分数(板书)
例3:计算化肥硝酸铵(NH4NO3)中氮元素的质量分数
解:先根据化学式计算出相对分子质量:
NH4NO3的相对分子质量=14+1×4+14+16×3=80
再计算氮元素的质量分数:
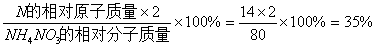
练习:1、计算氯酸钾中氧元素的质量分数
2、课后习题9
(4)化合物的质量与所含元素质量的互算(板书)
例4:为满足生产需要,要使每公顷土地增加2kg氮元素,问50公顷的土地上应需施加硝酸铵(NH4NO3)肥料多少千克?
解法一: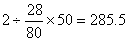 kg
kg
解法二:
50公顷土地需氮元素:50×2kg=100 kg
设50公顷的土地上应需施加硝酸铵(NH4NO3)肥料的质量为X
则:X×35%=100kg X=285.5kg
答:略
例5:若改用碳酸氢铵,多少克碳酸氢铵与285.5kg硝酸铵含氮量相当?
解:设: 与285.5kg硝酸铵含氮量相当的碳酸氢铵的质量为X

X=563.9(kg)
答:略
练习:课后习题10
介绍:药品、食品等商品的标签或说明书上常常用质量分数来表示物质的成分或纯度,请同学们根据收集来的说明书对药品、食品的有关情况作记录。
作业:新学案
教后:
第二篇:九年级化学上册教案——化学式与化合价
课题4 化学式与化合价
★ 教学目标
1.知识与技能:
(1)、了解化学式及其意义;
(2)、了解常见元素及原子团的化合价;
(3)、能用化学式表示某些物质的组成,并能利用化合价推求化学式;
(4)、了解相对分子质量的涵义,并能利用相对原子质量和相对分子质量计算物质的组成;
(5)、能看懂某些商品标签或说明书上标示的物质成分和含量。
2.过程与方法:
(1)、通过对图、表的观察,让学生学会对学过的知识进行整理归纳并初步运用;
(2)、通过讨论交流、活动探究,培养学生利用所学的知识解决实际问题的能力和基本计算能力;
3.情感、态度与价值观:
(1)、通过自编化合价口诀,激发学生的学习兴趣和求知欲;
(2)、通过讨论交流、活动探究,发展学生善于合作、勤于思考、勇于实践的精神。
★ 教学资源分析
本课题安排在第四单元的最后一部分,包括“什么是化学式”、“化合价”和“有关相对分子质量的计算”这三部分内容,它们是学习化学的重要工具,是“双基”的重要部分。虽然有元素符号知识作为基础,但仍是初三化学学习中的知识分化点。
本课题的内容比较抽象,教材首先讲述了化学式的概念,以学生最熟悉的纯净物——水为例,介绍了化学式表示的意义;接着介绍化合价知识,并以推求五氧化二磷的化学式为例讲解推求的步骤和方法,在此基础上,介绍化学式的读法;最后是有关相对分子质量的计算。课程标准对这些内容要求不高,故教学中不需要任意扩展与加深。
★ 教学策略分析
在前面的学习中,学生已具有了有关元素符号的知识,用元素符号来表示某种元素,学生兴致很高;那么,对于物质能否用专门的符号来表示呢?学生对此的求知欲望很强。但最基本的元素、原子团化合价的记忆却又是那么枯燥乏味,因此,教师要充分发挥学生的主观能动性,以试编口诀、讨论交流、活动探究等多种形式活跃课堂气氛,提高教学的效率。 ★ 教学重、难点
重点:化合价知识及其应用、有关相对分子质量的计算。
难点:1.化合价的理解及应用。
2.物质中某元素质量分数的计算。
★ 教学准备
1.有关投影片;
2.将教材P,9图4—11、P。。表4—6放大后复印。
★ 课时建议
3课时
★ 教学过程
第一课时
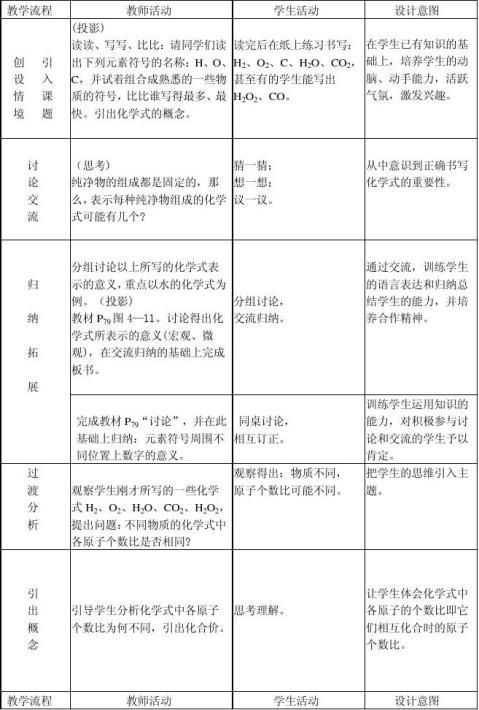
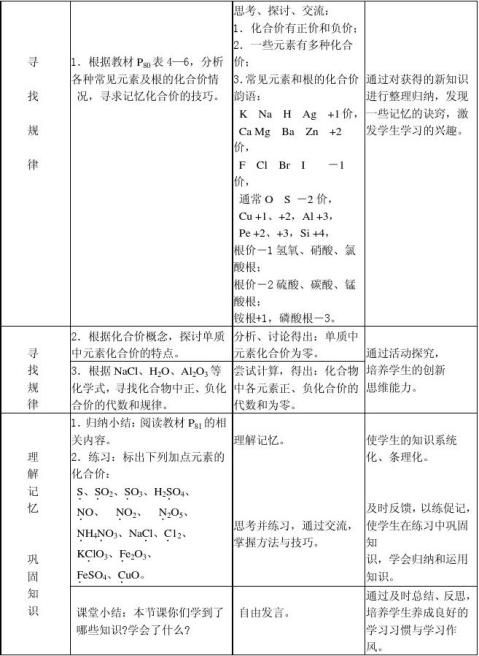
第二课时
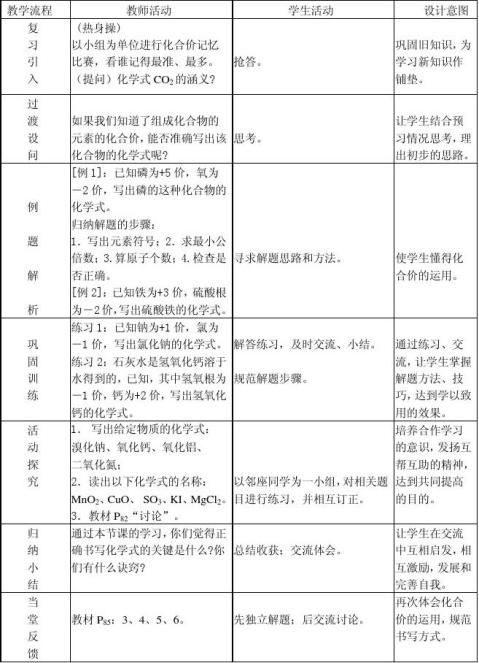
第三课时
★ 板书设计
课题4 化学式与化合价
一、化学式
1.定义:用元素符号表示物质组成的式子。(一种纯净物只有一个化学式。)
2.化学式的意义:包括宏观意义和微观意义。
二、化合价
1.原子团:
2.化合价规律:
(1)金属通常显正价,非金属通常显负价;
(2)化合物中H通常显+1价,O、S通常显—2价;
(3)单质的化合价为零;
(4)化合物中各元素的化合价代数和为零。
3.记忆规律:
4.根据化合价写化学式(最小公倍数法):
5.根据化学式判断元素或原子团的化合价(“化合价代数和为零”原则):
三、有关相对分子质量的计算
1.计算相对分子质量:
2.求化学式中各元素的质量比:
3.求化学式中某元素的质量分数:
★ 教后小记
