初三化学有关酸碱盐化合物沉淀知识汇总
1、 硫酸铜溶液跟铁反应:CuSO4 + Fe = ZnSO4 +Fe 铁表面覆盖红色物质,溶液由蓝色变浅绿色
2、 碳酸钠跟盐酸反应:Na2CO3 + 2HCl = 2NaCl +H2O +CO2↑有气泡产生固体逐渐减少
3、 碳酸氢钠跟盐酸反应:NaHCO3 + HCl = NaCl +H2O + CO2↑有气泡产生固体逐渐减少
4、 石灰石跟稀盐酸反应:CaCO3 + 2HCl = CaCl2 +H2O +CO2↑有气泡产生固体逐渐减少
5、 硝酸银跟稀盐酸反应:AgNO3 + HCl = AgCl↓ +HNO3 有白色沉淀产生
6、 氯化钡跟稀硫酸反应:BaCl2 + H2SO4 = BaSO4↓ + 2HCl 有白色沉淀产生
7、 氢氧化钙根碳酸钠溶液反应:Ca(OH)2 + Na2CO3 = 2NaOH + CaCO3↓ 有白色沉淀产生
8、 硝酸银溶液跟氢氧化钠溶液反应:AgNO3 + NaCl = AgCl↓ + NaNO3有白色沉淀产生
9、 氯化钡溶液跟硫酸钠溶液反应:BaCl2 + Na2SO4 = 2NaCl + BaSO4↓有白色沉淀产生
1、 氢氧化铜跟稀盐酸反应: Cu(OH)2 + 2HCl = CuCl2 + 2H2O 蓝色沉淀消失
2、 氢氧化铜跟稀硫酸反应: Cu(OH)2 + H2SO4 = CuSO4 + 2H2O 变成蓝色溶液
3、 氢氧化钠跟硫酸铜溶液反应:2NaOH + CuSO4 = Na2SO4 + Cu(OH)2 ↓ 有蓝色沉淀产生
4、 氢氧化钠跟氯化铁溶液反应:3NaOH + FeCl3 = Fe(OH)3↓ +3NaCl 有红褐色沉淀产生
初三化学所有酸碱盐的俗名,性质,用途
第7单元 酸 碱 盐
1. 酸碱指示剂(石蕊、酚酞)遇酸、碱溶液的变色情况;
稀盐酸 氢氧化钠溶液
紫色石蕊试液 红 蓝
无色酚酞试液 无 红
2. 常见的酸
(1)常见酸的物理性质及用途:
物理性质 用途
盐酸
(HCl) 浓盐酸是无色、有刺激性气味的液体,易挥发,在空气中冒白雾,有酸味。 重要化工产品。用于金属表面除锈、制造药物(如盐酸麻黄素、氯化锌)等;人体胃液中的盐酸可帮助消化
硫酸
(H2SO4) 浓硫酸是无色、粘稠、油状液体,有吸水性,溶于水时放热。 重要化工原料。可用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等;在实验室常用作干燥剂
(2)酸的通性:(掌握稀盐酸、稀硫酸的化学性质,知道它们的用途。) ① 酸能使酸碱指示剂显示不同的颜色;
② 酸能与多种活泼金属反应,生成氢气;
注意:活泼金属指的是在金属活动顺序表中排在(H)前面的金属,但K、ca、Na等金属可直接与水反应,Sn和Pb反应过于缓慢,所以,一般我们讨论的是Mg、Al、Zn、Fe四种金属,且与酸反应的速度依次减慢;而酸一般指盐酸和稀硫酸,因浓硫酸和硝酸有氧化性,它们与活泼金属反应时,不能产生氢气。 与稀盐酸反应 与稀硫酸反应
镁 Mg+2HCl=MgCl2+H2↑ Mg+H2SO4=MgSO4+H2↑
铝 2Al+6HCl=2AlCl3+3H2↑ 2Al+3H2SO4=Al2(SO4)3+3H2↑
锌 Zn+2HCl=ZnCl2+H2↑ Zn+H2SO4=ZnSO4+H2↑
铁 Fe+2HCl=FeCl2+H2↑ Fe+H2SO4=FeSO4+H2↑
(FeCl2 溶液、FeSO4溶液的颜色为浅绿色)
③ 酸能与某些金属氧化物反应,生成水。
铁锈 氧化铜
盐酸 Fe2O3+6HCl=2FeCl3+H2O CuO+2HCl=CuCl2+H2O
硫酸 Fe2O3+3H2SO4=Fe2(SO4)3+3H2O CuO +H2SO4=CuSO4+H2O
(FeCl3溶液、Fe2(SO4)3溶液为黄色;CuCl2溶液为绿色;CuSO4溶液为蓝色。)
3. 常见的碱
(1)常见碱的物理性质及用途:
俗名 物理性质 用途
氢氧化钠
(NaOH)
苛性钠、火碱、烧碱 纯净的氢氧化钠是白色固体,极易溶于水、溶于水时放出大量的热,能够吸收空气中的水蒸气而潮解。 重要化工原料,用于肥皂、石油、造纸、纺织和印染等工业,在生活中可用来除去油污。
氢氧化钙
(Ca(OH)2) 熟石灰、消石灰 白色粉末状固体、微溶于水、其水溶液俗称石灰水。 用于建筑材料、制漂白粉、氢氧化钠,改良土壤,制波尔多液。
氢氧化钙制取CaO+H2O=Ca(OH)2 (反应放出大量的热)
(2)碱的通性:(掌握氢氧化钠、氢氧化钙的性质,知道它们的用途。) ①碱能使酸碱指示剂显示不同的颜色;
② 碱能与某些非金属氧化物反应,生成水。
比较:2NaOH+CO2=Na2CO3+H2O与 Ca(OH)2+CO2=CaCO3↓+H2O (可用于区别两种碱)
注意:氢氧化钠的保存方法—密封保存。原因:易吸收水分潮解;能与空气中的CO2反应。
4. 酸、碱溶液的稀释方法;
浓硫酸稀释的正确操作:在稀释浓硫酸时,一定要把浓硫酸沿器壁慢注入水里,并不断搅拌。切不可将水倒进浓硫酸里。
5. 酸和碱有腐蚀性,使用时一定要注意安全;
6. 中和反应:酸和碱作用生成盐和水的反应叫中和反应。中和反应有广泛的应用。
7. 溶液的酸碱度可用pH表示。PH与溶液酸碱性的关系:
pH<7,溶液为酸性;pH=7,溶液为中性;pH>7,溶液为碱性。
用pH试纸可测定溶液的酸碱度。
8. 盐是在水溶液中能解离出金属离子和酸根离子的化合物。
1.重要的酸——盐酸.硫酸的物理性质及其用途;
2.酸的化学性质;
3.中和反应及应用;
4.浓硫酸的特性.稀释及事故的处理;
5.重要的碱——氢氧化钠和氢氧化钙的物理性质.用途及腐蚀性;
6.溶液的导电性及原因;
7.溶液酸碱度表示——pH及应用;
8.重要的盐——氯化钠.碳酸钠.碳酸钙的物理性质及用途;
9.粗盐的提纯;过滤和蒸发操作;
10.CO32-的鉴定;
11. 发生复分解反应的条件。
知识提要
1. 中常见的酸有盐酸、硫酸、硝酸等。
(1) (1) 盐酸和硫酸的物理性质
①盐酸是氯化氢的水溶液,化学上也叫氢氯酸,化学式HCl,相对分子质量为36. 5。
纯净的盐酸是无色有刺激性酸味的液体,有挥发性,和腐蚀性。
常用于制药、试剂、金属除锈及制造其他化工产品,是胃液中的主要成分,帮助消化。
②硫酸H2SO4,相对分子质量98。
纯净的浓硫酸为无色粘稠油状液体,有吸水性,易溶于水,溶解时放出大量热,有强烈的腐蚀性。
可用作一些气体的干燥剂,广泛用于生产化肥、农药、火药、染料及金属除锈、蓄电池等。
稀释浓硫酸时会放出大量的热,很易使水和酸液沸腾飞溅出来而发生事故。因此,在稀释浓硫酸时,一定要把浓硫酸沿着器壁慢慢地注入水里,并不断地用玻璃棒搅拌。
(2) (2) 盐酸和硫酸的化学性质
HCl H2SO4
①跟指示剂的作用 使紫色石蕊试液变红色
无色酚酞不变色 使紫色石蕊试液变红色
无色酚酞不变色
②跟活泼金属的反应 Mg+2HCl==MgCl2+H2↑
Fe+2HCl==FeCl2+H2↑ Zn+H2SO4==ZnSO4+H2↑
2Al+3H2SO4==Al2(SO4)3+3H2↑
③跟金属氧化物的反应 Fe2O3+6HCl=2FeCl3+3H2O
CuO+2HCl= CuCl2+H2O Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
CuO+H2SO4=CuSO4+H2O
④跟碱的中和反应 NaOH+HCl=NaCl+H2O
Cu(OH)2+2HCl=CuCl2+2H2O 2NaOH+H2SO4=Na2SO4+2H2O
Cu(OH)2+H2SO4=CuSO4+2H2O
⑤跟某些盐的反应 CaCO3+2HCl=CaCl2+H2O+CO2↑
HCl+AgNO3=AgCl↓+HNO3 H2SO4+Na2CO3=Na2SO4+H2O+CO2↑
H2SO4+BaCl2=BaSO4↓+2HCl
2. 生活中常见的碱有氢氧化钠、氢氧化钙等
(1) (1) 氢氧化钠、氢氧化钙的物理性质
①氢氧化钠化学式NaOH,相对分子质量是40,俗名叫火碱、烧碱、苛性钠。 纯净的氢氧化钠为白色固体,在空气中易吸湿而潮解。极易溶于水且放热。有强烈的腐蚀性。
可用作干燥剂,广泛用于制肥皂、石油、造纸、纺织和印染等。
②氢氧化钙化学式Ca(OH)2,相对分子质量74,俗名熟石灰、消石灰等
氢氧化钙是白色粉末,微溶于水,放热,其澄清水溶液叫石灰水,有腐蚀性和吸湿性。
用于建筑业、农业上的改良酸性土壤等。
(2) (2) NaOH和Ca(OH)2的化学性质
NaOH Ca(OH)2
①跟指示剂的反应 使紫色石蕊变蓝色
使无色酚酞变红色 使紫色石蕊变蓝色
使无色酚酞变红色
②跟非金属氧化物的反应 2NaOH+CO2=Na2CO3+H2O
2NaOH+SO2=Na2SO3+H2O Ca(OH)2+CO2=CaCO3↓+H2O
③跟酸的中和反应 NaOH+HNO3=NaNO3+H2O Ca(OH)2+2 HCl=CaCl2+ 2H2O
3. 常见的盐有氯化钠、碳酸钠、碳酸钙等
①氯化钠化学式NaCl,广泛分布在海水、盐湖、盐井、盐矿中,它是食盐的主要成分,是一种白色有咸味的固体,易溶于水,溶解度受温度变化影响不大。对维持人体体液的平衡起着重要作用。它是重要的化工原料,用于制造烧碱、氯气、盐酸、漂白粉、纯碱等,医疗上的生理盐水、农业上的选种等用途。
②碳酸钠化学式Na2CO3,俗名纯碱或苏打,是白色易溶于水的固体。它是一种重要的化工原料,用于玻璃、造纸、纺织和洗涤剂的生产等。
③碳酸钙化学式CaCO3。它是石灰石、大理石的主要成分,是一种白色难溶于水的固体。石灰石、大理石是重要的建筑材料。还可作人体补钙剂。
4. 常见的化肥氮肥、磷肥、钾肥和复合肥。
(1)常见的氮肥有铵盐如NH4Cl、NH4HCO3,硝酸盐如NH4NO3和NaNO3,还有尿素CO(NH2)2、氨水NH3?H2O等。氮是植物体内蛋白质、核酸和叶绿素的组成元素,能促进作物的茎、叶生长茂盛,叶色浓绿。
(2)常见的磷肥有磷矿粉Ca3(PO4)2、钙镁磷肥、过磷酸钙〖Ca (H2PO4)2和CaSO4的混合物〗。磷是植物体内核酸、蛋白质和酶等多种重要化合物的组成元素,可以促进作物生长,增强作物的抗寒、抗旱能力。
(3)常用的钾肥有K2SO4和KCl等。钾具有保证各种代谢过程的顺利进行、促进植物生长、增强抗病虫害和抗倒伏能力等功能。
(4)时含有两种或两种以上的营养元素的化肥叫复合肥料。如KNO3和NH4H2PO4等。
化肥对提高农作物产量有重要作用,但不合理的使用也对环境造成一定的污染。
5. CO32-的鉴定:
取样品与试管中,加入稀盐酸,如有能使澄清石灰水变浑浊的气体产生,证明样品中含有CO32-。
6. 复分解反应的条件:只有两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生。
初三化学酸碱盐中哪些物质可溶?哪些物质沉淀?及一些特殊性质的物质
碱(氢氧根) 除铵根、钾离子、钠离子、钡离子以外其他都不溶
硝酸盐遇水无影踪(全可溶解)
氯化物不容氯化银
硫酸盐不容硫酸钡 硫酸钙(微溶)
碳酸盐只溶钾 钠 铵 氢根
初中这个口诀够用了~
常见的沉淀:五白、一蓝、一红褐
五白:AgCl、BaSO4 、BaCO3、CaCO3、Mg(OH)2 一蓝:Cu(OH)2 一红褐:Fe(OH)3
特殊的如 NaHCO3 既能与酸又能与碱反应 NH3 是唯一的碱性气体
第二篇:初三化学酸碱盐知识点汇总
育英辅导班
初三化学《酸-碱-盐》知识点总结
一、酸、碱、盐的组成
酸是由氢元素和酸根组成的化合物 如:硫酸(H2SO4)、盐酸(HCl)、硝酸(HNO3) 碱是由金属元素和氢氧根组成的化合物 如:氢氧化钠、氢氧化钙、氨水(NH3·H2O) 盐是由金属元素元素(或铵根)和酸根组成的化合物 如:氯化钠、碳酸钠
酸、碱、盐的水溶液可以导电(原因:溶于水时离解形成自由移动的阴、阳离子) 二、酸
1、浓盐酸、浓硫酸的物理性质、特性、用途
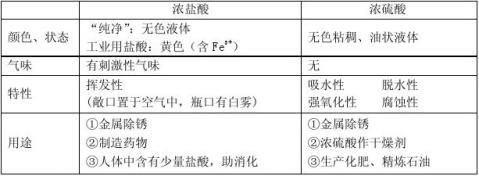
2(1)碱溶液与酸碱指示剂的反应: 使紫色石蕊试液变蓝色,使无色酚酞试液变红色 (2)酸性氧化物+碱 → 盐+水 (3)酸+碱 → 盐+水
(4)盐+碱 → 另一种盐+另一种碱(反应物均可溶,产物符合复分解条件) 注:①难溶性碱受热易分解(不属于碱的通性) 如Cu(OH)2O
2Fe(OH)2O3+3H2O
②常见沉淀:AgCl↓ BaSO4↓ Cu(OH)2↓ F e(OH)3↓ Mg(OH)2↓ BaCO3↓ CaCO3↓ ③复分解反应的条件:当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生。
五、酸性氧化物与碱性氧化物
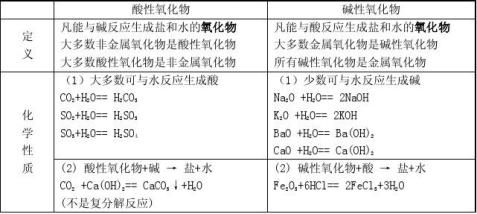
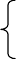

1、定义:酸与碱作用生成盐和水的反应 2、应用:
(1)改变土壤的酸碱性 (2)处理工厂的废水
(3)用于医药
3、溶液酸碱度的表示法——pH
2(1)与酸碱指示剂的反应: 使紫色石蕊试液变红色,不能使无色酚酞试液变色 (2)金属 + 酸 → 盐 + 氢气
(3)碱性氧化物 + 酸 → 盐 + 水
(4)碱 + 酸 → 盐 + 水
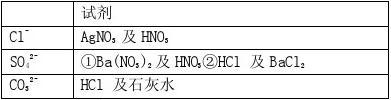
(5)盐 + 酸 → 另一种盐 + 另一种酸(产物符合复分解条件) 3、三种离子的检验

三、碱
1、氢氧化钠、氢氧化钙的物理性质、用途

(1)0 7 14
(2)pH的测定:最简单的方法是使用pH试纸
用玻璃棒(或滴管)蘸取待测试液少许,滴在pH试纸上,显色后与标准比色卡对照,读出溶液的pH(读数为整数)
育英辅导班初中化学资料
育英辅导班
(3)酸雨:正常雨水的pH约为5.6(因为溶有CO2)
pH<5.6的雨水为酸雨
育英辅导班初中化学资料
