初三化学知识点总结—酸、碱、盐
一.酸碱盐的组成与性质
酸、碱、盐的组成:
酸是由氢元素和酸根组成的化合物如:硫酸(H2SO4)、盐酸(HCl)、硝酸(HNO3)
碱是由金属元素和氢氧根组成的化合物如:氢氧化钠、氢氧化钙、氨水(NH3·H2O)
盐是由金属元素元素(或铵根)和酸根组成的化合物如:氯化钠、碳酸钠
酸、碱、盐的水溶液可以导电(原因:溶于水时离解形成自由移动的阴、阳离子)
1.酸
(1)浓盐酸、浓硫酸的物理性质、特性、用途

(2)酸的通性(具有通性的原因:酸离解时所生成的阳离子全部是H+)
① 与酸碱指示剂的反应:使紫色石蕊试液变红色,不能使无色酚酞试液变色
②金属+酸→盐+氢气
③碱性氧化物+酸→盐+水
④碱+酸→盐+水
⑤盐+酸→另一种盐+另一种酸(产物符合复分解条件)
(3).三种离子的检验
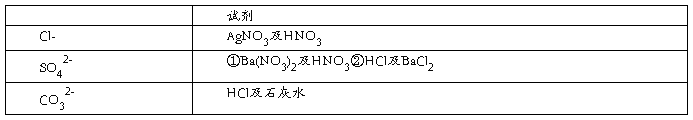
2.碱
⑴氢氧化钠、氢氧化钙的物理性质、用途

⑵碱的通性(具有通性的原因:离解时所生成的阴离子全部是OH-)
①碱溶液与酸碱指示剂的反应:使紫色石蕊试液变蓝色,使无色酚酞试液变红色
②酸性氧化物+碱→盐+水
③酸+碱→盐+水
④盐+碱→另一种盐+另一种碱(反应物均可溶,产物符合复分解条件)
注:a.难溶性碱受热易分解(不属于碱的通性)
如Cu(OH)2ΔCuO+H2O
2Fe(OH)3ΔFe2O3+3H2O
B.常见沉淀:AgCl↓BaSO4↓Cu(OH)2↓F e(OH)3↓Mg(OH)2↓BaCO3↓CaCO3↓
C.复分解反应的条件:当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生。
3.酸性氧化物与碱性氧化物

4.中和反应溶液酸碱度的表示法--pH
⑴定义:酸与碱作用生成盐和水的反应
⑵应用:
①改变土壤的酸碱性
②处理工厂的废水
③用于医药
⑶溶液酸碱度的表示法--pH
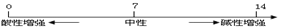 ①
①
②pH的测定:最简单的方法是使用pH试纸
用玻璃棒(或滴管)蘸取待测试液少许,滴在pH试纸上,显色后与标准比色卡对照,读出溶液的pH(读数为整数)
③酸雨:正常雨水的pH约为5.6(因为溶有CO2)
pH<5.6的雨水为酸雨
二.单质、氧化物、酸、碱、盐的相互关系
(1)金属单质+酸---盐+氢气(置换反应)
1.锌和稀硫酸Zn+H 2SO4=ZnSO4+H 2 ↑(最常用)
(实验室制H2用的金属有Zn,Fe,Mg,Al,酸有稀H2SO4和稀HCl)
(2)金属单质+盐(溶液)---另一种金属+另一种盐
2.铁和硫酸铜溶液反应:Fe+CuSO4=FeSO4+Cu
3.铝和硝酸银溶液反应:Al+3AgNO3=Al(NO3)3+3Ag
(3)碱性氧化物(金属氧化物)+酸---盐+水
4.氧化铁和稀硫酸反应:Fe2O3+3H2SO4=Fe2(SO4)3+3H 2 O
5.氧化钙和稀盐酸反应:CaO+2HCl=CaCl2+H 2 O (4)酸性氧化物(非金属氧化物)+碱--------盐+水
6.苛性钠暴露在空气中变质:2NaOH+CO2=Na2CO3+H 2 O
7.消石灰放在空气中变质:Ca(OH)2+CO2=CaCO3↓+H 2 O
(5)酸+碱--------盐+水(中和反应)
8.盐酸和烧碱反应:HCl+NaOH=NaCl+H2O
9.盐酸和氢氧化钙反应:2HCl+Ca(OH)2=CaCl2+2H 2 O
10.氢氧钠和硫酸反应:2NaOH + H2SO4==Na2SO4+2H2O 3 2 4
(6)酸+盐--------另一种酸+另一种盐
11.大理石与稀盐酸反应:CaCO3+2HCl=CaCl2+H 2 O+CO 2 ↑(实验室制CO2)
12.碳酸钠与稀盐酸反应:Na 2CO3 +2HCl=2NaCl+H 2 O+CO 2 ↑
13.硫酸和氯化钡溶液反应:HSO4+BaCl2=BaSO4↓+2HCl
(7)碱+盐---另一种碱+另一种盐
14.氢氧化钙与碳酸钠:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
15.硫酸铜溶液与氢氧化钡:CuSO4+Ba(OH)2=BaSO4↓+Cu(OH)2↓
(8)盐+盐---两种新盐
16.氯化钠溶液和硝酸银溶液:NaCl+AgNO3=AgCl↓+NaNO3
17.硫酸钠和氯化钡:Na2SO4+BaCl2=BaSO4↓+2NaCl
复分解反应必须生成沉淀,气体或水生成才能发生,且生成物的元素化合价不变。
+1价:HClO;NaClO;Ca(ClO)2.
+5价:HClO3;KClO3.
+7价:HClO4;KClO4.
第二篇:专题2 九年级酸碱盐化学方程式总结(表格)
专题二 九年级化学方程式总结
化学方程式是学习化学的语言,是学习化学的基础。每年河南中考试卷涉及的有关化学方程式的试题分值有10-15分,可见化学方程式对我们确实非常重要。要熟练准确地书写化学方程式特别是有关酸碱盐的化学方程式,须掌握好以下化学基础知识。 1, 复分解反应的特点:双交换,价不变(中间结合,两边结合,化合价不变)
AB+CD===AD+CB
如: H2SO4 + 2NaOH === Na2SO4 + 2H2O
2,化合价知识
以下元素或原子团在化合物中一般只有一种化合价,它们分别是: +1 -1 +1 +1 +1 -1 -1 一价:H Cl K Na Ag 一价 : NO3 OH -2 +2 +2 +2 +2 -2 -2 二价:O Ca Ba Mg Zn 二价 : SO4 CO3 +3 +1 +1 三价:Al 四价:Si 正一价: NH4 你能应用以上元素或原子团组成化合物吗?试一试
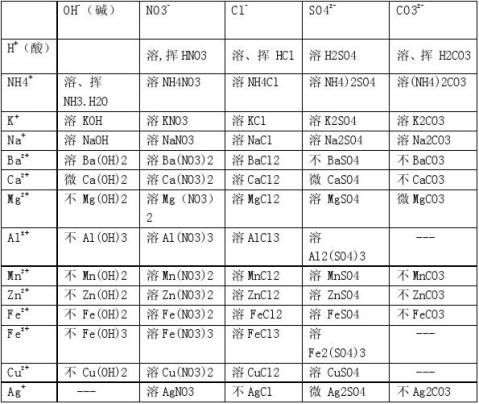
横酸竖碱片盐
盐:钾钠铵盐都易溶,硝酸盐见水影无踪,氯化物不溶氯化银(AgCl) ,硫酸
盐不溶钡和铅(BaSO4) 碳酸盐只溶钾钠铵(BaCO3, CaCO3) 。 碱:钾钙钠钡氨碱可溶
Fe(OH)3(红褐色),Cu(OH)2 (蓝色),其它碱和盐大多白色
1
注:记住7种不溶物Mg(OH)2, Al(OH)3,Fe(OH)3(红褐色),Cu(OH)2 (蓝色), AgCl(不溶酸), BaSO4(不溶酸), BaCO3, CaCO3 一,有关酸碱盐的化学方程式
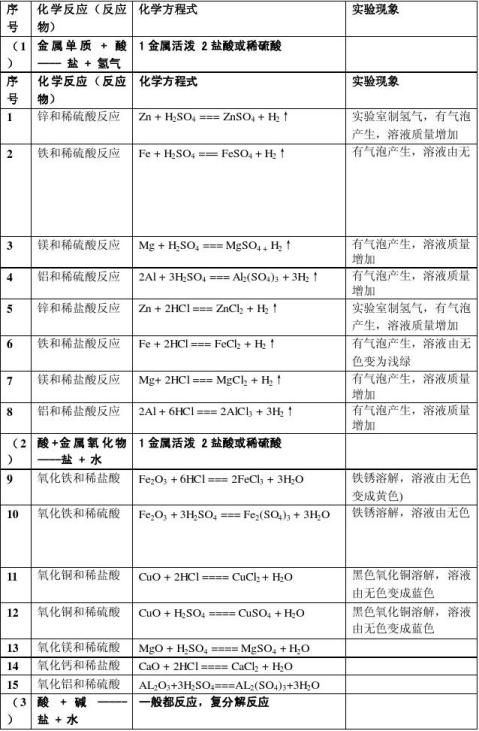
2
3
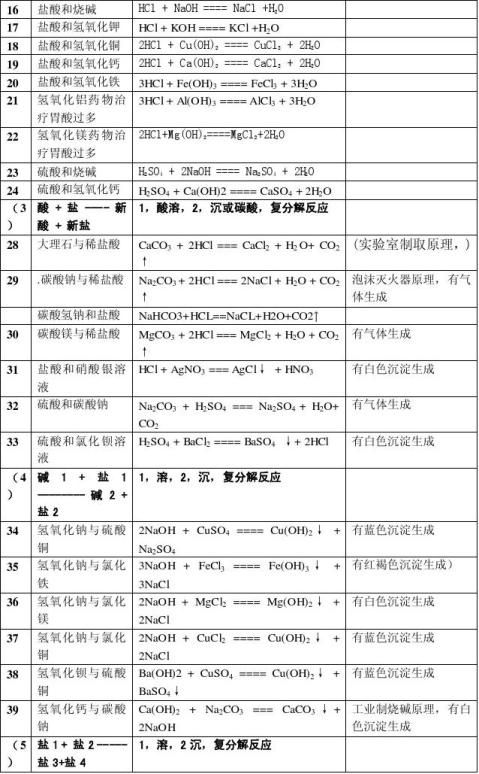
化学1-9单元化学方程式
4
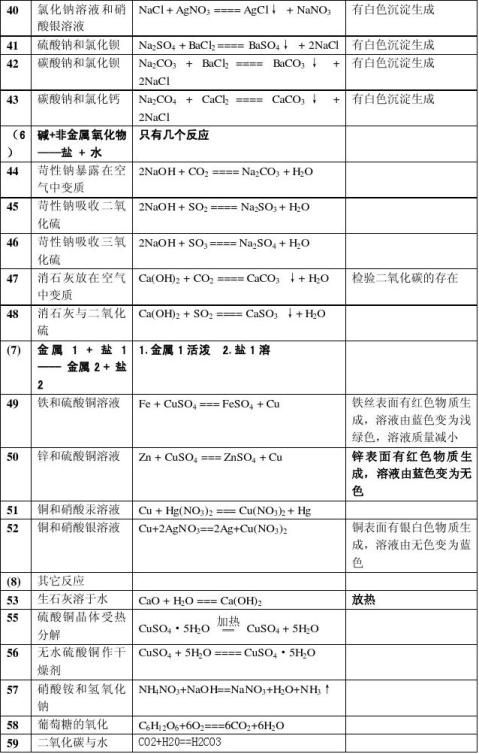
5
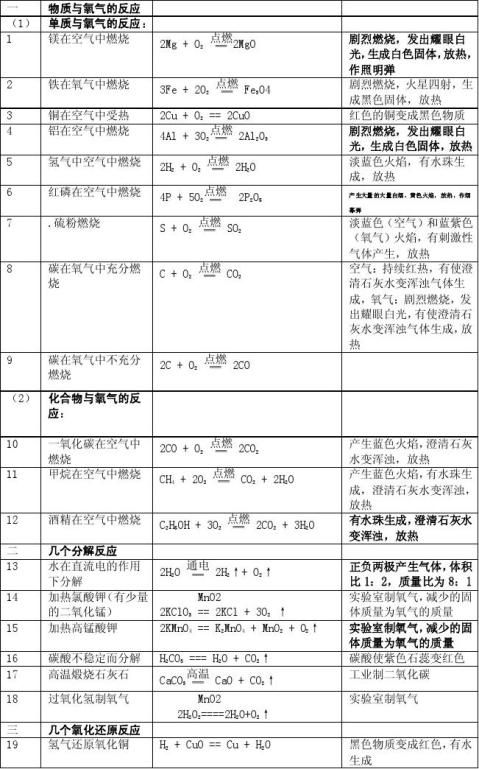
寄语同学们:
聪明来自勤奋,成功来自努力。 习惯决定成绩,细节决定成败。
成功往往不是取决于你的智力,而是取决于你的态度和学习方法! 智力很好的同学往往并未成功,实现理想,为什么? 请妥善保存,丢失不补
6

