2010高考高三化学知识点详解大全
——《物质的量_气体摩尔体积》 考点一 物质的量、阿伏加德罗常数、摩尔质量
1.物质的量
(1)物质的量是七个基本物理量之一,其意义是表示含有一定量数目的粒子的集体。
符号为:n ,单位为:摩尔(mol)。
(2)物质的量的基准(NA):以0.012kgC所含的碳原子数即阿伏加德罗常数作为物质
的量的基准。阿伏加德罗常数可以表示为NA,其近似值为6.02×10 mol
2.摩尔质量(M)
1摩尔物质的质量,就是该物质的摩尔质量,单位是g/mol 。1mol任何物质均含有阿伏加德罗常数个粒子,但由于不同粒子的质量不同,因此,1 mol不同物质的质量也不同;C的相对原子质量为12,而12 g C所含的碳原子为阿伏加德罗常数,即1 mol C的质量为12g。同理可推出1 mol其他物质的质量。
3.关系式:n =N;n =m
NAM12121223-112
[例1]下列关于物质的量的叙述中,正确的是( )
A.1mol食盐含有6.02×10个分子 B.Mg的摩尔质量为24
C.1mol水中含有2mol氢和1mol氧 D.1molNe含有6.02×10个电子
[解析] NaCl为离子化合物,其结构中无分子,且食盐为宏观物质,不可用mol来描述,
故A不正确;Mg的摩尔质量为24g/mol,单位不对,故B不正确;C中对1mol水的组成的描述不正确,应为:1mol水中含有2mol氢原子和1mol氧原子;故答案为D。
[答案]D
特别提醒:
1.摩尔只能描述原子、分子、离子、质子、中子和电子等肉眼看不到、无法直接称量的化学微粒,不能描述宏观物质。如1mol麦粒、1mol电荷、1mol元素的描述都是错误的。
2.使用摩尔作单位时,应该用化学式(符号)指明粒子的种类。
如1mol水(不正确)和1molH2O(正确);1mol食盐(不正确)和1molNaCl(正确)
3.语言过于绝对。如6.02×10mol就是阿伏加德罗常数;摩尔质量等于相对原子质量、相对分子质量;1摩尔任何物质均含有阿伏加德罗常数个粒子等。
232423-1
考点二 气体摩尔体积
1.定义:单位物质的量的气体所占的体积,叫做气体摩尔体积。
2.表示符号:Vm
3.单位:L/mol(或L·mol) -1
4.标准状况下,气体摩尔体积约为22.4L/mol
5.数学表达式:气体的摩尔体积=气体所占的体积, 即Vm?气体的物质的量V n
[例2](2009·广州七区联考)下列有关气体体积的叙述中,正确的是( )
A.一定温度和压强下,各种气态物质体积的大小,由构成气体的分子的大小决定
B.一定温度和压强下,各种气态物质体积的大小,由构成气体的分子数决定
C.不同的气体若体积不同,则它们所含的分子数也不同
D.气体摩尔体积是指1mol任何气体所占的体积约为22.4L
[解析]决定物质体积的因素有:①微粒数的多少②微粒本身的大小③微粒间的距离,其
中微粒数的多少是决定物质体积大小的主要因素。对于气体物质,在一定温度和压强下,其体积的大小主要由分子数的多少来决定,故A不正确,B正确;气体的体积随温度和压强的变化而变化。体积不同的气体,在不同的条件下,其分子数可能相同,也可能不同,是无法确定的,故C不正确;气体摩尔体积是指1mol任何气体所占的体积,其大小是不确定的,会随着温度、压强的变化而变化,22.4L/mol是标准状况下的气体摩尔体积,故D不正确。
[答案]B
特别提醒:
气体摩尔体积的一个特例就是标准状况下的气体摩尔体积(V0)。在标准状况下,1mol任何气体的体积都约等于22.4 L。在理解标准状况下的气体摩尔体积时,不能简单地认为“22.4 L就是气体摩尔体积”,因为这个22.4 L是有特定条件的。这些条件就是: ①标准状况,即0℃和101.325 kPa,气体的物质的量为1 mol,只有符合这些条件的气体的体积才约是22.4 L。因此,22.4 L是1 mol任何气体在标准状况下的体积。 ②这里所说的标准状况指的是气体本身所处的状况,而不指其他外界条件的状况。例如,“1 mol H2O(g)在标准状况下的体积为22.4 L”是不正确的,因为在标准状况下,我们是无法得到气态水的。
③1mol任何气体的体积若为22.4 L,它所处的状况不一定就是标准状况。根据温度、压强对气体分子间平均距离的影响规律知,温度升高一倍或压强降低一半,分子间距将增大一倍;温度降低一半或压强增大一倍,分子间距将减小一半。由此可知,1 mol任何气体在0℃ 、101 kPa条件下的体积与273℃ 、202kPa条件下的体积应相等,都约为22.4L。
考点三 阿伏加德罗定律及其推论
1.阿伏加德罗定律:
在同温同压下,同体积的气体含有相同的分子数。即:T1=T2;P1=P2 ;V1=V2 ? n1 = n2
2.阿伏加德罗定律的推论:
(1)三正比:
同温同压下,气体的体积比等于它们的物质的量之比.V1/V2=n1/n2
同温同体积下,气体的压强比等于它们的物质的量之比.p1/p2=n1/n2
同温同压下,气体的密度比等于它们的相对分子质量之比.M1/M2=ρ1/ρ2
(2)二反比:
同温同压下,相同质量的任何气体的体积与它们的相对分子质量成反比.V1/V2=M2/M1同温同体积时,相同质量的任何气体的压强与它们的摩尔质量的反比.p1/p2=M2/M1。
(3)一连比:
同温同压下,同体积的任何气体的质量比等于它们的相对分子质量之比,也等于它们的密度之比。m1/m2=M1/M2=ρ1/ρ2
(注:以上用到的符号:ρ为密度,p为压强,n为物质的量,M为摩尔质量,m为质量,V 为体积,T为温度;上述定律及其推论仅适用于气体,不适用于固体或液体。)
[例3](全国理综I)在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是( )
A.p(Ne)>p(H2)>p(O2) B.p(O2)>p(Ne)>p(H2)
C.p(H2)>p(O2)>p(Ne) D.p(H2)>p(Ne)>p(O2)
[解析]根据阿伏加德罗定律,当它们的温度和密度相同时,摩尔质量与压强成反比,摩
尔质量由小到大的顺序为H2<Ne<O2
[答案]D
考点四 混合气体的平均摩尔质量
1.已知混合物质的总质量m(混)和总物质的量n(混):M(混)=m(混) n(混)
2.已知混合物各成分的摩尔质量和在混合体系内的物质的量分数或体积分数。
M(混)=M1×n1%+M2×n2%+??=M1×V1%+M2×V2%+??
3.已知标准状况下混合气体的密度:M(混)=22.4ρ(混)
4.已知同温同压下与单一气体A的相对密度:M(混)=?(混) M(A)?(A)
[例4](2009·山东泰安)已知NH4HCO3NH3+H2O+CO2↑,则150℃时NH4HCO3分解产生
倍。 的混合气体A的密度是相同条件下H2密度的 A.26.3 B.13.2 C.19.8 D.无法计算
[解析]假设NH4HCO3为1 mol,则其质量为79 g ,完全分解产生的气体为3 mol ,故
有:M混合气体=79g/3mol =26.3g/mol;又由“相同条件下,气体的密度比等于其摩尔质量比”,故混合气体A的密度是相同条件下H2密度的26.3/2 = 13.2倍。
[答案]B
第二篇:测量学知识点总结
测量学是研究地球的形状和大小以及确定地面点位的科学。测定、测设两部分内容
测定是使用测量仪器和工具,通过测量和计算,得到一系列测量数据或成果,将地球表面的地形缩绘成地形图,供经济建设,国防建设,规划设计及科学研究使用。测设(放样)是指用一定的测量方法,按要求的精度,把设计图纸上规划好的建(构)筑物的平面位置和高程标定在实地上,作为施工依据。
1954年北京坐标系,新1954年北京坐标系,1980年国家大地坐标系(现用)
独立平面直角坐标:一般将坐标原点选在测区的西南角,使测区内的点坐标均为正值。
一个城市只应采取一个统一的高程系统。
俩点间高差与高程起算面无关 现逐步归算至全国统一的1985国家高程基准
1、地球的自然表面 2、地球的物理表面——水准面 3、地球的数学表面——旋转椭球体面
铅垂线:重力的方向线称为铅垂线—基准线
水准面: 任何一点都与重力方向相垂直的面。或水在静止时的表面。
水平面: 与水准面相切的平面。
大地水准面: 与平均海水面相吻合并向大陆岛屿延伸而形成的封闭曲面称为大地水准面——测量基准面 所包围的形体称为大地体。
地球椭球体: 椭圆绕其短轴旋转而成的旋转椭球体,又称地球椭球体。
地面点位的确定:地面点的空间位置须由三个参数来确定,即该点在大地水准面上的投影位置(x,y)和该点的高程H。
测量坐标系与数学坐标系的区别:坐标轴不同;象限旋转顺序不同
地面点的高程(1)绝对高程:地面点到大地水准面的铅垂距离,称为该点的绝对高程,简称高程,用H表示(2)相对高程:地面点到假定水准面的铅垂距离,称为该点的相对高程或假定高程。(3)高差:地面两点间的高程之差,称为高差,用h表示。高差有方向和正负。
用水平面代替水准面的限度:平面坐标:半径10km范围内
? 高程:影响大,一般超过200m即需改正
测量工作的程序1、控制测量(平面控制测量和高程控制测量):2、碎部测量:以控制点为依据,测定控制点至碎步点之间的水平距离,高差及其相对于某一已知方向的角度来确定碎部点的位置。 平面控制测量的形式:导线测量,三角测量,交会定点
测量工作的原则:1、在布局上 遵循“由整体到局部”的原则,在精度 “由高级到低级”,在程序上 “先控制后碎部”.2、在测量过程中,遵循“随时检查,杜绝错误”的原则
测量的基本工作:测距离、角度、高差是测量的基本工作
距离、水平角、高差称测量三要素 观测、计算、绘图是测量工作的基本技能
水准测量原理:水准测量是利用水准仪提供的水平视线,借助于带有分划的水准尺,直接测定地面上两点间的高差,然后根据已知点高程和测得的高差,推算出未知点高程。
A、B两点间高差hAB为: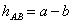 >0(B比A高)。高差等于后视读数减去前视读数。
>0(B比A高)。高差等于后视读数减去前视读数。
高差法: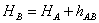 视线高法
视线高法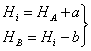 转点作用:传递高程
转点作用:传递高程
水准测量所使用的仪器为水准仪,工具有水准尺和尺垫。 组成:望远镜,水准器,基座
水准仪的操作1、安置仪器2、粗略整平3、瞄准水准尺4、精确整平5、读数
视差:眼睛在目镜端上下移动有时可看见十字丝的中丝与水准尺影像之间相对移动的现象。
产生的原因:水准尺的尺像与十字丝平面不重合。
消除的方法:依次调焦:目镜调焦使十字丝清晰;仔细地转动物镜对光螺旋,直至尺像与十字丝平面重合。
用水准测量的方法测定的高程控制点,称为水准点。
在水准点间进行水准测量所经过的路线,称为水准路线。 相邻两水准点间的路线称为测段。
水准路线布设形式主要有:1.附合水准路线2.闭合水准路线3.支水准路线4.水准网
普通水准测量方法检核1、测站检核:变仪器高法(高差0.1m以上误差5mm以内)和双面尺法(同一尺红黑面3mm以内,黑面吃高差与红面尺高差5mm)
2、计算检核: ∑a-∑b=∑h=2∑h平均=2(H终-H起)
3、成果检核: 附合水准路线: ∑h理=H终-H始 闭合水准路线: ∑h理=0
支水准路线: ∑h往理+ ∑h返理=0
目的:求 各点高程
误差分类:仪器误差,观测与操作者误差,外界环境影响
前后视距相等可消除i角残余误差对高差影响和地球曲率和大气折光对高差影响
视准轴CC :十字丝交点与物镜光心的连线 水准管轴LL:过零点与内表面相切的直线
CC∥LL —构造满足的主要条件 圆水准器轴L′L′ 过零点的球面法线。L′L′∥VV。
水准仪应满足的几何条件(1)圆水准轴L′L′∥VV;(2)十字丝的中丝^仪器竖轴VV(3)水准管轴LL∥视准轴CC 。
1.圆水准器的检校检校目的:L′L′∥VV
检验方法:整平圆气泡,转180°,若气泡仍居中,条件满足,否则,需校正。
校正方法:校正螺丝校一半,脚螺旋调一半。
2.十字丝中丝的检校:检校目的:十字丝中丝^ VV
检验方法:瞄准一固定点,转动望远镜,若该点始终沿中丝移动,说明条件满足,否则需校正。 校正方法:转动十字丝环,直至中丝水平
3.水准管的检校检校目的: LL∥CC
检验方法(1)水准仪在A、B中点测出正确高差hAB(2)水准仪在B点附近,得A尺应有读数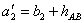 (3)计算
(3)计算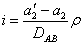 若 i>20″,校正。
若 i>20″,校正。
校正方法:转动微倾螺旋,使十字丝的中丝对准A点尺上应读读数a2′,此时视准轴处于水平位置,而水准管气泡不居中。
用校正针先拨松水准管一端左、右校正螺钉,再拨动上、下两个校正螺钉,使偏离的气泡重新居中,最后要将校正螺钉旋紧。
角度测量包括水平角测量和竖直角测量。
水平角测量原理:水平角(求算地面点的平面位置:地面上某点到两目标的方向线铅垂投影在水平面上所成的角度。 用β表示,0?~360?。
竖直角α (求算高差或将倾斜距离换算成水平距离):在同一竖直面内,地面某点至目标方向线与水平视线间的夹角,又称倾角。
视线在水平线的上方,为仰角,符号为正; 视线在水平线的下方,为俯角,符号为负。
测量原理:视线水平时的竖盘读数为一常数(90?的倍数)。
组成:照准部,基座,水平读盘 基本操作:安置仪器,瞄准目标,读数
安置仪器(1)对中目的:仪器水平读盘中心与测站点位于同一铅垂线上。(方法:垂球:误差<3mm 光学:误差<1mm)(2)整平目的:使仪器竖轴处于铅垂位置,水平度盘处于水平位置(方法:升降脚架使圆气泡大致居中;转脚螺旋,使长气泡居中)
水平角的观测:测回法,方向观测法
1.测回法的观测方法(1)在测站点O安置经纬仪(2)盘左位置:顺时针转动照准部观测(3)盘右位置:逆时针转动照准部观测
2.方向观测法的观测方法(1)在测站点O安置经纬仪(2)盘左位置:顺时针转动照准部观测(3)盘右位置:逆时针转动照准部观测
盘左位置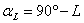 盘右位置
盘右位置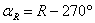 一测回竖直角
一测回竖直角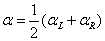
竖盘指标偏离正确位置的差值x角,称为竖盘指标差。
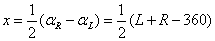
竖直角观测(1)在测站点O安置经纬仪(2)盘左位置:(3)盘右位置:
经纬仪的轴线及各轴线间应满足的几何条件(1)水准管轴LL^竖轴VV;(2)十字丝竖丝^横轴HH;(3)视准轴CC^HH;(4)HH^VV;(5)竖盘指标指在正确的位置
1.照准部水准管轴的检校(1)检校目的:L L ^ V V(2)检验方法大致整平,水准管平行于一对脚螺旋的连线,整平,转180°,气泡偏一格以上,需校正(3)校正方法校正螺丝校一半,脚螺旋改一半。
2.十字丝竖丝的检校(1)检校目的:竖丝^HH(2)检验方法瞄准一固定点,转动望远镜,若该点始终沿竖丝移动,说明条件满足(3)校正方法:慢慢转动十字丝分划板座
3.视准轴的检校(1)检校目的: C C ^ H H(2)检验方法:二分之一法(盘左盘右读数法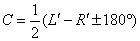 。对于DJ6经纬仪,如果C> 60″,则需要校正(3)校正方法
。对于DJ6经纬仪,如果C> 60″,则需要校正(3)校正方法
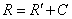 拨左右两校正螺丝,直至影象与十字丝交点重合
拨左右两校正螺丝,直至影象与十字丝交点重合
4.横轴检校(1)检校目的: H H ^ V V(2)检验方法:盘左瞄准墙上高处P点,放平望远镜在墙上定A,盘右瞄准P点,放平望远镜在墙上定B,同时测P点竖直角a,量AB距离,计算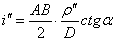 ,i">20" ,需校正(3)校正方法:瞄准AB中点M ,抬高望远镜,拨支架上的偏心轴承,使十字丝交点对准P点。
,i">20" ,需校正(3)校正方法:瞄准AB中点M ,抬高望远镜,拨支架上的偏心轴承,使十字丝交点对准P点。
5.竖盘指标差的检验(1)检校目的:竖盘指标指在正确位置。(2)检验方法
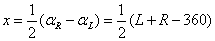
仪器误差:1.CC不^HH横轴(视准轴误差)盘左、盘右观测取平均值
2.HH不^VV(横轴误差)盘左、盘右观测取平均值
3.水平度盘的偏心差:盘左、盘右观测取平均值
4.水平度盘刻划不均匀误差:多测回观测,按180º/ n变换水平度盘位置
5.仪器竖轴倾斜误差:无法用一定的观测方法消除。使用之前应严格检校仪器竖轴与水准管轴的垂直关系
观测误差:1仪器对中误差2.目标偏心误差
距离:两点间的水平长度(钢尺量距:定线 量距 成果计算,视距测量,光电测距)
在两点的连线上标定出若干个点,这项工作称为直线定线(目估定线,经纬仪定线)
普通视距测量的相对精度1/200至1/300
视线倾斜时水平距离的计算公式为: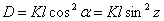
视线倾斜时高差的计算公式为:

测量误差的来源:仪器:观测者;外界环境
观测条件相同称等精度观测 测量误差的分类:系统误差,偶然误差
定义:在相同观测条件下,对某量进行一系列观测,如果误差出现的符号和大小均相同,或按一定的规律变化,这种误差称为系统误差。
特性:累积性。 消除或削减措施:(1)进行计算改正 (2)选择适当的观测方法
在相同的观测条件下,对某量进行一系列的观测,如果观测误差的符号和大小都不一致,表面上没有任何规律性,这种误差称为偶然误差
偶然误差的统计特性:(1)在一定的观测条件下,偶然误差的绝对值有一定的限值(范围)(2)绝对值较小的误差比绝对值较大的误差出现的概率大(大小)(3)绝对值相等的正、负误差出现的概率相同(符号)(4)同一量的等精度观测,其偶然误差的算术平均值,随观测次数n的无限增加而趋于零(抵偿性)即偶然误差的数学期望等于零
测量中可用s作为衡量精度指标的一个标准
目的:求观测值的最可靠值,并衡量其精度;指导实际。
精度:指误差分布的密集或离散的程度,即离散度的大小。
衡量精度的指标:能够反映误差离散度大小的数字
在测量工作中,常采用以下几种标准评定精度。中误差,相对中误差,极限误差
中误差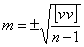 Z = F(x1,x2,...,xn)
Z = F(x1,x2,...,xn)
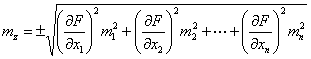
算术平均值的中误差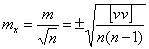

确定直线与标准方向之间的水平角度,称为直线定向
标准方向1.真子午线方向:过地球表面某点的真子午线的切线方向,称该点的真子午线方向。
2.磁子午线方向: 是在地球磁场作用下,磁针在某点自由静止时其轴线所指的方向
3.坐标纵轴方向:在高斯平面直角坐标系中,坐标纵轴线方向就是地面点所在投影带的中央子午线方向。
表示直线方向的方法:方位角:从直线起点的标准方向北端起,顺时针方向量至该直线的水平夹角。取值范围:0?~360?。
ON为真子午线方向——真方位角A ;ON为磁子午线方向——磁方位角Am
ON为坐标纵轴方向——坐标方位角a
正、反坐标方位角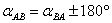
坐标方位角的推算
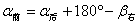
某直线与x轴北南方向所夹的锐角(0?~90?),再冠以象限符号,称为该直线的象限角R。
将测区内相邻控制点用直线连接而构成的折线图形,称为导线。
构成导线的控制点,称为导线点。
依次测定各导线边的长度和各转折角,根据起算数据,推算出各边的坐标方位角,从而求出各导线点的坐标,称为导线测量。
导线的布设形式1.闭合导线2.附和导线3.支导线
导线测量的外业工作1.踏勘选点2.建立标志3.导线边长测量4.转折角测量5连接测量
地形:地物和地貌。 地球表面的高低起伏状态称为地貌。
地面上有明显轮廓的,天然形成或人工建造的各种固定物体称为地物。
地形图:按一定的比例尺,用规定的符号表示地物、地貌平面位置和高程的正射投影图。
地形图上任一线段的长度与它所代表的实地水平距离之比,称为地形图比例尺。
比例尺表示方法:数字比例尺,图示比例尺
地形图上0.1mm的长度所代表的实地水平距离,称为比例尺精度,用ε表示即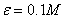
比例尺越大,精度越高
用途:(1) 确定测图时的量距精度(2)可确定测图的比例尺。
? 梯形分幅(国际分幅):按经纬线。矩形分幅:按坐标格网
? 编号:图幅西南角坐标公里数编号x—y
地形图的图框外注记1、地形图的图名2、图号3、图廓和接合图表
地形图上表示地物类别、形状、大小及位置的符号称为地物符号。 (比例符号,非比例符号,半比例符号,地物注记)
地貌符号—等高线(地面上高程相同的相邻各点连成的闭合曲线,称为等高线。)
相邻等高线之间的高差称为等高距,也称为等高线间隔,用h表示。越小地貌越详细
相邻等高线之间的水平距离称为等高线平距,用d表示平距越小,坡度越大
等高线的分类:首曲线,计曲线,间曲线,助曲线
等高线的特性(1)同一条等高线上各点的高程相同 (等高性) (2)等高线必定是闭合曲线。如不在本图幅内闭合,则必在相邻的图幅内闭合(闭合性) (3)除在悬崖、陡崖处外,不同高程的等高线不能相交 (非交性 )(4)等高线平距小,表示坡度陡,平距大表示坡度缓,平距相等则坡度相等 (疏密性)(5)山脊、山谷的等高线与山脊线、山谷线正交。(正交性)
在地形图测绘中,决定地物、地貌位置的特征点称为地形特征点,也称碎部点。
经纬仪测绘法:安置仪器,定向,立尺,观测,记录,计算,展绘碎部点
一、在图上确定某点的坐标二、在图上确定两点间的水平距离三、在图上确定某一直线的坐标方位角四、在图上确定任意一点的高程五、在图上确定某一直线的坡度
已知水平距离的测设:根据给定的起点、直线的方向和两点间的水平距离,将另一端点在地面上标定出来。
用钢尺直接丈量两次,相对误差在1/3000~1/5000内取平均。
已知水平角的测设:根据已知水平角和一个已知方向,将另一方向在地面上标定出来
已知高程的测设:已知高程的测设,是利用水准测量的方法,根据已知水准点,将设计高程测设到现场作业面上
点的平面位置的测设方法:直角坐标法,极坐标法,角度交会法,距离交会法
