高中化学必修一总结
第一章 从实验到化学
一化学实验基本方法
1 粗盐的提纯
1提纯粗盐的步骤:溶解、过滤、蒸发
2过滤 用于固液混合的分离 一贴、二低、三靠 (一贴:指滤纸要紧贴漏斗壁。二低:一是滤纸的边缘要稍低于漏斗的边缘,二是在整个过滤过程中还要始终注意到滤液的液面要低于滤纸的边缘。三靠:一是待过滤的液体倒入漏斗中时,盛有待过滤液体的烧杯的烧杯嘴要靠在倾斜的玻璃棒上(玻璃棒引流),二是指玻璃棒下端要靠在三层滤纸一边,三是指漏斗的颈部要紧靠接收滤液的接受器的内壁


3离子检验
Cl- AgNO3、稀HNO3 产生白色沉淀 Cl-+Ag+=AgCl↓
SO42- 稀HCl、BaCl2 白色沉淀 SO42-+Ba2+=BaSO4↓
4蒸发和结晶 用来分离和提纯几种可溶性固体的混合物 加热蒸发皿使溶液蒸发时,要用玻璃棒不断搅动溶液;当蒸发皿中出现较多的固体时,即停止加热 分离NaCl和KNO3混合物
2蒸馏、萃取、分液
1蒸馏:提纯或分离沸点不同的液体混合物(蒸馏水的制取)。
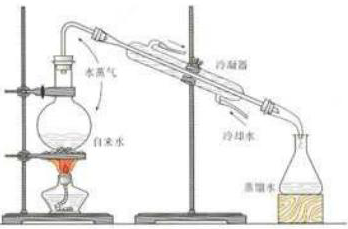

2萃取 利用溶质在互不相溶的溶剂里的溶解度不同,用一种溶剂把溶质从它与另一种溶剂所组成的溶液中提取出来的方法 选择的萃取剂应符合下列要求:和原溶液中的溶剂互不相溶;对溶质的溶解度要远大于原溶剂 用四氯化碳萃取溴水里的溴、碘
3分液:分离互不相溶的液体 如用四氯化碳萃取溴水里的溴、碘后再分液
二化学计量在实验中的应用
1物质的量的单位——摩尔
1阿伏加德罗常数:12g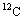 原子所含的碳原子数,实验测得值为6.02×1023mol-1,符号为
原子所含的碳原子数,实验测得值为6.02×1023mol-1,符号为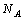 .
.
2摩尔(mol): 把含有6.02 ×1023个粒子的任何粒子集体计量为1摩尔。
31mol任何物质中都含有相同数目的粒子;1mol不同物质的质量是不同的
4.摩尔质量(M)(1) 定义:单位物质的量的物质所具有的质量叫摩尔质量.(2)单位:g/mol 或 g..mol-1(3) 数值:等于该粒子的相对原子质量或相对分子质量. 物质的量=物质的质量/摩尔质量 ( n = m/M )
2气体摩尔体积
1气体摩尔体积(Vm)(1)定义:单位物质的量的气体所占的体积叫做气体摩尔体积.(2)单位:L/mol
2物质的量=气体的体积/气体摩尔体积n=V/Vm
3标准状况下(0℃和101.325kPa), Vm = 22.4 L/mol
3物质的量浓度.
1定义:以单位体积溶液里所含溶质B的物质的量来表示溶液组成的物理量,叫做溶质B的物质的浓度。(2)单位:mol/L(3)物质的量浓度 = 溶质的物质的量/溶液的体积 CB = nB/V
2 配置一定量浓度的物质
a.检验是否漏水.b.配制溶液 1计算.2称量.3溶解.4转移.5洗涤.6定容.7摇匀8贮存溶液.
注意事项:A 选用与欲配制溶液体积相同的容量瓶. B 使用前必须检查是否漏水. C 不能在容量瓶内直接溶解. D 溶解完的溶液等冷却至室温时再转移. E 定容时,当液面离刻度线1—2cm时改用滴管,以平视法观察加水至液面最低处与刻度相切为止.
第二章 化学物质及其变化
一物质的分类
1
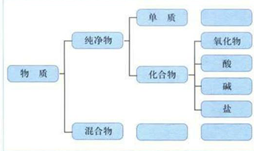
2 把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系,叫分散系。被分散的物质称作分散质(可以是气体、液体、固体),起容纳分散质作用的物质称作分散剂(可以是气体、液体、固体)。
溶液、胶体、浊液三种分散系的比较
分散质粒子大小/nm 外观特征 能否通过滤纸 有否丁达尔效应 实例
溶液 小于1 均匀、透明、稳定 能 没有 NaCl、蔗糖溶液
胶体在1—100间 均匀、有的透明、较稳定 能 有 Fe(OH)3胶体
浊液 大于100 不均匀、不透明、不稳定 不能 没有 泥水
二离子反应
1 电解质:在水溶液中或熔化状态下能导电的化合物,叫电解质。酸、碱、盐都是电解质。在水溶液中或熔化状态下都不能导电的化合物,叫非电解质。
注意:①电解质、非电解质都是化合物,不同之处是在水溶液中或融化状态下能否导电。②电解质的导电是有条件的:电解质必须在水溶液中或熔化状态下才能导电。③能导电的物质并不全部是电解质:如铜、铝、石墨等。④非金属氧化物(SO2、SO3、CO2)、大部分的有机物为非电解质。
2 离子方程式:用实际参加反应的离子符号来表示反应的式子。它不仅表示一个具体的化学反应,而且表示同一类型的离子反应。
复分解反应这类离子反应发生的条件是:生成沉淀、气体或水。书写方法:
写:写出反应的化学方程式
拆:把易溶于水、易电离的物质拆写成离子形式
删:将不参加反应的离子从方程式两端删去
查:查方程式两端原子个数和电荷数是否相等
3 离子共存
⑴生成难溶物或微溶物:Ca2+与CO32-、SO42-、OH-,Ag+与Cl-、Br-、I-等.
⑵生成气体或挥发性物质:H+和CO32-、HCO3-,NH4+与OH-等.
⑶生成难电离物质: H+离子与弱酸根离子:F-、ClO-、S2-、HS-、、SO32-、HCO3-、CO32-、PO43-、 HPO42-等不共存,OH-离子与弱碱的离子:NH4+、Mg2+、Al3+、Fe3+、Fe2+等.
⑷发生氧化还原反应:具有较强氧化性的离子(如MnO4-、ClO-、NO3-、Fe3+等)与具有较强还原性的离子(如I-、S2-、Fe2+、SO32-等)不能共存.
注意:有些离子在通常情况下可共存,但在某些特殊情况下不共存.如NO3-与I-、S2-与SO32-、ClO-与Cl- 等离子,在碱性或中性溶液中可共存,但在酸性条件下不共存.
⑸形成配位化合物:如Fe3+与SCN-离子因反应生成[Fe(SNH)]2+离子而不可共存.
⑹弱酸的酸根与弱碱的阳离子因易发生双水解反应而不共存.如Al3+与HCO3-、Fe3+与PO43-等不共存.
注意:①阴离子与阴离子之间也不能共存,如HCO3-与OH-.
②无色溶液不存在MnO4-、Fe3+、Fe2+、Cu2+.
三氧化还原反应
1 、氧化还原反应:反应中有电子转移(得失或偏移)的反应
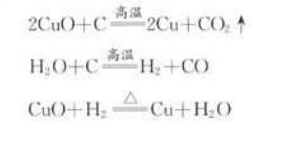
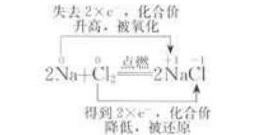
2氧化还原反应中概念及其相互关系如下:
失去电子——化合价升高——被氧化(发生氧化反应)——是还原剂(有还原性)
得到电子——化合价降低——被还原(发生还原反应)——是氧化剂(有氧化性)
第三章 金属及其化合物
一金属的化合性质
1金属活动性Na>Mg>Al>Fe,,特别活泼的如Na等可以与H2O发生反应置换出H2,特殊金属如Al可以与碱溶液反应而得到H2。
2钠
1钠在空气中的缓慢氧化过程及现象:切开金属钠,呈银白色(钠的真面目)→变暗(生成Na2O)→变白色固体(生成NaOH)→成液(NaOH潮解)→结块(吸收CO2成NaCO3﹒10H2O)→最后粉末(变为Na2CO3风化)
2钠与水(加酚酞)反应有四个现象:浮在水上(比水轻);熔化成闪亮的小球,发出嘶响(反应放热,钠熔点低);迅速游动(产生氢气);溶液呈红色(生成NaOH遇酚酞变红).
注意:①Na的制法:2NaCl(熔触) 2Na+Cl2↑
②Na2O2与H2O反应,Na2O2既是氧化剂,也是还原剂.
3 铝与酸碱的反应
a、与非金属: 2Al+3S==Al2S3,2Al+3Cl2==2AlCl3
b、与酸:2Al+6HCl==2AlCl3+3H2↑
常温常压下,铝遇浓硫酸或浓硝酸会发生钝化,所以可用铝制容器盛装浓硫酸或浓硝酸
c、与强碱:2Al+2NaOH+2H2O==2NaAlO2(偏铝酸钠)+3H2↑ (2Al+2OH-+2H2O==2AlO2-+3H2↑)
4 铁
①物理性质:银白色光泽,密度大,熔沸点高,延展性,导电导热性较好,能被磁铁吸引。铁在地壳中的含量仅次于氧、硅、铝,排第四。
②化学性质:
a、与非金属:Fe+S==FeS,3Fe+2O2===Fe3O4,2Fe+3Cl2===2FeCl3
b、与水:3Fe+4H2O(g)===Fe3O4+4H2
c、与酸(非氧化性酸):Fe+2H+==Fe2++H2 与氧化性酸,如硝酸、浓硫酸,会被氧化成三价铁
d、与盐:如CuCl2、CuSO4等,Fe+Cu2+==Fe2++Cu
二几种重要的金属化合物
1 钠的化合物
1过氧化钠

2Na2CO3(纯碱或苏打 )和NaHCO3(小苏打)比较
俗名 纯碱或苏打 小苏打
色态 白色晶体 细小白色晶体
水溶性 易溶于水,溶液呈碱性使酚酞变红 易溶于水 溶液呈碱性(酚酞变浅红)
热稳定性 较稳定,受热难分解 受热易分解
相同条件下放出CO2的速度NaHCO3比Na2CO3快
3关于焰色反应:
⑴焰色反应采用煤气灯较理想,若用酒精灯焰,则要使用外焰的侧面(因为焰心的颜色偏黄).
⑵蘸取待测物的金属丝,最好用铂丝,也可用铁丝,钨丝代替,每次使用金属丝时,必须在火焰上烧至无色,以免对实验现象造成干扰.
⑶金属丝在使用前要用稀盐酸将其表面物质洗净,然后在火焰上烧至无色,这是因为金属氯化物灼烧时易气化而挥发,若用硫酸洗涤金属丝,由于硫酸盐熔沸点高而难以挥发,故不用硫酸.
⑷观察钾的焰色反应时,要透过蓝色钴玻璃,因为钾中常混有钠的杂质,蓝色钴玻璃可以滤去黄光.
2铝的化合物
1氧化铝
难溶于水 易溶于酸 碱
Al2O3(典型的两性氧化物)
a、与酸:Al2O3+6H+==2Al3++3H2O b、与碱:Al2O3+2OH-==2AlO2-+H2O
2制取氢氧化铝
Al(OH)3(典型的两性氢氧化物):白色不溶于水的胶状物质,具有吸附作用
a、实验室制备:AlCl3+3NH3?H2O==Al(OH)3↓+3NH4Cl,Al3++3NH3?H2O==Al(OH)3↓+3NH4+
b、与酸、碱反应:与酸 Al(OH)3+3H+==Al3++3H2O 与碱 Al(OH)3+OH-==AlO2-+2H2O
3 KAl(SO4)2(硫酸铝钾)
KAl(SO4)2?12H2O,十二水和硫酸铝钾,俗名:明矾
KAl(SO4)2==K++Al3++2SO42-,Al3+会水解:Al3++3H2O =Al(OH)3+3H+
因为Al(OH)3具有很强的吸附型,所以明矾可以做净水剂
3 铁的氧化物
1铁红、铁矿:Fe2O3 (红棕色粉末) 磁铁矿:Fe3O4 (磁性黑色晶体) FeO (黑色粉末)
2 Fe2+和Fe3+离子的检验:
①溶液是浅绿色的
Fe2+ ②与KSCN溶液作用不显红色,再滴氯水则变红
③加NaOH溶液现象:白色 灰绿色 红褐色
①与无色KSCN溶液作用显红色
Fe3+ ②溶液显黄色或棕黄色
③加入NaOH溶液产生红褐色沉淀
三用途广泛的金属材料
1 合金:两种或两种以上的金属(或金属与非金属)熔合在一起而形成的具有金属特性的物质。
合金的特点;硬度一般比成分金属大而熔点比成分金属低,用途比纯金属要广泛。
2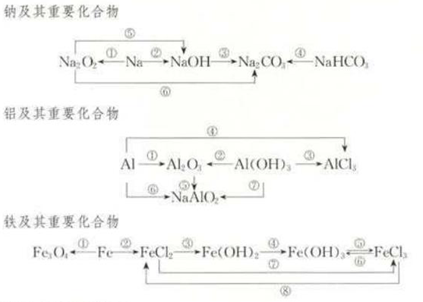
第四章 非金属及化合物
一无机非金属材料的主角-硅
1 地壳中的元素的含量大小依次为:氧、硅、氯、铁。“养闺女贴锅盖,哪家没青菜”
2 二氧化硅(SiO2)
天然存在的二氧化硅称为硅石,包括结晶形和无定形。(玛瑙饰物,石英坩埚,光导纤维)
物理:熔点高、硬度大、不溶于水、洁净的SiO2无色透光性好
化学:化学稳定性好、除HF外一般不与其他酸反应,可以与强碱(NaOH)反应,是酸性氧化物,在一定的条件下能与碱性氧化物反应
SiO2+4HF == SiF4 ↑+2H2O
SiO2+CaO ===(高温) CaSiO3
SiO2+2NaOH == Na2SiO3+H2O
不能用玻璃瓶装HF,装碱性溶液的试剂瓶应用木塞或胶塞。
3硅酸(H2SiO3)
酸性很弱(弱于碳酸)溶解度很小,由于SiO2不溶于水,硅酸应用可溶性硅酸盐和其他酸性比硅酸强的酸反应制得。
Na2SiO3+2HCl == H2SiO3↓+2NaCl
4硅酸盐是由硅、氧、金属元素组成的化合物的总称,分布广,结构复杂化学性质稳定。一般不溶于水。(Na2SiO3 、K2SiO3除外)最典型的代表是硅酸钠Na2SiO3 :可溶,其水溶液称作水玻璃和泡花碱,可作肥皂填料、木材防火剂和黏胶剂。 常用硅酸盐产品:玻璃、陶瓷、水泥
太阳能电池、计算机芯片用到硅单质
二富集在海水中的元素-氯
1 氯气
物理性质:黄绿色气体,有刺激性气味、可溶于水。
制法:MnO2+4HCl (浓) MnCl2+2H2O+Cl2
闻法:用手在瓶口轻轻扇动,使少量氯气进入鼻孔。
化学性质:很活泼,有毒,有氧化性, 能与大多数金属化合生成金属氯化物(盐)。也能与非金属反应:
2Na+Cl2 ===(点燃) 2NaCl 2Fe+3Cl2===(点燃) 2FeCl3 Cu+Cl2===(点燃) CuCl2
Cl2+H2 ===(点燃) 2HCl 现象:发出苍白色火焰,生成大量白雾。
燃烧不一定有氧气参加,物质并不是只有在氧气中才可以燃烧。燃烧的本质是剧烈的氧化还原反应,所有发光放热的剧烈化学反应都称为燃烧。
2 氯气的用途
①自来水杀菌消毒Cl2+H2O == HCl+HClO 2HClO ===(光照) 2HCl+O2 ↑
1体积的水溶解2体积的氯气形成的溶液为氯水,为浅黄绿色。其中次氯酸HClO有强氧化性和漂泊性,起主要的消毒漂白作用。次氯酸有弱酸性,不稳定,光照或加热分解,因此久置氯水会失效。
②制漂白液、漂白粉和漂粉精
制漂白液 Cl2+2NaOH=NaCl+NaClO+H2O ,其有效成分NaClO比HClO稳定多,可长期存放制漂白粉(有效氯35%)和漂粉精(充分反应有效氯70%) 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
3氯离子的检验
使用硝酸银溶液,并用稀硝酸排除干扰离子(CO32-、SO32-)
HCl+AgNO3 == AgCl ↓+HNO3
NaCl+AgNO3 == AgCl ↓+NaNO3
Na2CO3+2AgNO3 ==Ag2CO?3 ↓+2NaNO3
Ag2CO3+2HNO3 == 2AgNO3+CO2 ↑+H2O
Cl-+Ag+ == AgCl ↓
三硫和氮的氧化物
1二氧化硫
制法(形成):硫黄或含硫的燃料燃烧得到(硫俗称硫磺,是黄色粉末)
S+O2 ===(点燃) SO2
物理性质:无色、刺激性气味、容易液化,易溶于水(1:40体积比)
化学性质:有毒,溶于水与水反应生成亚硫酸H2SO3,形成的溶液酸性,有漂白作用,遇热会变回原来颜色。这是因为H2SO3不稳定,会分解回水和SO2
SO2+H2O --H2SO3 因此这个化合和分解的过程可以同时进行,为可逆反应。
2 一氧化氮和二氧化氮
一氧化氮在自然界形成条件为高温或放电:N2+O2 ========(高温或放电) 2NO,生成的一氧化氮很不稳定,在常温下遇氧气即化合生成二氧化氮: 2NO+O2 == 2NO2
一氧化氮的介绍:无色气体,是空气中的污染物,不溶于水。
二氧化氮的介绍:红棕色气体、刺激性气味、有毒、易液化、易溶于水,并与水反应:
3NO2+H2O == 2HNO3+NO 这是工业制硝酸的方法。
3 大气污染
SO2 、NO2溶于雨水形成酸雨。防治措施:
① 从燃料燃烧入手。
② 从立法管理入手。
③从能源利用和开发入手。
④从废气回收利用,化害为利入手。
(2SO2+O2 2SO3 SO3+H2O= H2SO4)
四氨硝酸硫酸
1 氨气及铵盐
氨气的性质:无色气体,刺激性气味、密度小于空气、极易溶于水(且快)1:700体积比。溶于水发生以下反应使水溶液呈碱性:NH3+H2O NH3?H2O NH4++OH- 可作红色喷泉实验。生成的一水合氨NH3?H2O是一种弱碱,很不稳定,会分解,受热更不稳定:NH3。H2O ===(△) NH3 ↑+H2O
浓氨水易挥发除氨气,有刺激难闻的气味。
氨气能跟酸反应生成铵盐:NH3+HCl == NH4Cl (晶体)
铵盐的性质:易溶于水(很多化肥都是铵盐),受热易分解,放出氨气:
NH4Cl =NH3 ↑+HCl ↑
NH4HCO3 =NH3 ↑+H2O ↑+CO2 ↑
可以用于实验室制取氨气:(干燥铵盐与和碱固体混合加热)
NH4NO3+NaOH =Na NO3+H2O+NH3 ↑
2NH4Cl+Ca(OH)2 CaCl2+2H2O+2NH3 ↑ 用向下排空气法收集,湿润的红色石蕊试纸检验是否收集满。
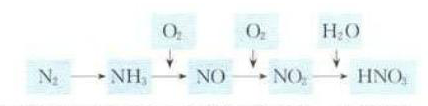
2硫酸
物理性质:无色粘稠油状液体,不挥发,沸点高,密度比水大。
化学性质:具有酸的通性,浓硫酸具有脱水性、吸水性和强氧化性。是强氧化剂。
C12H22O11 ======(浓H2SO4) 12C+11H2O放热
2 H2SO4 (浓)+C CO2 ↑+2H2O+SO2 ↑
还能氧化排在氢后面的金属,但不放出氢气。
2 H2SO4 (浓)+Cu CuSO4+2H2O+SO2 ↑
稀硫酸:与活泼金属反应放出H2 ,使酸碱指示剂紫色石蕊变红,与某些盐反应,与碱性氧化物反应,与碱中和
3 硝酸
物理性质:无色液体,易挥发,沸点较低,密度比水大。
化学性质:具有一般酸的通性,浓硝酸和稀硝酸都是强氧化剂。还能氧化排在氢后面的金属,但不放出氢气。
4HNO3(浓)+Cu == Cu(NO3)2+2NO2 ↑+4H2O
8HNO3(稀)+3Cu 3Cu(NO3)2+2NO ↑+4H2O
反应条件不同,硝酸被还原得到的产物不同,可以有以下产物:N(+4)O2,HN(+3)O2,N(+2)O,N(+1)2O,N(0)2, N(-3)H3△硫酸和硝酸:浓硫酸和浓硝酸都能钝化某些金属(如铁和铝)使表面生成一层致密的氧化保护膜,隔绝内层金属与酸,阻止反应进一步发生。因此,铁铝容器可以盛装冷的浓硫酸和浓硝酸。
