金属钠的性质及应用
——珠江“水雷”探秘
金坛市直溪高级中学 执教者:陈菊平
学习目标:
1、了解金属钠的主要物理性质;
2、了解金属钠与氧气、水等反应的化学性质;
3、通过对金属钠化学性质的实验探究,增强化学学习的兴趣,发展科学探究能力。
【新闻资料】
20xx年7月7日,在珠江石溪附近,前前后后共飘着七个白色的来历不明的金属桶。突然,从飘在水面上的一个金属桶内冒起一股白烟,窜起亮黄色火苗,紧接着一声巨响,蘑菇状的水柱冲天而起,这个铁桶接着又连续爆炸了多次,爆炸腾起的白色烟雾有近十米高,还有许多未燃尽的白烟飘进旁边的公司内,这些灰白色的物体一遇到水就不停地冒泡,有时甚至还突然着火。
据悉,其中另有一铁桶被过往船只发现,并将其打捞上船,打算清洗后使用,但当船员把盖子打开后,桶内冒起浓浓白烟,一接触桶内物质,双手立即感到剧烈地疼痛,于是他们又将其推入江里,一遇水,这个桶就又爆炸了。所幸该船只迅速逃离,伤亡不大。
珠江水面上尚有五个一触即发的“水雷”漂浮着,消防队员、民警及广州化工集团的化学品专家赶来凑在一起,紧张地调查爆炸物的性质及研究“水雷”的处置对策。
铁桶中究竟装有什么神秘物质???
【学生探究实验】金属钠与水的反应
1.用小刀切割金属钠,观察切面颜色、光泽。
2.在250ml烧杯中加入60ml水并向其中滴加3、4滴酚酞试剂,然后取一小粒(绿豆粒大小)金属钠,投入其中,请注意观察实验现象并完成实验报告。 1
交流讨论:
1.金属钠为什么要保存在煤油中?
2.金属钠露置在空气中,表面为什么会迅速变暗? ..
3.金属钠长期暴露在空气中,最终将会变成什么物质?
4.你能设计一个简单的实验来检验产生的气体是H2吗?
5.通过实验,我们能知道金属钠有哪些主要的物理性质和化学性质?
常温下金属钠与氧气反应生成氧化钠,如果在加热或点燃的条件下与氧气反应是否同样生成氧化钠呢? 【探究实验2】金属钠与氧气在加热或点燃条件下的反应
将一小块金属钠放在石棉网上加热,并将产物投入到水中,请注意观察实验现象。
2
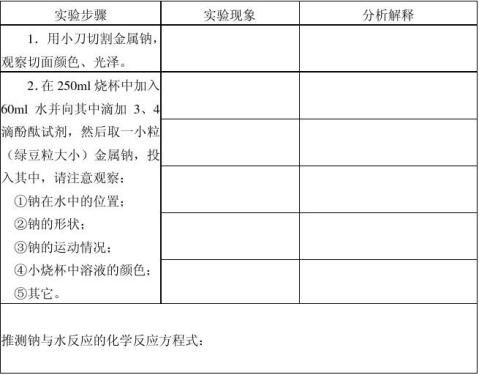
交流讨论:
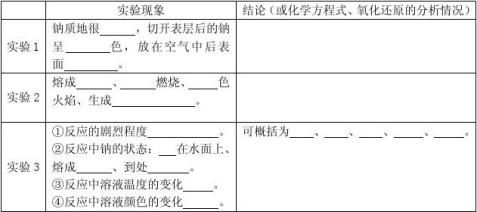
1.金属钠在空气中燃烧的实验现象。
2.写出Na2O与水反应的化学方程式。
3.根据Na2O与水反应的化学方程式和上述产物与水反应的现象,判断产物是否仍为Na2O?
4.写出金属钠与氧气在加热或点燃条件下反应的化学方程式,并指出氧化剂、还原剂,判断氧在生成物中的化合价。 .
金属钠能在不同条件下与氧气反应,虽然得到不同的产物,但是金属钠在反应中同样失去电子,表现出很强的还原性。
【思考】
1.钠作为活泼金属,能否和其它的非金属单质发生反应?
2.钠作为金属,推测一下,钠还能和哪些物质发生反应?
【小结归纳】
金属钠的金属活动性很强,常作还原剂,具有强还原性!!!
【珠江“水雷”解谜】
通过我们自己的分析归纳,已经了解了钠的基本性质。那么现在你能不能解释珠江“水雷”之谜了呢?
1.为什么“水里的东西也能着火爆炸”?
2.还有5个金属桶在水中,该怎么处理?假如你是现场指挥,你怎么做?
【阅读课本】
结合金属钠的性质,讨论归纳金属钠的存在、制备和用途。
【课堂小结】
通过这堂课的学习,你有哪些收获,学到了什么?
【作业布置】
3
1.通过你的观察和推理,判断下列实验室中对于少量Na的保存方法正确的是( )
A.保存在水中 B.密封,保存在广口瓶中
C.用铝箔包裹,密封在广口瓶中 D.密封,保存在煤油中
2.钠与水反应的现象与钠的下列性质无关的是( )
A.钠的熔点较低 B.钠的密度比水的小
C.钠的硬度小 D.钠有很强的还原性
3.下列有关钠的叙述中,错误的是( )
A.钠的化学性质很活泼,可以用来冶炼金属钛、锆、铌等
B.钠的化学性质非常活泼,钠元素只能以化合态存在于自然界
C.钠是一种灰黑色的固体
D.钠的质地软,可用小刀切割
4.取一小块钠放在玻璃燃烧匙里加热,下列实验现象正确的是( ) ①金属先熔化 ②在空气中燃烧火焰呈黄色 ③燃烧时火星四射 ④燃烧后生成淡黄色固体 ⑤燃烧后生成白色固体
A.①②③ B.①②④ C.①②⑤ D.①③⑤
5.将一小块钠投入盛有5mL饱和石灰水的试管中,不可能观察到的现象是( )
A.钠熔成光亮的小球,在液面四处游动 B.有气体产生
C.溶液底部有银白色的物质 D.溶液变浑浊
6.将一小块金属钠投入到FeCl3溶液中,此时观察到的现象是___________,有关化学反应方程式是_____________________________。
7.在烧杯中加入水和苯(密度:0.88g/cm3)各50mL将一小粒金属钠(密度:0.97g/cm3)投入烧杯中,可能观察到怎样的现象呢(Na与苯不发生反应)?
8.一块表面已部分氧化的钠质量为0.77g,放入10g水中后,得到氢气的质量是0.02g。求:⑴钠表面的氧化钠的质量是多少?⑵所得溶液的溶质的质量分数是多少?
4
第二篇:金属钠的性质与应用(学案)
2011级高一化学教学案(必修1) 江苏省昆山中学
金属钠的性质与应用
班级 姓名
【学习目标】
1.掌握金属钠的物理性质,理解钠的化学性质。
2.了解钠的存在、用途和贮存方法;了解钠的生产原理。
3.获得实验的基本技能,学习实验研究的方法。
【整理归纳】
一、金属钠的物理性质:
钠是一种 色金属,质 ,密度为 ,比水 ,比煤油 , 熔点较 ,导电,导热。
二、金属钠的化学性质:
钠原子的最外层电子数为 个,是不稳定结构,在反应中易 ,形成钠离子,所以金属钠是化学性质 的金属单质,在反应中是强 剂。
1.钠能与 、 等非金属反应。(写出有关反应、弄清有关物质颜色、分析氧化还原情况)。
2.钠能与水剧烈反应。(写出化学方程式,分析氧化还原情况,弄清反应实质)
【活动探究1】钠与盐酸、硫酸的反应如何?
3.钠与盐酸、硫酸的反应。
1
2011级高一化学教学案(必修1) 江苏省昆山中学
【问题解决1】
1.向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中轻缓地加入绿豆大小的金属钠,可能观察到的现象是 ( )
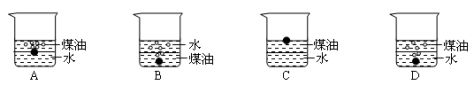
【活动探究2】我国在西汉时期,就掌握了湿法炼铜技术,其原理就是用铁与硫酸铜反应置换出铜。活泼金属能够把不活泼金属从它们的盐溶液中置换出来。如果金属钠与硫酸铜溶液作用结果会如何呢?请你预测,并简要说明理由。
4.钠与盐溶液的反应。
向一只盛有CuSO4的大烧杯中加入一小块金属钠,观察实验现象。
结论:钠加入盐的水溶液,首先和 反应,生成的 再和盐反应。所以钠 能从盐的水溶液中,把比它不活泼的金属置换出来。
5.钠从 盐中置换金属
钠可用于从 等金属氯化物中置换出金属单质。
例如:钠置换出钛,写出方程式: 。
【拓展视眼】Li、Na、K、Rb、Cs,称为碱金属(对应的碱均为强碱),均为活泼的(强还原性)金属单质,单质及化合物性质相似,Li、Na、K、Rb、Cs还原性逐渐增强。
三、钠的存在、制备、保存、用途。
1.存在:钠的化学性质很 ,在自然界中只能以 态存在,如 。
2.钠的制备:工业上现在用的比较多的方法是,电解熔融的氯化钠: 。
3.在实验室里金属钠是保存在 中。
【活动探究3】
在实验室里金属钠是保存在煤油中的,请同学们想一想:
(1)金属钠为什么可以保存在煤油中? (2)金属钠为什么要保存在煤油中?
(3)取用钠时,为什么要用镊子,不能用手?
(4)取用钠时,多余的钠能不能放回煤油中?
【交流讨论】4.钠的用途
(1)制取钠的化合物: 。
(2)中子反应堆作热交换剂:钠、钾合金在常温下为 ,有很好的导热性。
(3)高压钠灯:黄光射程远,透雾能力强
(4)冶炼某些贵金属:钠有很强的 性。
【问题解决2】1.钠着火时,应如何扑灭?( )
A.用水扑灭 B.用泡沫灭火器 C.撒上沙子.
2.钠暴露在空气中最终会转化成什么?为什么?
2
2011级高一化学教学案(必修1) 江苏省昆山中学
【巩固练习】 班级 姓名
1.钠与水反应的现象和钠的下列性质无关的是 ( )
A.钠的熔点低 B.钠的密度小 C.钠的硬度小 D.钠的强还原性
2.2.3g金属钠溶于97.7g水中所得溶液的溶质质量分数是 ( )
A.2.3% B.4% C.略小于4% D.略大于4%
3.将一小块钠投入盛饱和澄清石灰水的试管里,不可能观察到的现象是 ( )
A.熔成小球并在液面上游动 B.有气体生成
C.溶液底部有银白色物质生成 D.溶液变浑浊
4.NaH与水反应的化学方程式为NaH+H2O==NaOH+H2 ↑,在该反应中的水是 ( )
A.是氧化剂 B.是还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
5.少量的金属钠长期放置在空气中,最终的产物是 ( )
A.Na2CO3 B.NaOH C.Na2O D.NaHCO3
6.下列叙述中不正确的是 ( )
A.钠原子有强还原性,钠离子有弱氧化性
B.若电解熔融的氯化钠,则钠离子被氧化成了钠原子
C.由于钠很活泼,所以它能从溶液中置换金属活动顺序中钠后面的金属
D.钠是电和热的良导体
7.将等质量的钠分别投入质量和质量分数均为100g和9.8%的HCl,H2SO4,H3PO4溶液中, 金属钠完全参加了反应。则生成的氢气在标准状况下的体积比是 ( )
A.1∶2∶3 B.3∶2∶1 C.1∶1∶1 D.无法计算
8.有关钠的叙述中正确的是 ( )
A.可以把钠保存在煤油或四氯化碳里
B.大量钠着火时,可以用水浇灭
C.钠是一种很活泼的金属,原因是其原子最外层只有一个电子,在化学反应中易失去
D.不能用手直接拿金属钠
339.在烧杯中加水和苯(密度为0.88g/cm)各50mL。将一小粒金属钠(密度为0.97 g/cm)
投入烧杯中,观察到的现象可能是 ( )
A.钠在水层中反应并四处游动 B.钠停留在苯层中不发生反应
C.钠在苯的液面上反应并四处游动 D.钠在苯与水的界面处反应并可能作上下跳动
10.钠的下列用途与其化学性质无关的是 ( )
A.制过氧化钠 B.原子反应堆的导热剂
C.冶炼金属钛 D.制取贵重金属钽
11.已知钡的金属活动性介于钠和钾之间,则下列推论中可能成立的是 ( )
A.钡与水反应较钠与水反应剧烈,但较钾弱
B.钡与水反应较钾与水反应剧烈,但较钠弱
C.钡可以从KCl溶液中置换出钾
D.钡可以从NaCl溶液中置换出钠
-112.Na、Mg、Al各0.1mol,分别投入到1mol·L稀盐酸50ml,充分反应后,放出的氢
气 ( ) 3
2011级高一化学教学案(必修1) 江苏省昆山中学
A.钠最多 B.铝最多 C.镁、铝一样多 D.三者一样多
13.将一小块钠投入下列溶液时,既能产生气体又会出现沉淀的是 ( )
A.稀H2SO4 B.氢氧化钠溶液 C.硫酸铜溶液 D.氯化钠溶液
14.下列反应及其叙述中,正确的是 ( )
A.2Na +2H2O == 2NaOH + H2↑水是氧化剂,钠是还原剂
B.Na2O + H2O == 2NaOH 水既是氧化剂又是还原剂
C.Cl2 + H2O HCl + HClO水既不是氧化剂又不是还原剂
D.2NaHCO32CO3 + CO2 ↑+ H2O水既是氧化产物又是还原产物
15.用光洁的铂丝在蘸取了某无色溶液后,在无色火焰上灼烧,直接观察,火焰呈黄色,下列各判断正确的是 ( )
+++A.只含有Na B.一定含有Na,可能有K
++++C.既含有Na,又含有K D.可能有Na,可能有K
16.已知用金属钠生成氧化钠,可有多种方法:
①4Na+O2=2Na2O ②4Na+CO2=2Na2O+C ③NaNO2+3Na=2Na2O+N2↑
在上述三种方法中最好方法是 ,原因是 _________ 。
17.为了测定钠的相对原子质量,设计装置如右图,该装置(包括水、固
体NaOH和仪器)的总质量为ag,将质量为bg(不足量)的钠放到水中,
立即盖好瓶塞,反应后再称量此装置的总质量为cg。
(1)计算金属钠相对原子质量的数学表达式是:______________
(2)固体NaOH作用是_____________________, 如果不用固体NaOH,
测出的相对原子质量比实际的相对原子质量__________(填偏大,偏小或
相等)。
18.有一块表面已经氧化为Na2O的金属钠,质量是10.8g,将它投入到100g水中,产生
0.200g
气体。
求(1)Na2O的质量。
(2)反应后溶液中NaOH
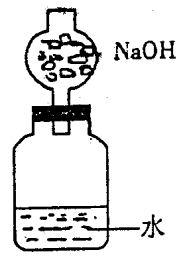
的质量分数。
4
