第一章从实验学化学 第一节 化学实验基本方法
【巩固教材——稳扎马步】
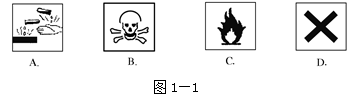 1.对危险化学药品要在包装标签上印上警示性标志。在盛放浓硫酸的试剂瓶的标签上应印有的警示标记是 ( )
1.对危险化学药品要在包装标签上印上警示性标志。在盛放浓硫酸的试剂瓶的标签上应印有的警示标记是 ( )
2.下列操作不属于提纯粗盐所涉及的方法是 ( )
A.蒸发 B.过滤 C.溶解 D.分液
3.实验室常用的玻璃仪器①试管;②烧杯;③量筒;④普通漏斗;⑤分液漏斗;⑥烧瓶;⑦滴管;⑧容量瓶。其中把碘水中的碘提取出来用到的仪器有 ( )
A.②④⑥ B.②⑤ C.③⑤⑥⑧ D.②③④⑥⑦
4.除去NaCl中混有的MgCl2、Na2SO4选用的化学药品是 ( )
A.NaOH和Ba(NO3)2 B.Ca(OH)2和AgNO3 C.NaOH和BaCl2 D.Na2CO3和BaCl2
【重难突破——重拳出击】
1.下列事故处理正确的是 ( )
A. 浓硫酸不慎沾到皮肤上,可立即用大量的水冲洗。
B.眼睛里不慎溅入氢氧化钠溶液,应立即用大量的水中洗,边洗边眨眼睛,最后点硼酸滴眼液。
C.实验中不慎将酸液溅到眼中,应立即用稀碱液冲洗,边洗边眨眼睛。
D.实验中不慎打翻酒精灯,失火时,立即打用大量的水扑灭。
2.人们在生活和生产中,为了防止事故的发生,常需采取一些安全措施或安全限制,下列行为危急安全的是 ( )
A. 学校驻地,车辆限速20千米 B.液化气站、加油站附近焚烧垃圾
C.进入久未开启的地窖或深井时要做灯火实验 D.严禁旅客携带易燃易爆物品上车
3.已知I2在有机溶剂中溶解度比在水中的大,下列有机溶剂能从碘水中萃取I2的是( )
A.酒精 B.四氯化碳 C. 乙酸 D.汽油
4.水资源非常重要,联合国确定20##年为国际淡水年。下列关于水的说法中错误的是( )
A.蒸馏法是海水淡化的方法之一 B.融化的雪水中矿物质的含量比深井中少
C.淡水的密度比海水的密度小 D.0℃以上,温度越高,水的密度越小
5.提纯含有少量硝酸钡杂质的硝酸钾溶液,可以使用的方法为 ( )
A.加入过量碳酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
B.加入过量硫酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
C.加入过量硫酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
D.加入过量碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
6.下列固体,只用水就能区别的是 ( )
A.NaCl、NaOH、NH4NO3、CaCO3 B.FeCl3、CuSO4、Mg(OH)2、NaCl
C.BaSO4、AgCl、KOH、NH4Cl D.NH4HCO3、MgCl2、BaCl2、Ba(NO3)2
7.下有三组混合物:①氯化钠和水;②硫酸钡和水;③煤油和水。分离以上混合液的正确方法依次是 ( )
A.分液、萃取、蒸馏 B.蒸发、过滤、分液
C.分液、蒸发、萃取 D.蒸馏、萃取、分液
8.下列仪器:①漏斗;②蒸馏烧瓶;③坩埚;④分液漏斗;⑤托盘天平;⑥烧杯。常用于物质分离的是 ( )
A.①③⑥ B.①②④ C.①③⑤ D.①③⑤⑥
【巩固提高——登峰揽月】
1.工业酒精是含水约4%的液态乙醇。向工业酒精中加入生石灰,会发生CaO+H2O=Ca(OH)2反应且生成物不溶于乙醇。要在实验室中将工业酒精转化为无水酒精请回答下列问题:
(1)下列做法不可取的是(填代号) 。
A.加入过量的生石灰后过滤 B.加入过量的生石灰后蒸馏 C.加入过量的生石灰后分液
(2)在你选择的需要加热的实验方法中需用的玻璃仪器,除酒精灯以外,还有: ;在该方法的实验步骤里,紧挨加热之前的操作是 。并且对此要注意的问题是 。
(3)实验中保持蒸馏烧瓶支管处温度恒定的方法是 。
2.在实验室中拟用氧化铜、稀硫酸和锌制取纯净的铜,甲、乙两同学分别设计了如下实验方案。
甲:①将CuO溶于适量的稀硫酸中;
②在①的溶液中加入适量的锌,充分反应后,过滤、烘干,即得纯净的铜。
乙:①锌与稀硫酸反应得氢气;
②将氢气通入氧化铜中并加热,充分反应后即得纯净的铜。
问:若要制得相同质量的纯铜,甲乙所耗用的锌和稀硫酸是否相同?为什么?
。
丙同学认为上述两种方案所制得的铜都难以保证铜的纯度,应对上述两种方案加以完善。你是否同意丙同学的看法?为什么?你认为应该怎样完善实验方案?
。
【课外拓展——超越自我】
1.某校学生课外活动小组现欲用下图的仪器和药品制取纯净的一氧化碳(用浓硫酸干燥)并进行还原氧化铜实验(要求实验中不排放有害气体)。图中A---I表示玻璃管接口。
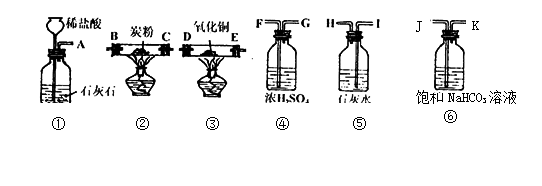
请从实验的科学性和安全性方面考虑,回答下列问题:
(1)装置①中所发生反应的化学方程式是 。
(2)实验装置的连接顺序是(填字母符号) 。
(3)装置④中浓硫酸的作用是 。
(4)实验中证明氢气有还原性的现象是 。
(5)在实验中不排放有害气体应该怎样操作?
。
2.某校化学课外兴趣小组的同学欲测定某品牌味精中食盐的含量。下面是该小组所进行的实验步骤:
①称取某品牌袋装味精样品10.0g放入烧杯中,并加适量蒸馏水溶解;
② ;
③ ;
④用蒸馏水洗涤沉淀2~3次;
⑤将沉淀烘干、称量,测得固体质量4.90g。
根据上述实验步骤回答下列问题:
(1)请你补齐所缺的实验步骤:② ③
(2)实验③所用的玻璃仪器有 ;
(3)检验沉淀是否洗净的方法是 。
(4)若味精商标上标注:“谷氨酸钠含量≥80.0%,NaCl含量≤20.0%”,则此样品是否合格?(填“合格”,“不合格”)。
参考答案第一章 从实验学化学 第一节 化学实验基本方法
【巩固教材——稳扎马步】1.A 2.D 3.B 4.C
【重难突破——重拳出击】B 2.B 3.B、D 4.D 5.D 6.A、B 7.B 8.B(
1. 【巩固提高——登峰揽月】
1.(1)A、C。(2)蒸馏烧瓶、温度计、冷凝管、牛角管、锥形瓶;向冷凝管内通冷却水;使冷却水从下口进,上口出。(3)加热中适时调整酒精灯火焰的位置,可上下左右移动酒精灯。
简析:(1)CaO和Ca(OH)2都是不溶于酒精难挥发的固体,酒精是易挥发的液体。因此可用过滤或蒸馏分离,不用分液。(2)本题用的方法是蒸馏,因此除了酒精灯以外还有蒸馏烧瓶、温度计、冷凝管、牛角管、锥形瓶。在蒸馏的操作中,为了使馏出的蒸气及时冷却,要先向冷凝管内通冷却水,然后加热,冷却水要从下口进,上口出,可提高冷却效果。(3)用酒精灯做热源,温度的升降可通过控制酒精灯火焰的位置来实现。)
2.(1)不相同。因为乙方案中氢气除了还原氧化铜外,还需用来排尽装置中空气和做保护气,所以乙方案耗用的氢气多,所耗用的锌和稀硫酸多。
(2)同意。因为甲方案制得的铜中可能混有锌而且过滤后未洗涤。改进方法是:加入锌充分反应后,再加入足量的稀硫酸,不断搅拌、至不再产生气体为止,静止、过滤、洗涤、烘干。乙方案制得的铜中可能混有氧化铜,改进的方法是:将所得的铜粉中加入足量的稀硫酸,不断搅拌、至不再产生气体为止,静止、过滤、洗涤、烘干。
简析:从理论上讲甲乙两方案所耗用的锌和稀硫酸的量是相同的。但在实际过程中乙方案中氢气除了还原氧化铜外,还需用来排尽装置中空气和做保护气,所以乙方案耗用的氢气多,所耗用的锌和稀硫酸多。甲方案制得的铜中可能混有锌而且过滤后未洗涤,乙方案制得的铜中可能混有氧化铜,因此两方案都是不完善的。应先用稀硫酸将杂质出去。
【课外拓展——超越自我】
1.(1)CaCO3+2HCl=CaCl2+H2O+CO2↑ (2)AJKFGBCDEIH。(3)除去气体中的水蒸气,干燥二氧化碳。(4)装置③中固体变红色。(5)在装置⑤的H管口放一个燃着的酒精灯。
简析:(1)装置①产生CO2,发生反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑。装置的连接顺序是,制取CO2,净化除HCl气体和水蒸气,产生CO,还原氧化铜,吸收CO2和多余的CO。所以顺序是AJKFGBCDEIH。(3)装置④中浓硫酸的作用是吸收气体中的水蒸气,干燥二氧化碳。(4)装置③中氢气与氧化铜反应得铜,铜是红色的,可由此判断氢气的还原性。(5)因过量的CO是有毒的大气污染物,应除去,可用点燃的方法处理。
2. (1)②加入硝酸酸化的硝酸银溶液于样品溶液中,直到不再产生沉淀为止;③过滤
(2)漏斗、玻璃棒、烧杯 (3)取最后几滴洗出液加入稀盐酸,若无浑浊现象,说明沉淀已洗净 (4)合格
解析:要测定食盐的含量,必须根据Cl-的量进行计算。因此必须准确测定AgCl的量,当得AgCl的质量为4.90g时,含Cl的质量为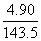 ×35.5=1.21g,则NaCl的质量为
×35.5=1.21g,则NaCl的质量为 ×58.5g≈1.99g,则食盐的含量为
×58.5g≈1.99g,则食盐的含量为 ×100%=19.9%≤20.0%,样品是合格。
×100%=19.9%≤20.0%,样品是合格。
第二篇:高一化学:1.1《化学实验基本方法》教案(新人教版必修1).doc
第一章 从实验学化学
第一节 化学实验基本方法
一、 教材分析
1.教学内容分析
“化学实验基本方法”在强调化学实验安全性的基础上,通过“粗盐的提纯”实验,复习过滤和蒸发等操作。蒸馏则是在初中简易操作的基础上引入使用冷凝管这一较正规的操作。在复习拓宽的基础上又介绍一种新的分离和提纯方法——萃取。本节还结合实际操作引入物质检验的知识,这样由已知到未知,由简单到复杂,逐步深入。
2.教学重点的分析与确定:
化学是以实验为基础的科学,通过让学生讨论一些实验问题来初步体会化学研究的方法。初中化学已经介绍了药品的取用、物质的加热、仪器的洗涤、天平的使用等基本操作,也介绍了过滤、蒸发等分离操作。本节选择粗盐提纯这一涉及基本操作较多的典型实验,复习实验原理和步骤,使学生掌握溶解、过滤、蒸发、离子检验等基本操作。进而继续学习蒸馏和萃取等新的分离方法,使学生的实验技能进一步提高。基于以上观点:
教学重点:混合物的分离与离子的检验,分离与提纯过程的简单设计。
3.教学难点的分析与确定:
从三维目标的层面上来看,掌握化学实验方法是学习化学的重要途径。能根据物质的性质设计分离和提纯的方案,并在初步掌握溶解、过滤的基础上学习蒸馏、萃取的操作,可以由已知到未知,由简单到复杂,逐步深入,并可为选修课《实验化学》中相关知识的学习打下良好的基础。基于以上观点:
教学难点:物质检验试剂的选择,蒸馏、萃取的操作,分离与提纯过程的简单设计。
二、学生分析
1.学生有一定知识基础,学习较为主动,有学习动机和兴趣,能与教师和同学进行良好的交流与合作,能够达到预定的学习目标与要求,积极关注教师创设的问题情景,积极主动参与到学习活动中去,学生在学习活动中能提出有意义的问题或能发表个人见解,能按要求正确操作,能够倾听、协作、分享。
2.学生在初中的学习过程中已经接触到一些实验知识,本章第一节的内容是对初中已有的有关实验知识的拓宽和提升。初中学生实验过程中已经涉及一些实验安全问题、分离的方法。已经初步了解了粗盐提纯的方法,蒸馏的简易装置。在本章中要在初中学习的基础上巩固粗盐提纯的操作,掌握蒸馏的实验室正规的装置和规范的操作,学习新的分离提纯的方法——萃取,还要了解有关离子的验检。可以看到第一节中学生学习的重点是混合物的分离与离子的检验。在分离提纯的学习过程中纯盐提纯有关的操作学生比较熟悉,其学习的难度不大。但对于课本中提到的提纯后溶液依然存在的杂质如何设计简单的实验进行分离提纯,对学生而言涉及物质的性质,和对性质的灵活应用,需要一定分析和逻辑思维能力,是学生学习的难点。蒸馏和萃取的实验学生比较陌生,所以学习过程中也存在一定的困难。
3.学生尚未形成适合高中学习的学习方法
三、教学目标
1.知识与技能目标
(1)初步学会物质的分离和提纯的常见方法。
(2)初步学会常见物质的检验方法。
(3)能识别化学品安全使用标识。
(4)知道基本的安全措施和意外事故的紧急处理方法。
2. 过程与方法目标
(1)通过设计粗盐进一步提纯的实验方案,体验科学探究的过程,学习运用以实验为基础的实证研究方法。
(2)通过物质的检验,混合物的分离、提纯等实验过程,学会运用观察、实验、查阅资料等多种手段获取信息,并运用比较、分类、归纳概括等方法对信息进行加工的方法。
(3)通过分组实验,交流讨论,养成实事求是的科学素养及合作意识。
3. 情感态度与价值观目标
(1)通过识记一些化学品安全标识,树立安全意识,形成良好的实验习惯。
(2)通过学习混合物的分离操作,了解化学在生产、生活和科学研究中的意义及作用,学会应用所学知识解决实际问题。
(3)通过学习废弃物处理方法,形成关心环境、爱护环境的意识。
四、教学过程
第一课时
【教学流程】

(第二课时)
【教学流程】
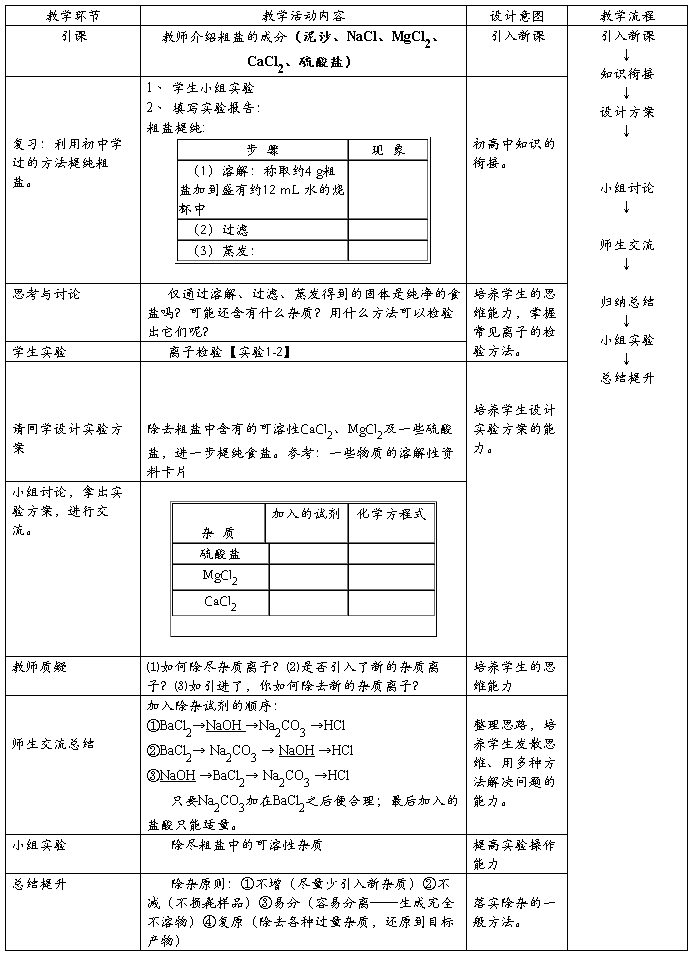
(第三课时)
【教学流程】

w.w.w.k.s.5.u.c.o.m
www.ks5u.com
w.w.w.k.s.5.u.c.o.m
www.ks5u.com
