离子共存专题
教学目标:1.掌握不同条件下,在同一水溶液中不同的离子能否大量共存的判断原则;
2.培养学生探究发现、解决问题的能力
重 点:判断在指定条件下,在同一溶液中离子能否大量共存;
根据离子共存规律推断溶液组成
难 点:根据离子共存规律及指定条件推断溶液中可能存在的离子。
考试要求:离子共存是高考及各种考试常见考点,经常以选择题以及填空题的形式出现,要求学生对于各种元素的性质具有充分的认识、掌握离子共存的规律
教学内容:
一、基础知识
问题1:常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.1.0mol/L的KNO3溶液中:H+ Fe2+ Cl- SO42-
B. 甲基橙呈红色的溶液:NH4+ Ba2+ AlO2- Cl-
C. PH=12的溶液:K+ Na+ CH3COO- Br-
D. 与铝反应产生氢气的溶液:Na+ K+ CO32- Cl-
解析:A中H+与NO3-的组合具有强氧化性,会将Fe2+氧化为Fe3+,所以不可大量共存。在考试常见的还有H+与ClO-、MnO4-的组合也具有强氧化性,不能和具有还原性的离子共存;B中甲基橙呈红色说明溶液呈酸性,存在H+,弱酸根离子AlO2-不能大量存在;C溶液呈碱性,互相之间不发生反应可以大量共存;D中与铝反应产生氢气的溶液既可以呈酸性,也可以呈碱性,若溶液为酸性,弱酸根离子CH3COO-不可以大量存在,若溶液为碱性,可以大量共存。但题干要求一定能大量共存,所以选C。
问题2:在某无色透明酸性溶液中,能共存的离子组是( )
(A)NH4+ NO3- Al3+ Cl- (B)Na+ AlO2- K+ NO3-
(C)MnO4- K+ SO42- Na+ (D)K+ SO42- HCO3- Na+
解析:在酸性溶液中,AlO2- 、HCO3-均不可大量存在,溶液为无色透明而MnO4- 为紫红色,所以选A
问题3:因发生氧化还原反应在水溶液中不能大量共存的离子组是 ( )
(A)Ca2+ Br- Fe3+ CO32- (B)Fe2+ Cl- NO3- H+
(C)Fe3+ Ca2+ H+ NO3- (D)NO3- OH- Cl- Ba2+
解析:A中离子不可大量共存因Ca2+与CO32-可以发生复分解反应产生沉淀;C、D中离子可以大量共存,B中“H++NO3-”的组合具有强氧化性,能与Fe2+发生氧化还原反应,故选B
总结:判断离子共存的关键是看离子间能否发生反应,以及是否符合指定条件,总结起来就是一句话:一色二性三特殊四反应。
一色。溶液的颜色。若限定为无色溶液,则Cu2+(蓝色)、Fe2+(浅绿色)、Fe3+(棕黄色)、MnO4- (紫红色)等有色离子不能够存在;
二性。溶液的酸性和碱性。在强酸性溶液中,OH-及弱酸根阴离子(如CO32-、SO32-、AlO2-、CH3COO-、S2-、ClO-、F-、SiO32-、C6H5O-等)均不能大量存在;在强碱性溶液中,H+及弱碱阳离子(如NH4+、Al3+、Mg2+、Fe3+等)均不能大量存在;酸式弱酸根离子(如HCO3-、HSO3-、HS-、H2PO4-等)在强酸性或强碱性溶液中均不能大量存在。
三特殊。指三种特殊情况:①AlO2-与HCO3-不能大量共存:AlO2-+ HCO3-+H2O==Al(OH)3↓+ CO32-;②“H++NO3-”的组合具有强氧化性,能与S2-、Fe2+、I-等发生反应,而这种组合往往较为隐蔽,不易被察觉;③NH4+与 CH3COO-、CO32-,Mg2+与HCO3-等组合中,虽然两组离子都能水解且水解相互促进,但总的水解程度仍然很小,它们在溶液中能够大量共存,但加热条件下就不同了。
四反应。指离子之间通常发生的四种类型的反应,能相互反应的离子显然不能大量共存。①复分解反应,如Ca2+与CO32- ,Ag+ 与Cl-等;②氧化还原反应,如Fe3+与I-,NO3-(H+)与Fe2+,MnO4-(H+)与S2-等;③双水解反应,如Al3+与HCO3- 、CO32-、HS- 、S2-、AlO2-等,Fe3+与HCO3- 、CO32-、AlO2- ,NH4+与AlO2-、SiO32-等;④络合反应,如Fe3+与SCN-等
注意:①“透明”与“澄清”溶液指此溶液不形成沉淀或混浊与溶液颜色无关
②题中涉及到水的电离则考虑到
a、室温时溶液中由水电离出来的H+浓度如果大于10-7mol/L表示溶液显酸性
b、室温时溶液中由水电离出来的H+浓度如果小于10-7mol/L表示溶液显酸性或碱性
二、课堂练习:下列离子组一定可以大量共存的是( )
A.甲基橙呈黄色的溶液:I- Cl- NO3- Na+
B.石蕊呈蓝色的溶液:Na+ AlO2- NO3- HCO3-
C.含有大量Al3+的溶液:Na+ K+ NO3- ClO-
D.含有大量OH-的溶液:K+ Cl- F- CO32-
变式:既能溶解Al(OH)3又能溶解H2SiO3的溶液中,能大量共存的离子是( )
A. NH4+ NO3- Cl- Al3+ B. Na+ AlO2- K+ NO3-
C. HSO3- K+ SO42- Na+ D. K+ SO42- HCO3- Na+
解后反思:题干中溶液显碱性,有哪些隐含条件:
①酚酞变红;
②pH=13;
③使pH试纸变蓝;
④25℃时,c(H+)/c(OH-)=10-10;
⑤既能溶解Al(OH)3又能溶解H2SiO3的溶液
思考:题干中溶液可能显酸性,也可能显碱性的隐含条件有哪些?
①由水电离产生的c(H+)=1×10-13mol/L的溶液;
②与铝反应放出氢气的溶液;
③能溶解Al(OH)3的溶液
1. 下列各组离于在溶液中既可以大量共存,且加入氨水后也不产生沉淀的是 ( )
A.Na+ Ba2+ Cl- SO42- B.K+ AlO2- NO3- OH-
C.H+ NH4+ Al3+ SO42- D.H+ Cl- CH3COO- NO3-
2.下列各组离子,在强碱性溶液中可以大量共存的是( ).
A.K+ Na+ HSO3- Cl- B.Na+ Ba2+ AlO2-
C.NH4+ K+ Cl- NO3- D.K+ Na+ ClO- S2-
3.某溶液中有NH4+、Mg2+、Fe2+和Al3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是( ).
(A) NH4+ (B) Mg2+ (C) Fe2+ (D) Al3+
4.在pH=1的溶液中,可以大量共存的离子组是 ( )
A.Na+、K+、S2-、Cl- B.Al3+、Mg2+、SO42-、Cl-
C.K+、Na+、AlO2-、NO3- D.K+、Na+、SO42-、S2O32-
三、总结:
离子共存问题解题思路:
1.审题
(1) 看清试题的前置条件,如“无色透明”、“酸性条件”、“与铝反应放出氢气的溶液” 等等
(2) 特殊要求,如“某离子存在下不能共存的”、“生成气体或沉淀不能大量共存的”、“发生氧化还原反应而不能大量共存的”等等;
(3) 看题目中要求“可能大量共存”、“一定能共存”、“一定不能共存”等等。
2.分析离子之间的反应:一般有氧化还原反应、双水解反应、络合反应和复分解反应。
四、课后作业:
1. 若某溶液跟甲基橙作用呈红色,则下列离子在该溶液中浓度不可能很大的是:( )
(A)SO42- (B)S2- (C)CO32- (D)Cl-
2. 在PH=1的无色透明溶液中不能大量共存的离子组是( )
A.Al3+ Ag+ NO3- Cl- B.Mg2+ NH4+ NO3- Cl-
C.Ba2+ K+ S2- Cl- D.Zn2+ Na + NO3- SO42-
3. 在pH=l含Ba2+离子的溶液中,还能大量存在的离子是( )
A.AlO2- B. ClO- C.Cl- D.SO42-
4. 下列各组离子:①I-、ClO-、NO3-、H+
②K+、NH4+、HCO3-、OH-
③SO32-、SO42-、Cl-、OH-
④Fe3+、Cu2+、SO42-、Cl-
⑤H+、K+、AlO2-、HSO3-
⑥Ca2+、Na+、SO42-、CO32-
在水溶液中能大量共存的是( )
(A)(1)和(6) (B)(3)和(4) (C)(2)和(5) (D)(1)和(4)
5.有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液的实验如下:

由此判断:
(1)溶液中一定存在的离子是__________________;溶液中肯定不存在的离子是:_______________;
(2)为进一步确定其它离子,应该补充的实验及对应欲检验离子的名称(如为溶液反应,说明使用试剂的名称。不必写详细步骤)___________________。
答案:(1)Mg2+、Al3+、NO3-、SO42- ;Fe2+、Ba2+、-、HCO3-;(2)焰色反应——K+、AgNO3——Cl-
第二篇:离子教案

课题3 离 子
教学目标:
1、知识与技能
(1)初步了解核外电子是分层排布的。
(2)了解离子形成的过程,认识离子是构成物质的一种粒子
2、过程与方法
(1)学习运用讨论的方法,将所学知识进行对比。
(2)运用比较、归纳的方法将所学的知识进行加工整理。
3、情感态度与价值观
(1)逐步培养学生的微观想象能力和推导思维的方法
(2)通过核外电子排布知识的介绍展示核外电子排布的规律美。
重点:离子的形成过程、核外电子排布
难点:核外电子运动的特点,离子的形成过程
教学方法:多媒体教学与发现探究
课时:二课时
第一课时
情景导入:
提问:1、你对电子有何认识?
2、你对电子还想了解什么?
问题:电子很小,运动的空间又这样特殊,它的运动与普通物体的运动有何不同,有什么特
点?你猜想下电子会怎样运动?
猜想:1、电子绕核运动
2、电子在离核近的区域运动
3、电子在离核远的区域运动
4、电子是分层运动的
验证:从课本上寻找资料,从网上查找资料
出示:从网上下载的电子形成模型
讲解:核外电子的分层排布

电子层数:一、二、三、四、五、六、七
离核距离:由近远
高
出示:原子结构示意图
提问:你从原子结构示意图中能看出什么?(即原子结构示意图表示了什么知识?) 说明:用原子结构示意图能简洁、方便地表示出原子的结构
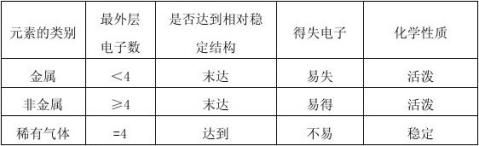
观察:课本图3-16,
想一想:你发现什么规律?
找一找:金属、非金属、稀有气体这三类元素的原子最外层有什么特点?
你知道:稀有气体为什么曾经叫惰性气体?这与它们的原子结构是否有关系?
你认为:元素的化学性质与原子的结构哪一部分有关?
小结:
练习:1、课后习题1、2
2、美国铱星公司(已破产)原计划发射77颗卫星,以实现全球卫星通讯,其要发射的数目恰好与铱元素(Ir)的原子核外电子数目相等。下列关于铱元素的各种说法中正确的( )
A、铱原子的质子数为70
B、铱原子的相对原子质量为77
C、铱原子的核电荷数为77
D、铱元素为非金属元素
总结:1、原子核外电子是分层排布的。
2、原子的结构可以用原子结构示意图表示。
3、原子的核外电子排布,特别是最外层的电子数目,跟元素的化学性质有密切关系。

总结:略
作业:新学案
教后:
第二课时 离子的形成
二、离子的形成(板书)
出示钠原子与氯原子的原子结构简图,利用钠原子和氯原子最外电子层的结构特征讲解分析离子的概念、离子符号的涵义、离子和原子的比较。
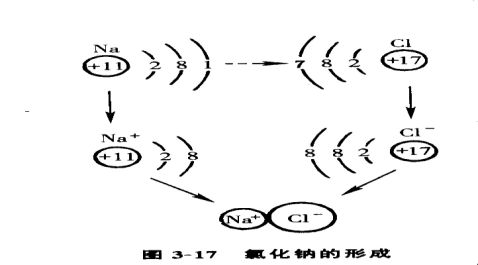
小结:1、离子:带电的原子或原子团
2、离子的表示法——离子符号
阳离子:H Na Mg Al NH4
阴离子:Cl、O、S、OH、SO4、CO3、NO3
3、离子符号的意义(数字2的意义)


离子符号前边的化学计量数表示离子个数 -2-2--2-2--++2+3++

4、离子化合物:由阴、阳离子相互作用而构成的化合物。
5、离子跟原子的比较
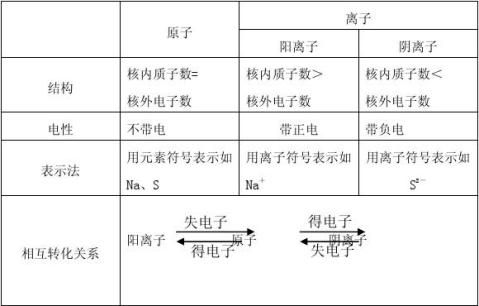
练习:请分析Kcl、CaO、MgCL2的形成过程。
小结:构成物质的微粒有分子、原子、离子等并举例说明 总结:略 作业:新学案 教后:
