湖北工程学院 化学与材料科学学院 无机化学实验报告(2013)
实验3 p区非金属元素(II)(氮族、硅、硼)
何 艳 (仅修改版面格式,未修改内容)
(学号:012301314211实验日期:20xx年3月19日 实验指导教师:周环波)
摘要(Abstracts):为了试验并掌握不同氧化态氮的化合物的主要性质,试验磷酸盐的酸碱性和溶解性,了解硅酸盐的主要性质。本实验通过一些简单可行的方法,完成了铵盐及硝酸盐的热分解的实验,磷酸盐的酸碱性和溶解性的测定与比较,以及硅酸水凝胶的制备。结果表明:铵盐加热易分解;亚硝酸易分解,不稳定,既具有氧化性又具有还原性;硝酸受热易分解,其产物取决于盐中的阳离子,且具有氧化性;磷酸盐都能水解;焦磷酸根离子具有配位性。
关键词(Key Words):氮;硅;硼;化合物;化学性质
- 1 - / 2
湖北工程学院 化学与材料科学学院 无机化学实验报告(2013)
3、结论
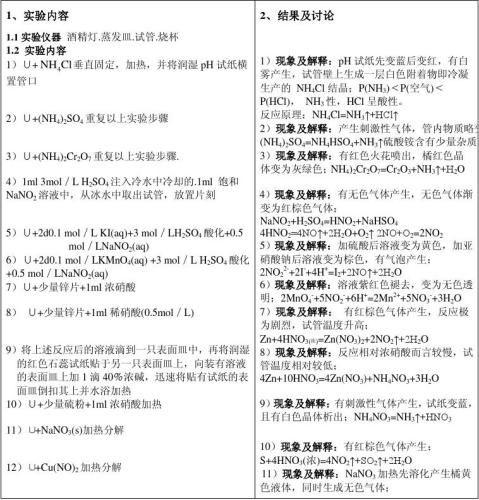
1)固态铵盐加热易分解,一般分解为氨气和相应的酸,如果酸不挥发,则生成氨气,如果生成的酸具有氧化性,则氨气被氧化为N2O,继而因不稳定分解为N2和O2;
2)硝酸盐受热易分解,其产物取决于盐中的阳离子;亚硝酸易分解,不稳定,具有弱酸性,同时既具有氧化性又具有还原性;
3)硝酸由于浓度不同具有不同程度的氧化性,与金属反应的产物也不相同;
4. 磷酸盐中,磷酸二氢盐均溶于水,正盐和一氢盐中除钾盐,钠盐,铵盐之外均不溶于水,磷酸盐都能水解,焦磷酸根离子具有配位性;硅酸盐与酸反应能产生硅酸胶体。
参考文献
[1] 北京师范大学无机化学教研室等编. 无机化学实验(第三版) [M]. 北京:高等教育出版社,2005:150-152. [2] 陈正萍. 硼砂珠实验的改进[J]. 贵州大学学报(自然科学社),1999,02:16-17. [3] 吴淑利. 新型硼酸盐的性质合成研究[D]. 宁波大学2010,25-45.

- 2 - / 2
第二篇:非金属(二)
非金属(二)
卤素
一、单质的物理性质
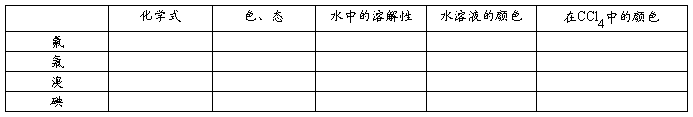
二、化学性质
1、氯气的化学性质
与金属反应:
a.与钠反应 现象 水溶液的颜色
化学方程式
b.与铜反应 现象 水溶液的颜色
化学方程式
c.与铁反应 现象 水溶液的颜色
化学方程式
与氢气反应

 a.条件① 现象
a.条件① 现象
b.条件② 现象
与水的反应:化学方程式
a.干燥的有色布条遇氯气,现象
b.湿润的有色布条遇氯气,现象
与碱的反应:离子方程式
a.与NaOH反应的方程式 用途
b.与Ca(OH)2反应的方程式 用途
2、卤素间的置换反应
a.氯气与溴化钠溶液反应 现象 离子方程式
b.氯气与碘化钾溶液反应 现象 ,向反应后的混合物中加入CCl4,现象①溶液分层,②上层 ,下层 ,
反应的化学方程式
c.溴水与碘化钾溶液反应 现象 离子方程式
3、HClO的性质① ② ③不稳定(方程式)
NaClO的性质①水溶液呈 性②与空气中CO2反应
Ca(ClO)2的性质①水溶液呈 性②与盐酸的反应
氧族
一、臭氧的性质
物理性质: 色 气味
化学性质:
a.不稳定 分解的化学方程式:
b.强氧化性
c.生成
作用与危害
二、过氧化氢
物理性质:色、态 ,俗称
化学性质:
a.弱酸性
b.强氧化性
(写出在酸性条件下氧化Fe2+的离子方程式: )
c.不稳定,在二氧化锰催化下分解的方程式:
三、SO2的性质
1、物理性质
色、 气味, 溶于水,比空气
2、化学性质
a.酸性氧化物
写出下列反应的化学方程式:
向NaOH溶液中通入少量SO2:
向Ca(OH)2溶液中通入过量SO2:
b.还原性
写出在催化剂和加热条件下,SO2与O2反应的化学方程式:
向酸性高锰酸钾溶液中通入SO2,现象
c.氧化性
SO2气体与H2S气体相遇,有黄色的固体产生,反应的化学方程式为:
d.特性
品红溶液中通入SO2气体,现象 ,加热该溶液,现象 。
四、浓硫酸的特性
1、吸水性,可做作干燥剂,但不能干燥 。
2、脱水性
浓硫酸与蔗糖(固体)混合,现象
稀硫酸与蔗糖溶液混合后,水浴加热,蔗糖转化为
3、氧化性
写出铜与浓硫酸反应的化学方程式:
若要将浓硫酸与碳反应的产物一一检出,顺序是 、 、
氮族
一、氨的性质
1、物理性质
氨气是 色、 气味的气体,密度比空气 , 溶于水。
2、化学性质
a.碱性
用化学方程式和离子方程式解释氨水呈碱性:
氨气与氯化氢气体相遇,现象 ;氨气与硝酸蒸气相遇,现
象 ,反应的化学方程式:
b.还原性
写出氨催化氧化的化学方程式:
二、硝酸的性质
1、不稳定性
写出硝酸见光或受热分解的化学方程式:
硝酸应放在 试剂瓶中保存。
2、酸的通性
3、氧化性
写出稀硝酸与铜反应的离子方程式:
由于 等金属在冷、浓的硝酸和硫酸中会 ,表面生成一层致密的氧化膜,所以可以用它们制成的容器来储存冷、浓的硝酸和硫酸。
碳族
一、二氧化碳
a.酸性氧化物
向NaOH溶液中通入CO2,随着CO2的量由少到多,将溶液低温蒸干后,固体产物可能的组合有(有多少写多少):
b.氧化性
金属镁在CO2中燃烧,现象: ,反应的化学方程式:
二、碳酸盐与酸式碳酸盐
1、同质量的Na2CO3和NaHCO3与足量的盐酸反应,产生的CO2 多。
2、向Na2CO3溶液中滴加稀盐酸至过量,开始 (有、无)气体生成,反应过程中所有的离子方程式:
3、要使NaHCO3溶液转化为Na2CO3溶液,需加 。
三、SiO2
NaOH溶液不能用带玻璃塞的试剂瓶盛放,原因是 ,反应的化学方程式为:
