实验一 有机化学实验基本知识
课时数:3学时
教学目标:
通过学习使学生了解做有机化学实验时要达到的目的和实验要求,掌握有机化学实验室规则和实验室的安全知识,介绍有机化学实验常用仪器设备使用方法以及实验预习、实验记录和实验报告的要求,使学生能够在充分安全环境中,以实事求是、严格认真的科学态度与良好的工作习惯,系统地完成有机化学实验。
教学内容:
一、有机化学实验重要性
有机化学是一门实验科学。许多有机化学的理论和规律都是在大量实验的基础上总结、归纳出
来的,并接受实验的检验而得到发展和逐步完善。在高校中,有机化学实验课始终与有机化学理论并存。可以说,有机化学离不开有机化学实验。很难想象一个不具备实验技能的人会在有机化学的科学研究和有机化工的生产指导中有重大成就。因此我们必须重视实验的教学。
二、有机化学实验目的
1、 印证课本上学到的有机化学理论知识,并加深对理论的理解。
2、 熟悉、掌握有机化学实验基本知识,基本操作能力。
(1)玻璃管的加工。
(2)组装反应装置:不同的有机反应需要不同的仪器装置,做蒸馏实验就组装蒸馏装置,做
回流实验就要求用回流装置,等等。(示范组装以上2个装置)。这就要求我们必须能够熟练组装各
种常用的反应装置。
(3)必须掌握的基本操作:重结晶、熔点的测定、沸点的测定、萃取、分液、洗涤、蒸馏(常
压、减压)、色谱分析。
重结晶常用于固体有机物的分离、提纯。萃取、分液以及洗涤的原理是一样的,都是利用物质
在不同溶剂中的溶解度不同来进行分离。而蒸馏是分离、提纯液态有机物最常用的方法之一,有的
化合物沸点较高,例如乙酰乙酸乙酯,它常压下的沸点达到180.4℃,而在这个温度下它已经部分分
解为去水乙酸和乙醇,这种情况下,我们往往采用减压蒸馏的方法。mp可用于识别物质和定性地检
测样品的纯度;bp测定可用于识别物质和液态有机化合物的分离纯化。至于色谱分析是下学期的实
验内容。
3、培养良好的科学素质。
(1)培养认真、仔细的实验态度和良好的实验习惯,做到准确、及时、详细地记录实验数据现
象,应一边实验一边直接在记录本上作记录,不能事后凭记忆补写;
(2)培养观察、分析、解决问题的能力,能正确控制反应条件和对实验结果进行综合整理分析;
(3)培养理论联系实际、严谨求实的实验作风,不虚报实验数据、现象;
(4)正确对待实验的成功、失败。
三、有机化学实验规则
1、加强预习:实验前须认真预习有关实验内容并写好预习报告,明确实验的目的要求,了解实验的原理,主要的实验试剂和实验的成败关键点、安全注意点,用简明的图表表示出反应步骤。每次实验开始前进行抽查。
2、仔细听老师讲解实验步骤、注意事项。
3、实验安全:
(1)严格按造规程操作。未经老师同意,不得擅自改变药品用量、操作条件或操作程序。
(2)实验中集中思想、认真操作、仔细观察、如实记录,不做与该次实验无关的事,不能擅自离开,
如必要时应请旁边同学代为照看。
(3)操作、处理易燃药品,如乙醚,应远离火源。
(4)取用试剂要小心。如强酸溅到皮肤上,立即用大量水冲洗,再用1%碳酸氢钠洗;如是沾到强
碱,也先用水洗,再用1%硼酸洗,再用水洗,如情况严重,紧急处理后再送到医院。
(5)有机溶剂着火:烧瓶内溶剂着火,可用湿毛巾盖灭;如果范围较大或电器着火,一定要先切断
电源、煤气,然后用四氯化碳灭火器灭火。
4、实验结束后的清理:
(1)废液倒入废液桶,不能倒入水槽。
(2)及时清洗实验仪器,打扫实验台。
(3)清点实验仪器,摆放整齐。经老师检查合格后方可离开。
(4)学生轮流值日,打扫实验室。
四、实验仪器介绍
1、 各种仪器:
烧瓶:19﹟(即烧瓶的瓶口直径为1.9cm)、24﹟,容量分为50ml、100ml、260ml等;
三口烧瓶:3×24﹟(即三个口直径均为24﹟);
直形冷凝管:蒸馏装置中用到,进水口在下端,出水口在上端;
球形冷凝管:回流装置中用到,进水口在下端,出水口在上端;
真空接引管:蒸馏装置中用到;
干燥管:下端塞脱脂棉,干燥剂常用无水氯化钙;
b形管:测熔点
蒸馏头;温度计套管;导气管;搅拌棒。
2、 注意点:
(1)、不能加热的器皿:量筒、吸滤瓶、表面皿;
(2)、需用石棉网加热的:烧杯、烧瓶、锥形瓶;
(3)、温度计不能当搅拌棒,受热后不能急冷;
(4)、带活塞的仪器用后洗净,用纸片塞上,用时涂凡士林;
(5)、仪器实行赔偿制度,属仪器质量问题或意外损坏的酌情处理,属不按操作规定而损坏的按
全额赔偿。
五、预习报告、实验报告
1、预习报告:包括实验名称、实验目的、实验原理、主要试剂和产物的物理常数、试剂规格用量、装置示意图和操作步骤。在操作步骤的每一步后面都需留出适当空白,以供实验时作记录之用。
2、性质实验报告:分二部分写,第一部分为实验目的,第二部分为实验内容。实验内容部分可用表格形式,如下:

3、 合成实验的实验报告:装置图和操作规程都按实际情况记录,不要照搬书上。实验报告应包
括以下内容。
实验题目
(1)实验目的;
(2)实验原理(或反应式,包括主反应、副反应);
(3)主要试剂及产物的物理常数;
(4)仪器装置图;
(5)实验步骤和现象记录:(用表格形式,如下图)

(6)产品外观、重量、产率;
(7)讨论:可写实验体会、成功经验、失败原因、反常现象的讨论分析、改进的设想等。
六、实验考核
实验课为单独设课的考查课程,成绩评定办法为:实验60%(包括实验预习报告、实验态度、产品质量、产率)、理论考试40%。下学期还有设计实验、实验操作考核也列入成绩评定部分。
第二篇:大学 有机化学实验内容讲义(打印版)
有机化学实验内容讲义
注:鉴于有机实验的危险性,老师应写好各个实验板书,向学生讲清实验步骤和注意事项,并于实验全程指导监督,以防事故发生。
实验安排:
第一、二周:(第1,2实验室)实验一、从果皮中提取果胶
(第3实验室) 实验二、从茶叶中提取咖啡因
第三、四周:(第1,2实验室)实验三、无水乙醇的蒸馏
(第3实验室) 实验四、甲基橙的制备
第五、六周:(第1,2实验室)实验五、乙酸异戊脂的合成
(第3实验室) 实验六、性质实验(烃、醇、醛、醛、酮)
第七、八周:(第1,2实验室)实验七、邻硝基苯酚和对硝基苯酚的合成
(第3实验室) 实验八、性质实验(羧酸、胺、糖性质)
 实验一、从果皮中提取果胶
实验一、从果皮中提取果胶
一、 实验目的
了解用酸提法从植物中提取果胶的原理和操作方法
二、 实验原理
果胶主要以不溶于水的原果胶形式存在于植物中,当用酸从植物中提取果胶时,原果被水解成果胶,果胶又叫果胶酯酸,其主要成分是牛乳糖尾酸甲酯,及半乳糖尾酸通过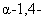 苷键连成的高分子化合物,结构片段示意如下:
苷键连成的高分子化合物,结构片段示意如下:
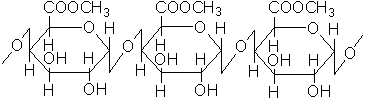
果胶不深于乙醇,在提取液中加入至约50%时,可使果胶沉淀下来而与杂质分离。
三、 仪器药品及实验材料
1. 仪器:烧杯、量筒、酒精灯、台秤
2. 药品与实验材料:果皮(柑橘、苹果、梨)、浓盐酸、活性炭、95%乙醇、滤纸、纱布
四、 实验步骤
取10g果皮(柑橘、苹果、梨)放入烧杯中,加60 ml水,再加入1.0~1.5 mL浓盐酸加热至沸腾,在搅拌下维持沸腾30min,减压过滤,滤液内加入少量活性炭,再加热20min,用滤纸过滤得浅黄色滤液。
滤液放入一小烧杯中,在不断搅拌下慢慢加入等体积的95%乙醇,会看到出现絮状的果胶沉淀。稍等片刻减压过滤,并用95%乙醇5mL分2~3次洗涤沉淀,然后将沉淀烘干,即得到果胶固体。
五、 思考题
为什么要用乙醇洗涤果胶沉淀?
实验二、从茶叶中提取咖啡因
一 实验目的
1 学习从植物中提取生物碱的原理和方法
2 练习并掌握升华操作
二实验原理
(见书略)
三实验步骤
1 称取10g茶叶,加到盛有200ml蒸馏水的大烧杯中, 用小火加热,煮沸30min,其间需不断补加蒸馏水,以弥补蒸发掉的水分;
2 趁热过滤,滤液于烧杯中加入几粒沸石,在石棉网上加热浓缩至50ml左右
3 浓缩液转移至蒸发皿中,加入少量(3g)生石灰,在沙浴上继续加热浓缩(注意:一定要有小火加热)
4 待浓缩液呈粘稠状时,蒸发皿上放一层有许多小空的滤纸,上部再放一干燥的玻璃漏斗,用沙浴加热升华
5 当滤纸上出现白色针状结晶时,停止加热,冷却即得产品。
四注意事项
1 必须要小火加热
2 沙子、沸石必须回收再利用
实验三、无水乙醇的蒸馏
一实验目的
1 学习制备无水乙醇的原理和方法
2 学习回流、蒸馏等基本操作
二实验原理
由于乙醇与水形成恒沸点为78.5℃混合物,故故为95%的工业乙醇中含有4.5%的水。要得到纯度较高的乙醇,在实验室中常用加入氧化钙加热回流,使乙醇中的水与氧化钙作用,生成不挥发性氢氧化钙来除去水分。这样得到的无水乙醇,其纯度最高可达99.5%。要制备纯度更高的绝对乙醇,可用金属镁进行处理。
三实验仪器和试剂
200ml圆底烧瓶、冷凝管、干燥管、水银温度计、尾接管、棉花、95%工业乙醇、250ml锥形瓶、生石灰、氧化钙、沸石、胶塞、水浴锅
四实验步骤
在200ml圆底烧瓶中,加入100ml 95%工业乙醇、和25g氧化钙,再加入几粒沸石。装上几粒沸石。装上回流冷凝管,在水溶上回流加热1h,稍冷后取下冷凝管,换上装有和75。玻璃弯管的胶塞,改成蒸馏装置,水浴加热蒸馏至无液滴流出,量取体积,计算回收率。
五注意事项
1 装置不要造成密闭体系,否则易爆;
2 沸石加入时不要击穿烧瓶底,沸石一定要回收利用,用后洗净放于讲台上;
3 要用小火加热,液滴回流速度为每秒1滴,否则容易爆沸飞溅;
4 胶塞安装时不要扎伤;
5 开始实验时要保证仪器干燥,不能用水洗;
6 清洗圆底烧瓶时可用热水(水浴锅)洗涮,可将Ca(OH)2;
实验四、甲基橙的制备
一、实验目的
1 掌握甲基橙的合成原理和方法
2 掌握重结晶提纯物质的方法和减压过滤等基本操作
二、实验原理
甲基橙是一种常用的酸碱指示剂,变色范围为3.1~4.4,颜色由红变黄,制备甲基橙最常用的方法是先将对氨基苯磺酸制成重氮盐,然后在低温、弱酸性条件下,与N,N-二甲基苯胺进行偶联,生成偶氮化合物甲基橙,系列合成反应如下:
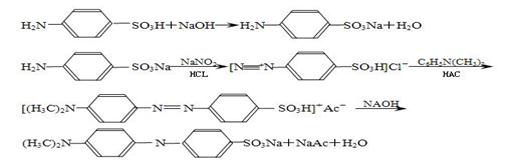
这样合成得到的甲基橙是有杂质的粗品,还要通过重结晶进行精制。
三、实验用品
1 仪器:烧杯(50mL,100mL)、试管、量筒、玻璃棒、温度计、托盘天平、布氏漏斗、抽滤瓶、滤纸
2 试剂:对氨基苯磺酸、亚硝酸钠、N,N-二甲基苯胺、浓盐酸、氢氧化钠、冰醋酸、95%乙醇、乙醚、冰块、碘化钾淀粉试纸
四、实验步骤
1 重氮盐溶液的制备:在50mL的小烧杯中,加入6mL水,然后将0.80 g 亚硝酸钠溶于水中,制成亚硝酸钠溶液备用。
在100mL的烧杯中,加入2.1 g 对氨基苯磺酸,用1.25 mol/L氢氧化钠溶液10mL 使它溶解,可适当加热。溶解后倒入已配好的亚硝酸钠溶液,不断搅拌,并将烧杯放在冰盐浴中冷却到0~5℃。然后在不断搅拌下将3mL浓盐酸和10mL水配成的溶液缓缓滴加到上述混合液中,继续搅拌10min,用碘化钾淀粉试纸检验重氮化反应的终点,若试纸出现蓝色,表示反应已到终点。此时制得的氨基苯磺酸(对磺基重氮苯)的重氮盐溶液中往往有细小的白色晶体析出[1]。把此溶液保存在冰盐浴中,待下步偶合反应中使用。
2 偶合反应:在小试管中加入1.2mL N,N-二甲基苯胺和1 mL 冰醋酸,摇匀后慢慢倾入到上述制备的重氮盐溶液中(在冰盐浴中操作),边加边搅拌,加完后继续搅拌10min,然后加入30mL左右的1.25mol/L氢氧化钠溶液,直到反应物变为橙色,得到碱式的甲基橙粗品,再放入冰水中冷却,产物完全析出,进行减压过滤。
在一小试管中取少量甲橙用水溶解,先后滴加稀盐酸和稀氢氧化钠溶液,观察溶液颜色的变化。
注释
[1]重氮盐在水中可以电离,形成中性内盐,而在低浊时难溶于水形成细小晶体析出。
五、思考题
1 为什么重氮化反应一般都要保持在0~5℃进行?
2 什么是偶联反应?结合本实验讨论一下偶联反应的条件。
3 试解释甲基橙在酸碱介质中变色的原因,并用反应式表示。
实验五、乙酸异戊酯的合成
一、实验目的
1、学习乙酸异戊酯的合成方法,了解合成香精的基础知识
2、巩固回流、蒸馏、萃取、分液、干燥等基本操作
二、实验原理
(见书略)
三、实验步骤
1、向干燥的100mL的圆底烧瓶中加18mL异戊醇、24mL冰乙酸然后缓慢分批地加入5滴浓硫酸,并加入几粒沸石,安装回流冷凝管,然后在石棉网上加热回流1h。
2、反应完毕后,取下烧瓶,在冰水浴(或冷水浴)中冷却至10℃,然后倒入125mL的分液漏斗中(注意不能使沸石进入分液漏斗)
3、摇动几分钟,等静止分层后弃去下层水溶液,若未分层可加入20mL饱和食盐水使之分层后分离,
4、再少量多次用10%碳酸钠溶液进行洗涤(注意放气),至上层液不再呈酸性为止。
四、注意事项
1、加入反应物前,所有仪器都必需干燥;
2、沸石要回收;
3、浓硫酸、冰醋酸、有强刺激性,使用时要小心,注意通风;
4、加浓硫酸一定要慢,摇匀,否则异戊醇易碳化;
5、碳酸钠溶液进行洗涤时注意放气,否则易飞溅;
6、加热时要使用小火
实验六、性质实验(烃、醇、醛、醛、酮)
(见书略)
注意事项:避免交叉污染
实验七、邻硝基苯酚和对硝基苯酚的合成
一、实验目的、原理
(见书略)
二、仪器与试剂
100mL圆底烧瓶、小烧杯、浓硫酸、硝酸钠、苯酚
三 实验步骤
1、在100mL圆底烧瓶中放入20mL蒸馏水,慢慢加入7mL浓硫酸及7.5g硝酸钠,将烧瓶放置于冷水中冷却;
2、在小烧杯中称取7g苯酚,并加少许水(3mL)温热搅拌至溶解,在振摇下用滴管向圆底烧瓶中逐滴加入苯酚溶液,保持反应温度在15~20℃之间,滴加完后放置半小时,并加以振荡,使之反应完全;
3、用冷水冷却并向烧瓶中加入25mL水,轻摇烧瓶使黄色油状物沉于瓶底,小心倾去上层酸液,油层再用水以倾泻法洗净,每次用水25mL,直至水溶液呈中性为止。
四、注意事项
1、苯酚容易氧化、聚合,不宜同混酸直接硝化;
2、苯酚对皮肤有腐蚀性,取药品时要小心,如沾到皮肤及手上,立即用肥皂水冲洗,最后用乙醇擦洗。
实验八、性质实验(羧酸、胺糖性质)
注意事项:避免交叉污染
