高二上学期第一次月考试题化学卷
可能用到的相对原子质量:C—12,O—16, H—1,S—32, N— 14
一.选择题(每小题3分,共45分)
1.下列对化学反应的认识错误的是 ( )
A.一定有化学键的变化 B.一定会产生新的物质
C.一定有物质状态的变化 D.一定伴随着能量的变化
2.已知:(1)Zn(s)+1/2O2(g)==ZnO(s) ΔH=-348.3kJ/mol
(2)2Ag(s)+1/2 O2(g)== Ag2O(s) ΔH=-31.0kJ/mol
则Zn(s)+ Ag2O(s)== ZnO(s)+ 2Ag(s)的ΔH等于 ( )
A.-317.3kJ/mol B.-379.3kJ/mol C.-332.8 kJ/mol D.+317.3 kJ/mol
3. 水的三态的熵值的大小关系正确的是( )
A. S(s)>S(l)>S(g) B. S(l)>S(s)>S(g)
C. S(g)>S(l)>S(s) D. S(g)>S(s)>S(l)
4.在温度不变的条件下,密闭容器中发生如下反应:2SO2+O2 2SO3,下列叙述能够说明反应已经达到平衡状态的是 ( )
2SO3,下列叙述能够说明反应已经达到平衡状态的是 ( )
A. 容器中SO2、O2、SO3共存
B. SO2与SO3的浓度相等
C. 容器中SO2、O2、SO3的物质的量之比为2∶1∶2
D. SO2与SO3的浓度不再变化
5.已知反应4NH3+5O2 4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(H2O)、v(NO)[mol/(L·min)]来表示,则下列关系正确的是( )
4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(H2O)、v(NO)[mol/(L·min)]来表示,则下列关系正确的是( )
A.v(NH3)=v(O2) B.v(O2)=v(H2O)
C.v(NH3)=v(H2O) D.v(O2)=v(NO)
6.热化学方程式C(s)+H2O(g) CO(g)+H2(g);△H =+131.3kJ/mol表示 ( )
CO(g)+H2(g);△H =+131.3kJ/mol表示 ( )
A.碳和水反应吸收131.3kJ能量
B.1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量
C. 1mol固态碳和1mol水蒸气反应生成1mol一氧化碳气体和1mol氢气,并吸热131.3kJ
D.1个固态碳原子和1分子水蒸气反应吸热131.1kJ
7.在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是( )
A.CH3OH(l)+3/2O2(g) CO2(g)+2H2O(l) △H=+725.8 kJ/mol
B.2CH3OH(l)+3O2(g) 2CO2(g)+4H2O(l) △H=-1452 kJ/mol
C.2CH3OH(l)+3O2(g) 2CO2(g)+4H2O(l) △H=-725.8 kJ/mol
D.2CH3OH(l)+3O2(g) 2CO2(g)+4H2O(l) △H=+1452 kJ/mol
8.长征二号捆绑式火箭推进剂以肼(N2H4)作为燃料,NO2作为氧化剂,反应生成N2和水蒸气。已知:
N2(g) + 2O2(g) = 2NO2(g);△H=+67.7 kJ/mol
N2H4(g) + O2(g) = N2(g) + 2H2O(g);△H=-534 kJ/mol
下列关于肼和NO2反应的热化学方程式中,正确的是 ( )
A.2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(l);△H=-1135.7 kJ/mol
B.N2H4(g) + NO2(g) = 3/2N2(g) + 2H2O(g);△H=-567.85 kJ/mol
C.N2H4(g) + NO2(g) = 3/2N2(g) + 2H2O(l);△H=-1135.7 kJ/mol
D.2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(g);△H=+1135.7 kJ/mol
9.氢气(H2)、一氧化碳(CO)、辛烷(C8H18)、甲烷(CH4)的热化学方程式分别为:
H2(g) + 1/2O2(g) = H2O(l);△H= —285.8 kJ/mol
CO(g) + 1/2O2(g) = CO2(g);△H= —283.0 kJ/mol
C8H18(l) + 25/2O2(g) = 8CO2(g) + 9 H2O(l);△H= —5518 kJ/mol
CH4(g) + 2 O2(g) = CO2(g) + 2 H2O(l);△H= —890.3 kJ/mol
相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是( )
A.H2(g) B.CO(g) C.C8H18(l) D.CH4(g)
10.下列关于热化学反应的描述中正确的是( )
A.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热
ΔH=2×(-57.3)kJ/mol
B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的ΔH=+2×283.0kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
11.决定化学反应速率的主要原因是 ( )
A.参加反应物质的性质 B.加入催化剂
C.温度和压强 D.各反应物和生成物的浓度
12. 在2A+B==3C+4D反应中,下面表示的反应速率最快的是( )
A.v(A)=0.5 mol·L-1·s-1 B. v (B)=0.005 mol·L-1·s-1
C.v (C)=0.9 mol·L-1·s-1 D.v (D)=1.0 mol·L-1·s-
13 在2升的密闭容器中,发生以下反应:2A(g)+ B(g)  2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速度为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是 ( )
2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速度为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是 ( )
A. 1.6 mol B. 2.8 mol C. 2.4 mol D. 1.2 mol
14. 反应2SO2+O2 2SO3经一段时间后,SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1,则这段时间为( )
2SO3经一段时间后,SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1,则这段时间为( )
A.0.1s B.2.5s C.5s D.10s
15.已知:H2O(g)=H2O(l) △H1=-Q1 kJ·mol—1; C2H5OH(g)=C2H5OH(l) △H2=-Q2 kJ·mol—1
 C
2H
5OH(g)+3O
2(g)=2CO
2(g)+3H
2O(g) △H
3=-Q
3 kJ·mol
—1
C
2H
5OH(g)+3O
2(g)=2CO
2(g)+3H
2O(g) △H
3=-Q
3 kJ·mol
—1
若使23g酒精液体完全燃烧,最后恢复到室温,则放出的热量是多少kJ( )
A.Q1+ Q2+Q3 B.0.5(Q1+Q2+Q3)
C.0.5 Q1-1.5 Q2+0.5Q3 D.1.5Q1-0.5Q2+0.5Q3
二.非选择题(共55分)
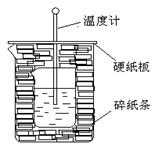 16、(7分)50ml 0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:
16、(7分)50ml 0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,尚缺少一种玻璃仪器,这玻璃仪器名称是
(2)烧杯间填满碎纸条的作用是 。
(3)若大烧杯上不盖硬纸板,求得的反应热数值 (填“偏大”“偏小”或“无影响”)。
(4)实验中该用60mL0.50mol·L-1盐酸跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”)。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会
(填“偏大”、“偏小”或“无影响”)。
(6)若三次平行操作测得数据中起始时盐酸与烧碱溶液平均温度相同,而终止温度与起始温度差t2-t1分别为12.2℃ 22.4℃ 33.4℃,则最终代入计算式的温差均值为 。
17.(6分)对于反应3X(g)+Y(g) ===Z(g),在其他条件不变时,改变其中一个条件,则生成Z的速率(填“增大”“减小”或“不变”):
===Z(g),在其他条件不变时,改变其中一个条件,则生成Z的速率(填“增大”“减小”或“不变”):
(1)升高温度:_____ ;(2)增大压强:____________;(3)增大容器容积:______________;
;(2)增大压强:____________;(3)增大容器容积:______________;
(4)加入X:______________;(5)加入Y:___________ ___;(6)压缩体积:______________.
___;(6)压缩体积:______________.
18.(12分)(1)请用热化学方程式表示
A.1mol N2(g)与适量H2(g)起反应,生成2mol NH3 (g),放出92.2kJ热量。
___________________________________________________________________
B.1mol N2(g)与适量O2(g)起反应生成2 mol NO2(g),吸收68kJ热量。
___________________________________________________________________
(2)随着科学技术的进步,人们研制了多种甲醇质子交换膜燃料电池,以满足不同的需求。有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是
A、CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0kJ/mol
B、CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ΔH=-192.9kJ/mol
由上述方程式可知,CH3OH的燃烧热 (填“大于”、“等于”或“小于”)192.9kJ/mol。已知水的气化热为44 kJ/mol,则氢气燃烧热的热化学方程式_______________________________。
(3)把煤作为燃料可通过下列两种途径:
途径Ⅰ C(s)+O2(g)=====CO2(g);ΔH1<0 ①
途径Ⅱ 先制成水煤气:C(s)+H2O(g)=====CO(g)+H2(g);ΔH2>0 ②
再燃烧水煤气:2CO(g)+O2(g)=====2CO2(g);ΔH3<0 ③
2H2(g)+O2(g)=====2H2O(g);ΔH4<0 ④
ΔH1、ΔH2、ΔH3、ΔH4的数学关系式是___________
A.2ΔH1=2ΔH2+ΔH3+ΔH4 B.2ΔH1<2ΔH2+ΔH3+ΔH4
C.2ΔH1+2ΔH2=ΔH3+ΔH4 D.ΔH1=ΔH2+ΔH3+ΔH4
19.(12分)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热。已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256.65kJ的热量。
(1)写出该反应的热化学方程式__________________________________________。
(2)已知H2O(l)====H2O(g);△H=+44kJ·mol-1,则16 g液态肼燃烧生成氮气和液态水时,放出的热量是________kJ。
(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是________________________。
(4)已知N2(g)+2O2(g)====2 NO2(g);△H=+67.7 kJ·mol-1, N2H4(g)+O2(g)=== N2(g)+2H2O (g);△H=-534 kJ·mol-1,根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式________________________________________。
20.(6分)将化合物A的蒸气8 mol充入2 L容器中加热,发生分解反应2A(g)  B(g)+ n C(g),反应到4 min时到达平衡状态,容器中B的浓度为1.6mol/L,并测得这段时间内用C的浓度变化表示的平均反应速率为v(C)=1.2 mol/(L? min)。
B(g)+ n C(g),反应到4 min时到达平衡状态,容器中B的浓度为1.6mol/L,并测得这段时间内用C的浓度变化表示的平均反应速率为v(C)=1.2 mol/(L? min)。
(1)求化学方程式中的计量数n的值=____
(2)以B的浓度变化表示该反应的平均速率为____ mol/(L? min)
(3)平衡时A的物质的量为________mol
21.(12分)将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g)===xC(g)+2D(g),经过5 min后测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的反应速率是0.1 mol/(L·min),A在5 min末的浓度是________,B的平均反应速率是________,D的平均反应速率是_ _______,x的值是________.
_______,x的值是________.
高二第一次月考化学试题答案
一.选择题(每小题3分,共45分)
1.B 2.A 3.C 4.D 5.D 6.C 7.B 8.B 9.B 10.B 11.A 12.C 13.B 14. C 15.D
16. (7分,每空1分)(1)环形玻璃搅拌棒
(2)保温(或隔热、或减少热损失)
(3)偏小
(4)不相等、相等
(5)偏小
(6)2.3
17.(6分,每空1分):(1)增大 (2)增大 (3)减小 (4)增大 (5)增大 (6)增大
18.(12分)(1)A. N2(g) + 3H2(g) ===== 2 NH3 (g) ΔH=-92.2kJ/mol (2分)
B. N2(g) + O2(g) ===== NO2 (g) ΔH=+68kJ/mol (2分)
(2)大于 (2分); H2(g)+1/2O2(g)=H2O(l) ΔH=-285.9kJ/mol (3分)
(3)A (3分)
19.(12分,每空3分)
(1)N2H4(l)+2 H2O2 (l) === N2(g)+ 4 H2O (g) △H= - 641.625 kJ·mol-1
(2)408.8 (3)生成N2和H2O,对环境无污染
(4)2N2H4(g)+2 NO2 (g) === 3N2(g)+4 H2O(g);△H= - 1135.7kJ·mol-1
20. (每空2分,共6分)
(1)3
(2)0.4
(3)1.6
21.(12分,每空3分)
0.75 mol/L, 0.05 mol/(L·min), 0.1 mol/(L·min) ,2
第二篇:高二下学期化学第一次月考试题
高二下学期化学第一次月考试题
第Ⅰ卷(共60分)
可能用到的相对原子原子质量:H─1 C─12 N─14 O─16 Na─23
Mg─24 Al─27 Cl─35.5 S─32
一、选择题(每小题只有1个正确答案,每小题3分,共60分)
1. 以下能级符号不正确的是 ( ) ...
A. 3s B. 3p C . 3d D. 3f
2、下列能跟氢原子形成最强极性键的原子是( )
A.F B.Cl C.Br D.I
3、X2+和Y-与氩(18Ar)的电子层结构相同,( )
A.原子半径: X>Y B.原子序数: X>Y
C.最外层电子数: X>Y D.电子层数: X>Y
4、下列叙述中,正确的是( )
A.两种粒子,若核外电子排布完全相同,则其化学性质一定相同
B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布式
C.两原子,如果核外电子排布相同,则一定属于同种元素
D.阴离子的核外电子排布与上一周期稀有气体元素原子核外电子排布相同
5、下列各组元素属于p区的是( )
A.原子序数为1,2,7的元素 B.O,S,P
C.Fe,Ar,Cl D.Na,Li,Mg
6、根据对角线规则,下列物质的性质具有相似性的是 ( )
A、硼和硅 B、铝和铁 C、铍和镁 D、铜和金
1
7、以下各分子中,所有原子都满足最外层为8电子结构的是( )
A、H3O+ B、BF3 C、CCl4 D、PCl5
8. 向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续
添加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象说法
正确的( )
A. 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变。
B. 沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4] 2+。
C. 向反应后的溶液加入乙醇,溶液没有发生变化 。
D. 在[Cu(NH3)4] 2+离子中,Cu2+给出孤对电子,NH3提供空轨道。
9. 关于CO2说法正确的是 ( )
A. 碳原子采取sp杂化。 B. CO2是正四面体型结构。
C. 干冰是原子晶体。 D. CO2为极性分子。
10. 下列物质的立体结构与NH3相同的是( )
A. H2O B. H3O+ C. CH4 D. CO2
11.下列分子或离子中,含有孤对电子的是 ( )
A.NH4+ B.CCl4 C.SiH4 D.H3P
12、已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( ) ..
A 、 X与Y形成化合物是,X可以显负价,Y显正价
B 、第一电离能可能Y小于X
2
C 、 最高价含氧酸的酸性:X对应的酸性弱于于Y对应的
D 、气态氢化物的稳定性:HmY小于HmX
13、实验测得 BeCl2为共价化合物,两个Be—Cl键间的夹角为180°。
由此可见,BeCl2属于( ) A.由极性键构成的极性分子
B.由极性键构成的非极性分子
C.由非极性键构成的极性分子
D.由非极性键构成的非极性分子
14.下列关于丙烯(CH3—CH =CH2)的说法正确的( )
A. 丙烯分子有7个δ键,1个∏键。
B. 丙烯分子中3个碳原子都是sp3杂化。
C. 丙烯分子存在非极性键。
D. 丙烯分子中3个碳原子在同一直线上。
15.下列说法中,错误的是( ) ..
A.非金属元素可能形成离子化合物
B.成键原子间原子轨道重叠的愈多,共价键愈牢固
C.对双原子分子来说,键能愈大,含有该键的分子愈稳定
D.键长愈长,化学键愈牢固
3
16、短周期元素R的原子核外电子数等于核内中子数,该元素单质7.8g
与氧气充分反应可生成13g化合物RO,则该元素的价电子层是 ( )
A、1s2 B、2s2 C、3s2 D、4s2
17.下列分子或离子中,能提供孤对电子与某些金属离子形成配位键的是( )。
①H2O ②NH3 ③F— ④CN— ⑤CO
A.①② B.①②③ C.①②④ D.①②③④⑤
18.膦(PH3)又称膦化氢,在常温下是一种无色、有大蒜臭味的有毒
气体,电石气的杂质中常含有膦化氢。它的分子构型是三角锥形。以下关于PH3的叙述正确的是( )。
A. PH3分子中有未成键的孤对电子 B PH3是非极性分子
C. PH3是一种强氧化剂 D. PH3分子的P—H键是非极性键
19.下列物质的杂化方式不是sp3杂化的是( )。
A.CO2 B.CH4 C.NH3 D.H2O
20、下列各组元素按电离能增加顺序排列的是 ( )
A、Li、Na、K B、B 、 Be、 Li
C、O、F、Ne D、C、P、Se
4
第Ⅱ卷(非选择题 共40分)
二、填空题(共40分)
21、(5分)某元素原子的价电子构型为4s24p1,它属于第__ 周期, _族,
最高正化合价为 ,元素符号是 _ ;外围电子排布图为。
22、(19分)根据下列某些短周期元素中元素性质的有关句回答问题。
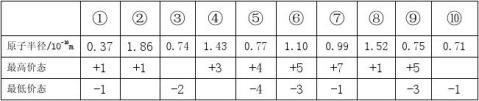
(1)元素①、②和⑧的第一电离能由大到小的顺序是
(填元素符号);元素③、⑥和⑨的氢化物中沸点由高到低的顺序是 (填化学式)。
(2)元素⑤、⑥和⑦的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质有 、 (写化学式)。
(3)某元素R的原子半径为1.02×10-10m,它与钠形成Na2R2,其化学
键类型有 、 ,其电子式是 (R用元素符号表示)。
(4)元素①和⑨形成阳离子 ,其电子式为 ,其中心原子以 杂化轨道成键。
(5)元素⑤的原子基态电子排布式为
5
23.(16分)A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和X均可形成10个电子化合物;B与Z的最外层电子数之比2:3,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红。请回答下列问题。
(1)Z的原子结构示意图为;化合物BA4的电子式为 X原子核外电子排布式为
(2)化合物Y2X2中含有的化学键类型有。
A.离子键 B.极性共价键C.非极性共价键 D.氢键
(3)化合物A2X和A2Z中,沸点较高的是,其主要原因是
(4)A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应的化学方程式为
(5)常温常压下,由A、B、X可组成的液态物质甲。现有2.3g甲与足量的X的单质充分反应,生成标准状况下2.24L的BX2气体和2.7g的A2X液体,同时放出68.35kJ的热量,该反应的热化学方程式为:。
6
高二下学期化学第一次月考试题
第Ⅰ卷(共60分)
一、 选择题(每小题只有1个正确答案,每小题3分,共60分)
第Ⅱ卷(非选择题 共40分)
二、填空题(共40分)
21. (5分22.(19分)
(1) (2分) (2分);
(2) (2分) (2分);
(3) 、(1分) , (2分)
(4) (2分) (2分);
(5) (2分)
23.( 16分)
(
1);; (各2分)
(2

)


(2分)
(3)(2分)
(4)(2分)
7
(5)(4分)
化学答案
一、选择题答案(每小题3分,共60分。每小题只有一个
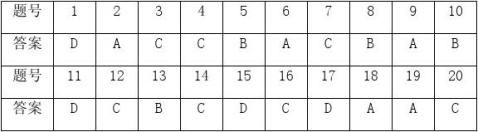
选项符合题意)
(6分)22.(18分)
(1)H、Li、Na;(2分) H2O、NH3、PH3 (2分)
;(2) CCl4、PCl3 (各2分)
-+(3)离子键、(1分)共价键,(1分)(2分) Na [ S S ]2Na+
(4) (2分)SP3 (2分);(5)1S22S22P2 (2分)
23.( 16分)
(1) ;1s22 2s22p4 (各2分) (2)A、C(2分)
(3)H2O 水分子间存在氢键(2分)
(4)4H2O2+H2S=H2SO4+4H2O或H2O+H2S=S↓+2H2O(写成H2SO3不得分)(2分) (5)C2H6O(1)+3O2(g)=2CO2(g)+3H2O(1);△H=-1367kJ·mol-1(4分
8
