电化学中对电极反应式、总反应式书写方法的总结
静海一中 张希彬
在高考复习中,同学们除了重视知识结构的建构以外,还要挖掘规律,抓住关键的知识生长点,进行迁移。在电化学的复习中要紧紧抓住原电池和电解池的本质不同,通过对电极材料和溶液介质情况分析判断后,再书写电极反应式和总反应式。
一、原电池与电解池的区别

例1 蓄电池在放电时起原电池的作用,在充电时起电解池的作用。下式是爱迪生蓄电池在放电和充电时发生的反应:


此电池负极上发生反应的物质为 ,充电时阴极发生反应的物质为 。
分析:
答:Fe;Fe(OH)2
二、原电池的电极反应和总反应式书写方法
方法:第一步确定电极的正、负;第二步根据溶液中离子参加反应情况确定电极反应;第三步将电极反应相加得总反应式。
1.仅有一电极材料参加反应
(1)酸性介质
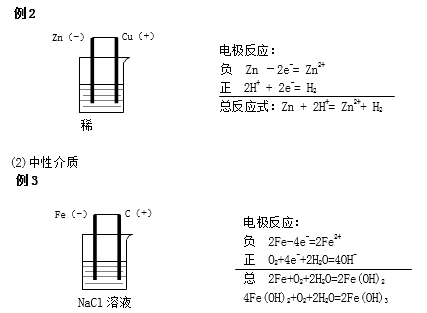
(3)将例3改为碱性介质时与中性介质电极反应式、总反应式一样
(4) 将例3改为含不活泼金属的盐溶液CuSO4溶液
负极 Fe-2e-=Fe2+
正极 Cu2++2e-=Cu

总反应式 Fe + Cu2+= Fe2++Cu
2.两电极材料均参与反应
将例1改为写出放电时的电极反应式和总反应式。
分析:正、负极电极反应式书写时,要考虑电解质对电极反应的影响,碱性介质中电极反应两边不能出现H+,电极反应为:
负极 Fe -2e-+2OH-=2Fe(OH)2
正极 NiO2+2H2O+2e-= Ni(OH)2+2OH-

总反应式 Fe+ NiO2+2H2O= Fe(OH)2+ Ni(OH)2
3.电极材料本身均不参加反应

例4 飞船上使用的电池是氢氧燃料电池。如图,两电极均由多孔性碳组成。通入气体在电极表面放电,总反应式为 2H2+O2=2H2O
写出酸性和碱性介质中的电极方程式

分析:此类电池电极不参加反应,反应的只是燃料,故确定失电子的物质为负极,得电子的物质为正极。书写电极反应要考虑介质;若介质为酸性时反应式两边不出现OH-;碱性介质反应式两边不出现H+。
三、电解池的电极反应和总反应式的书写方法
方法为:第一步:确定电极的材料及阴阳极;第二步:根据溶液中的离子判断电极反应;第三步:将电极反应相加得总反应式。
1. 仅有一个电极参加反应
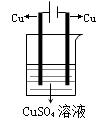 例5:
例5:
阳:Cu-2e-= Cu2+
阴:Cu2++2e-=Cu

总反应式 Cu ═ Cu
(粗铜)(精铜)

2. 两个电极都不参加反应
例5中将两个铜电极改为两
个惰性电极
阴:2Cu2++4e-=2Cu
阳:4OH--4e-=O2↑+2H2O
3.两个电极都参加反应
例如:例1中充电时书写电极反应式要考虑到反应物、生成物情况及碱性介质中在电极反应式两边不能出现H+,所以阴极与阳极的电极反应式为:
阴极:Fe(OH)2 + 2e-= Fe + 2OH-
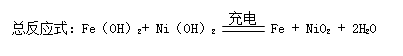

阳极:Ni(OH)2 + 2OH- -2=NiO2 + 2H2O
练习:
1.我国首创的以铝—空气—海水电池为能源的新型海水标志灯,它以海水为电解质溶液,利用空气中的氧使铝不断氧化产生电流,写出这种电池的电极材料、电极反应式及总反应式。
答:负极(Al):4Al-12e-=4Al3+
正极(C): 3O2+12e-+6H2O=12OH-
总反应式:4Al+6H2O+3O2=4Al(OH)3
2.熔融盐燃料电池具有高的发电效率,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为阳极燃气,空气与CO2的混合气为阴极助燃气,制得在650℃下工作的燃料电池。完成有关的电池反应式:
负极反应式:2CO+2CO32--4e-→4CO2
正极反应式:
总反应式:
答:正极:O2+2CO2+4e-=2CO32-
总反应式:2CO+O2=2CO2
联系电话:28942274转8002
第二篇:二轮复习电化学电极反应式的书写学案
二轮专题复习电化学——电极方程式的书写学案(一)
※ 考纲要求
1、 了解原电池和电解池的工作原理,能写出电极反应和电池反应方程式。
2、 了解常见化学电源的种类及其工作原理。
3、 理解金属发生电化学腐蚀的原因,金属腐蚀的危害,防止金属腐蚀的措施。
※近三年高考电化学的主要特点
(1)注重基础 判断电极、电极反应,电解产物以及电极反应的书写。
(2)起点高 电化学、氧化还原反应、特别是新型电池等联系,考查的知识有一定的综合度。
(3)注重实际 电化学知识与生产、生活知识(如金属的腐蚀与防护、铜的电解精炼、氯碱工业)以及新科技知识相结合。
※复习策略
电化学中电极反应式的书写不仅是电化学教学的重点和难点,更是高考的热点题型之一。 复习中应注意抓实质、重分析,注意知识的深化和迁移,分类归纳总结,突破重难点,提高复习针对性。
一、原电池中电极反应式的书写
例1、有人设计以Pt和Zn为电极材料,埋入人体内作为作为某种心脏病人的心脏起搏器的能源。它依靠跟人体内体液中含有一定浓度的溶解氧、H+ 和Zn2+ 进行工作,试写出该电池的两极反应式。
例2、用金属铂片插入KOH溶液中作电极,在两极上分别通入甲烷和氧气,形成甲烷—氧气燃料电池,该电池反应的离子方程式为:CH4+2O2+2OH-=CO32-+3H2O,试写出该电池的两极反应式。
原电池中电极反应式的书写小结:
1、先确定原电池的正负极,列出正负极上的反应物质,并标出相同数目电子的得失。
2、注意负极反应生成的阳离子与电解质溶液中的阴离子是否共存。若不共存,则该电解质溶液中的阴离子应写入负极反应式。
3、若正极上的反应物质是O2,且电解质溶液为中性或碱性,
电极反应式: 、
若电解质溶液为酸性,电极反应式: 。
4、正负极反应式相加(电子守恒)得到电池反应的总反应式。若已知电池反应的总反应式,可先写出较易书写的电极反应式,然后在电子守恒的基础上,总反应式减去较易写出的电极反应式,即得到较难写出的电极反应式。
巩固练习
1、Al-Cu-NaHCO3溶液构成的原电池中,铝件(负极)上发生的反应为:
2、(2012广东31)(4)碘也可用作心脏起搏器电源—锂碘电池的材料。该电池反应为:
2Li(s)+I2(s)=2LiI (s) △H
已知:4Li(s)+O2(g)=2Li2O(s) △H1
4 LiI(s)+O2(g)=2I2(s)+2Li2O(s) △H2
则电池反应的△H= ; 碘电极作为该电池的 极。
3、[2012·四川11]一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+ H2O = CH3COOH + 4H+。下列有关说法正确的是
A.检测时,电解质溶液中的H+向负极移动
B.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气
C.电池反应的化学方程式为:CH3CH2OH+O2=CH3COOH+H2O
D.正极上发生的反应是:O2+4e-+2H2O = 4OH-
二、电解池中电极反应式的书写
 例3 Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的水处理剂,其电解制法如下图所示,请根据图示分析:Fe电极的电极反应方程式为 。
例3 Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的水处理剂,其电解制法如下图所示,请根据图示分析:Fe电极的电极反应方程式为 。
例4 (2013广一模31)(4)电解Na2HPO3溶液也可得到亚磷酸,装置示意图如下:
① 阴极的电极反应式为_____________________________。
② 产品室中反应的离子方程式为_____________________。
电解池中电极反应式的书写小结:
巩固练习
4、(2011广东32)(4)镀铝电解池中,金属铝为 极,熔融盐电镀中铝元素和氯元素主要以AlCl4― 和Al2Cl7―形式存在,铝电极的主要电极反应式为
5、(2013江门一模)(5)工业上还可用电解法制备重铬酸钠,其装置示意图如右:
阴极发生的电极反应式为:

______
阳极发生的电极反应式为:
______
三、充电电池电极方程式的书写
例5 熔融状态下,Na单质和FeCl2能组成可充电电池(装置示意图如下),反应原理为:
 2Na+ FeCl2
2Na+ FeCl2  Fe + 2NaCl
Fe + 2NaCl
放电时,电池的正极反应式为 :
充电时, (写物质名称)电极接电源的负极;
该电池的电解质为 。
(注图中):Na:熔融Z电极 FeCl2:熔融FeG2电极
巩固练习6、蓄电池在放电时起原电池的作用,在充电时起电解池的作用。下面是爱迪生蓄电池分别在充电和放电时发生的反应:
下列有关爱迪生蓄电池的推断错误的是( )
A.放电时,Fe是负极,NiO2是正极
B.蓄电池的电极可以浸入某中酸性电解质溶液中
C.充电时,阴极上的电极反应为: 
D.放电时,电解质溶液中的阴离子向正极方向移动
课时作业 1、(2012安徽?11)某兴趣小组设计如下微型实验装置。实验时,现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是

A.断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl−  Cl2↑+H2↑
Cl2↑+H2↑
B.断开K2,闭合K1时,石墨电极附近溶液变红
C.断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e—=2Cl−
D.断开K1,闭合K2时,石墨电极作正极
2、(2013揭阳一模)11.右图所示装置中发生反应的离子方程式为:Zn + 2H+=Zn2+ + H2↑,下列说法错误的是

A.a、b不可能是同种材料的电极
B.该装置可能是电解池,电解质溶液为稀盐酸
C.该装置可看作是铜一锌原电池,电解质溶液是稀硫酸
D.该装置中通过2 mol电子,生成的气体在标况下的体积为22.4L
3、(1)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是 。
a.电能全部转化为化学能 b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动 d.利用阳极泥可回收Ag、Pt、Au等金属
(2)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为 。
(3)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为 ;与MnO2—Zn电池类似,K2FeO4—Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为 ,该电池总反应的离子方程式为 。
(4)粗铜的电解精炼如右图所示。在粗铜的电解过程中,粗铜板是图中电极 (填图中的字母);在电极d上发生的电极反应为 ;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的纯存在形式和位置为 。

4、 [2012·海南13](8分) 氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 ;
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4 (1) △H1= -195kJ·mol-1
②N2H4 ( (1) + O2(g)= N2(g) + 2 H2O △H2= -534.2kJ·mol-1
写出肼和N2H4 反应的热化学方程式 ;
(3)肼一空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为 。

