
植物生长调节剂对植物生长的影响
---S-3307烯效唑对小麦生长发育的影响
专业年级:园林08-2
姓名及学号:曾莹莹 20082621
杨洪萍 20082620
郑芳波 200825

完成日期:20##年7月6日
S-3307烯效唑对小麦生长发育的影响
摘要: 为了研究不同浓度烯效唑浸种对小麦幼苗形态和生理指标的影响。设0(CK)、5、20和40mg/L的烯效唑浸种4个处理,研究了不同浓度的烯效唑浸种对小麦幼苗的形态指标(株高、根长和发根数)与生理指标(发芽小麦呼吸强度的测定、幼苗根系活力测定、 叶绿素含量和丙二醛含量)测定。结果表明,不同浓度烯效唑浸种对小麦幼芽呼吸强度有一定的抑制作用;烯效唑能抑制地上部分的生长,促进根的伸长,增大根/冠比值;能够提高根系活力;促进叶绿素含量的增加;使丙二醛含量降低。烯效唑浸种可促进小麦壮苗、增强植物抗性,有利于小麦生产,但应注意浓度控制,以mg/L烯效唑效果最好。
关鍵词: 小麦种子 烯效唑 生长发育 形态指标 生理指标
S-3307为三唑类植物生长调节剂,又名优康唑,是一种新型高效的植物生长调节剂,广泛适用于农作物、蔬菜、果树、草坪等 。可被植物种子、叶片和根吸收,影响植物体内贝壳杉烯氧化酶活性,减少赤霉素前体的形成,阻抑内源赤霉素的合成,降低内源赤霉素水平。同时可降低内源生长素水平。S-3307是赤霉酸生物合成的颉颃剂之一,特别对单、双子叶植物均有强烈的生长抑制作用,主要抑制节间细胞的伸长,使植物生长延缓。同时促进果树花芽分化及提高作物抗逆性[1]。我国早在1958年已开始使用植物生长调节剂,但至今所使用的仅10余种。S3307作为植物生长调节剂的重要发展方向之一,近年来受到人们的广泛关注。S3307低浓度时抑制细胞伸长,高浓度时抑制细胞分裂,作用机理是阻碍植株体内赤霉素的生物合成,从而减缓细胞的分裂和伸长,抑制节间生长,幼苗高度明显降低,茎粗和分蘖数增加,增强根系活力,提高叶绿素含量,延缓作物衰老,促进花芽形成,根冠比增加和提高光合速率等生理效应[2]。对禾谷类作物有控长壮苗、促根增蘖的效果。烯效唑浸种或苗期施用可使水稻、小麦、大麦、大豆、油菜等作物增产4%~20%。种子经过浸种法处理可以充分吸收水分,利于催芽播种;可以使种子吸收一定量的农药,既可以杀灭种子携带的有害生物,又可以防止幼苗遭受病虫的危害[3]。用S3307对小麦进行干拌种(小麦籽粒冠毛对药粉有较好的粘附作用)处理,大量实验表明浸种可提高秧苗根系活力和根冠比,降低MDA含量,增加叶绿素的含量,从而保证健壮苗的形成。近些年对S3307大量实验研究表明,S3307浸种可使小麦幼苗健壮、叶片增加、叶色浓绿、根系发达和分蘖数增多,促进成穗,并有明显的增产效果[4]。
1、材料与方法
1.1 材料与试剂:小麦品种绵阳31,90%S-3307,0.1%消毒液HgCl2
1.2 方法:
1.2.1 种子的前处理
精选小麦种子100粒,用0.1%HgCl2消毒10min,用清水冲洗干净消毒液,分别用0(CK)、5、20、40mg/ml的多效唑溶液浸种24小时,倒掉浸泡液,将种子放在培养盘中,在250C-280C的恒温箱中催芽三天,待长出幼芽后,测定幼芽的呼吸强度。
1.2.2 幼苗栽植与培养(水培法)
选取在不同浓度S-3307浸泡的发芽种子240粒,栽植于塑料杯的纱网上,种植2杯,每杯种植30株,并标上记号,各大组集中放在植物生长室411进行培养,二周后用于测定幼苗的形态指标和生理指标。
2、测定项目
2.1 发芽小麦呼吸速率的测定(广口瓶法) [5]
2.1.1 空白值的测定:用移液管移取20mlBa(OH)2溶液在广口瓶中并振荡,使瓶中的CO2充分吸收,滴两滴酚酞。用浓度为1/44的草酸滴定,边滴便摇动广口瓶,使其充分显色。
2.1.2 样品值的测定:用移液管移取20mlBa(OH)2溶液在广口瓶中并振荡,使瓶中的CO2充分吸收。取不同浓度发芽小麦各40株,放进小网里里并用挂于小钩上放进广口瓶作用40分钟,其间不断晃动。同前滴定。
2.2 幼苗形态指标的测定
2.2.1 小麦株高、根长与发根数的测定:每小组分别取0、5、20、40 mg/ml多效唑处理的小麦幼苗10株,用直尺测量小麦幼苗的株高及所有根的最长根长,计算各组的平均株高、根长及发根数。
2.2.2小麦幼苗根/冠比的测定:用上面测定后的植株,除去其种子部分,把根、冠分开分别放在铝盒内,标上记号。然后在105oC杀青15-20min,在60-80℃下烘干5小时至恒重,待冷却后分别测定地上部分和根的干物质重量,计算根/冠比值。
2.3 幼苗根系活力的测定(TTC法) [6]
2.3.1 取长约1cm的根尖50根。
2.3.2 将小瓶用磷缓冲液润洗后,用移液管移取2ml磷缓冲液在小瓶内,并将根尖放入其内。加入2mlTTC,摇匀。
2.3.3 在7℃水浴中暗反应1小时。加入2ml 1mol/LH2SO4反应约2分钟后取出根尖,用吸水纸将根尖吸干。
2.3.4 色素提取:将研钵用乙酸乙酯润洗后,加入3ml乙酸乙酯,研碎。将上清液倒入试管中,用乙酸乙酯少量多次润研钵后倒入试管中。用乙酸乙酯定容至10ml。
2.3.5 比色测定:乙酸乙酯作参比液。在485nm下测定样品吸光光度值。
2.3.6 制定标准曲线。
2.4 幼苗叶片中叶绿素含量测定(分光光度计法) [7]
2.4.1 取长5cm、宽0.4cm的叶片5片。
2.4.2 色素提取:将叶片放入用80%乙醇润洗后的研钵中,加入石英砂、CaCO3少量,加入80%乙醇少量多次研钵,用漏斗过滤到25ml容量瓶中,用乙醇定容。
2.4.3 比色测定:80%乙醇润作参比液。分别在663nm、645nm下测定吸光光度值。
2.4.4 计算chl a、b含量及总量。
2.5 丙二醛(MDA)含量测定(TBA法)[8]
2.5.1 叶片处理:将剩下的叶片剪成0.5cm长的小段混匀,称取0.5g加入研钵中。加入2ml 10%TCA研磨成匀浆状。再加入6ml 10%TCA混匀,放入离心管,在4000转/分下离心10min,上清液位提取液。
2.5.2 显色测定:取两支试管,一支对照,用移液管移取提取液3ml,10%TCA3ml。一支为样品,用移液管移取提取液3ml,0.5%TBA3ml。混匀后与沸腾水浴中加热10分钟,待试管冒小泡时开始计时。冷却后,在分光光度计上波长为532nm下测定OD值。
3、结果分析
3.1 呼吸强度测定
表1 不同浓度S-3307对发芽小麦呼吸强度的影响
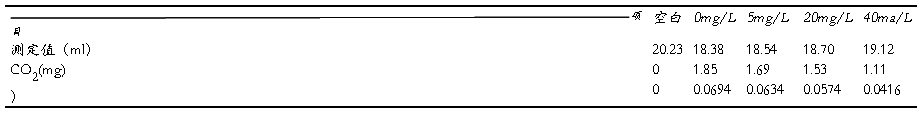
呼吸强度(CO2 mg/株.h)=(V1-V2)×C×44/株.h
实验数据表明,S-3307在一定浓度范围内会随浓度增加而抑制小麦种子的呼吸强度。烯效唑浸种处理的小麦呼吸速率显著减弱,说明S-3307作为一种生长调节剂,经过其浸泡的种子在萌发期间呼吸的强度受抑制。利用这个特点可以用于增加有机物积累,有助于提高小麦的产量。
3.2 苗形态指标的测定
表2 不同浓度多效唑浸种后幼苗的平均根长、平均苗高、发根数和根/冠比
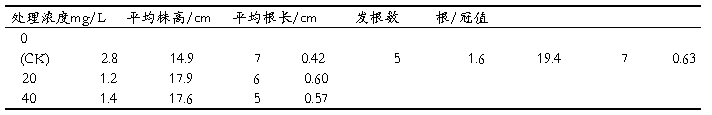
实验数据表明, S-3307在一定浓度范围内,对小麦幼苗的根生长具有促进作用,促进了分蘖;而对苗的生长具有抑制作用,减缓植株伸长。与对照相比,在S-3307浓度为5 mg/L时,根的平均长度最长,而大于5 mg/L 时,根长又有所减小。各种浓度的S-3307与对照组相比,处理浓度为5、20、40 mg/L时,幼苗株高比对照分别降低了42.86%、57.14%、50.00%;S-3307对根的生长有促进作用,当处理为5mg/L时,对根的生长有非常明显的促进作用,根长达到19.4,比对照增加30.20%。之后,随处理浓度的增加对根生长的促进作用开始减弱,20、40mg/L平均根长分别大于对照20.13%、18.12%。
所以适宜浓度S-3307浸种处理小麦种子能够防止小麦徒长,能促进小麦根系的生长,使小麦植株发育矮壮,增加其抗倒伏能力。
3.3 幼苗根系活力的测定
表3 不同浓度烯效唑浸种对小麦幼苗根系活力的影响

根系活力(ug TPF/株.h)=C×V/株×t
结果表明,S-3307在一定浓度范围内促进根系活力,如表4,其中浓度为20 mg/L的S-3307处理过的小麦,根系活力最强,大于20 mg/L的浓度处理的小麦根系活力开始降低,所以适宜浓度的S-3307处理小麦种子后,能够增强小麦幼苗根系活力,增强根系吸收水分、矿质元素的能力,获得充足的营养,有利于小麦茁壮成长,提高成活率,在农业生产上能够提高产量。
3.4 幼苗叶片中叶绿素含量的测定
表4 不同浓度烯效唑浸种对小麦幼苗叶绿素含量的影响

按Arnon公式计算有:
Chla含量(mg/dm2)=(12.7OD663—2.69OD645)×V/(S×10-2×1000)
Chlb含量(mg/dm2)=(22.9OD645—4.68OD663)×V/(S×10-2×1000)
Chl总含量(mg/dm2)=Chlb+Chla
实验结果表明,经过不同浓度S-3307处理的小麦,能够使叶片中叶绿体色素有不同程度的增加,且浓度为20 mg/L的S-3307对小麦叶片叶绿体色素含量增加最明显,超过20mg/L后有减少趋势,如表4。由此可知用20mg/l的烯效唑浸种小麦效果最佳。所以S-3307可以增加小麦叶片的叶绿素含量,从而提高光合作用的效率,促进有机物合成,增强储能,有利于增产增收。
3.5幼苗叶片中MDA含量的测定
表5 不同浓度烯效唑浸种对小麦幼苗MDA含量的影响

C( u mol/L ) = 6.45× OD532
MDA的含量(u mol/g FW)=C×V×10-3/W
实验表明,在一定浓度范围内,经过烯效唑处理的小麦叶片中MDA的含量有所减少,其中20mg/L 的S-3307处理幼苗叶片中MDA的减少量最多,超过20mg/L的S-3307处理幼苗叶片中MDA的含量又有所增加。MDA含量减少说明细胞损伤或死亡少因此可以证明烯效唑能够增强小麦的抗逆性。农业生产上用20mg/L的烯效唑浸种可以提高小麦的抗逆性,进而提高成活率所以能够提高产量。
4、结论
该试验结果表明,不同浓度的烯效唑浸种处理均可不同程度地提高小麦种子的发芽率和发芽势、叶绿素含量及根冠比,这与理论结果基本一致。种子的发芽势、发芽率是衡量植物是否具备产生壮苗能力的主要指标[9],根冠比是衡量根系吸收营养物质能力和根系发育情况的指标。叶绿素是植物合成有机物的必需物质,它含量的高低直接反映着植物合成有机物能力的高低[10] 。烯效唑处理会降低MDA含量和相对电导率,MDA是膜质过氧化的最终产物,相对电导率是衡量膜系统选择性透性的主要指标,2个指标均可以反映植物受伤害程度的高低。该试验结果表明:多效唑处理能提高种子的发芽率、根冠比、叶绿素含量,使得植物具备高产的潜力,并能增强植物抵抗不良环境胁迫的能力,有利于小麦的高产,但在使用时应注意将烯效唑浸种的浓度控制在20 mg/L以下。
参考文献
[1] 吕印谱,马奇祥,烯效唑,新编常用农药使用简明,2004
[2] 叶钟音,浸种,现代农药应用技术全书,2002
[3] 袁会珠,烯效唑,农药使用技术指南,2004
[4] 高希武,郭艳春,王恒亮,艾国民,张保民,烯效唑,新编实用农药手册,2006
[5]熊庆娥,植物呼吸速率的测定,广口瓶法,植物生理学实验教程,2003.8 68
[6]熊庆娥,植物根系活力的测定,TTC法,植物生理学实验教程,2003.8 30
[7]熊庆娥,叶绿素含量的测定,分光光度法,植物生理学实验教程,2003.8 55
[8]熊庆娥, 膜脂过氧化产物丙二酮含量的测定,植物生理学实验教程,2003.8 31
[9]吕印谱,马奇祥,烯效唑,新编常用农药使用简明手册,2004
[10]袁会珠,烯效唑,农药使用技术指南,2004
第二篇:四川农业大学植物生理学综合实验论文
四川农业大学
植物生理学综合实验论文
作者:
专业年级:
学号:
指导老师:刘帆
烯效唑(S3307)浸种对小麦种子成苗
与生长的影响
摘要: [目的]研究不同浓度的烯效唑浸种对小麦幼苗生长的影响。[方法]分别用0、10、20、40mg/L的烯效唑浸种处理,研究其对小麦幼苗形态指标和生理指标的影响。[结果]与对照相比,10、20、40mg/L的烯效唑浸种处理后,抑制了幼苗的生根和地上部分的生长,促进了其地下部分的生长,显著提高了根冠比,增强了幼苗根系活力,叶绿素总含量均明显增加,游离脯氨酸和丙二醛含量均是在10mg/L时相对升高,在20mg/L和40mg/L时相对降低。[结论]在小麦生产过程中,烯效唑使用浓度以20mg/L为宜。
关鍵词:小麦幼苗;烯效唑;形态指标;生理指标
小麦是小麦属植物的统称,是一种在世界各地广泛种植的禾本科植物。它是一种温带长日照植物,适应范围较广,自北纬17°~50°,从平原到海拔约4000m的高原(如中国西藏)均有种植。“川育20”小麦(品种)适宜在长江上游冬麦区的四川中西部。2006~20xx年度生产试验,平均亩产364.1公斤,比当地对照品种增产3.53%。川育20,春性,中熟,全生育期191天左右。幼苗半直立,分蘖力强,叶色绿,生长势旺。株高92厘米左右,略开张、整齐,成株叶片中等长宽斜上举。
烯效唑[(E)-1-对氯苯基-2-(1,2,4-三唑-1-基)-4,4-二甲基-1-戊烯-3-醇]又名高效唑,Sulgaic等,试验代号为S3307。烯效唑的生理作用很广泛,它能减弱顶端生长优势,抗倒伏,矮化植株,促进根系生长,增强植物光合作用,抑制呼吸作用。同时,具有保护细胞膜,细胞器膜,提高作物的抗逆能力的作用,并且有一定的杀菌和除草作用,是赤霉素合成抑制剂。用于小麦时,可控制营养生长,抑制细胞伸长,缩短节间,矮化植株,促进侧芽生长,花芽的形成,增强抗逆性。促进茎、叶、根生长,打破顶端优势,防止衰老。
- 1 - [2][1]
本实验采用对小麦进行不同浓度的烯效唑(S3307)浸种处理,通过研究其幼苗的形态指标和生理指标来综合反映烯效唑浸种对小麦幼苗生长的影响,增加我们对S3307的认识,同时也可为烯效唑在小麦生产中的应用提供一定的参考。
1.材料与方法
1.1 材料 “川育20”小麦,0.1%HgCl2 ,烯效唑
1.2 方法
1.2.1 小麦种子的前处理 选取健康、饱满的“川育20”小麦种子,用0.1%二氯化汞消毒10min,消毒完成后用蒸馏水反复冲洗3-4次至干净,并于吸水纸上吸干水分。将种子分成4份,分别用浓度为0(CK)、10、20、40mg/L的烯效唑浸泡,于室温条件下浸种24h。再在28℃的恒温箱中催芽3d,注意观察萌发情况并补充水。然后取4个托盘,在底层铺上吸水纸,用自来水润湿(不要有气泡)。将4份种子分别平铺在4个盘内,上面再铺一层吸水纸,将表面润湿并淋少许水。
1.2.2 幼苗的栽植与培养(基质培养) 每小组选取一种烯效唑浓度处理的发芽种子60株,分别栽种在以琼脂为基质的2个烧杯中,每杯种30株(栽植方法:以镊子在琼脂上面戳一小孔,将发芽小麦种子的根全部埋入琼脂中,芽留于琼脂面上)。栽好后在琼脂面上浇少量水。每个烧杯做好浓度标记,以每大组为单位集中放置于424温室进行培养,每隔几天适量浇水,以防止琼脂干燥。定期测定幼苗的形态指标和生理指标。
1.2.3 测定项目与方法
1.2.3.1 幼苗形态指标的测定
(1)株高、根长、发根数 选取10株幼苗,用直尺测量每株幼苗的株高、所有根的最长根长以及每株幼苗的发根数,并计算出它们的平均值。
(2)幼苗根冠比(R/T) 将上述测定后的10株幼苗取下种子按地上部分和地下部分分开,分别装入各有标记的铝盒中,先置于105℃烘箱中杀青10 min,之后降温至80℃恒温烘干至恒重(约5 h),最后在电子天平上分别称取地上和地下部分的重量并记录,计算根冠比。
1.2.3.2 幼苗生理指标的测定
1.2.3.2.1 幼苗根系活力的测定(TTC法) [3]
- 2 -
(1)标准曲线制作(全班统一) 取1ml TTC(1mg/mL)于100ml容量瓶中,加乙酸乙酯约10ml及0.5g左右的保险粉,剧烈震荡,使TTC充分还原为红色的TPF并溶于乙酸乙酯,用乙酸乙酯定容至刻度。此液中TPF浓度为10μg/mL。将上述TPF溶液稀释成系列浓度,取10ml容量瓶8个,编号,依次向各管加入TPF溶液0、2.00、4.00、6.00、8.00、10.00、12.00、14.00μg/mL,再加入乙酸乙酯定容至10ml。以空白做参比,在分光光度计上,测定485nm下的吸光度,绘制标准曲线。
(2)样品处理 选取约发芽种子15个,分别取长约1cm的幼苗根尖45根,吸干表面水分,迅速投入盛有2ml0.4%TTC和2ml磷酸缓冲液的反应混合夜的小瓶中,使根充分浸泡在溶液中。并把小瓶放入37℃恒温水域中保温1小时。
(3)根系活力测定 取出根尖吸干后置于研钵中,加入2-3ml乙酸乙酯和少量石英砂研磨。把红色提取液移入试管,并用少量乙酸乙酯洗涤残渣1次,合并入试管,最后加入乙酸乙酯定容至10ml,在分光光度计上测定485nm下的吸光度,查标准曲线后计算其根系活力。
1.2.3.2.2 幼苗叶片叶绿素含量(分光光度法)
(1)色素提取 剪取5片叶的中段(约4cm长),剪细并混匀,称取0.1g置于研钵,加入少许碳酸钙、石英砂和80%乙醇充分研磨,过滤,滤液入25ml容量瓶。用80%乙醇反复洗涤残渣和滤纸至无绿色,合并滤液,定容至25ml。
(2)比色测定 以80%乙醇做参比溶液,在分光光度计663nm、645nm下测定其吸光度(光密度OD)。
1.2.3.2.3 游离脯氨酸的测定(酸性茚三酮比色法)
(1)脯氨酸的浸提 取叶片数片剪碎后称取0.5g置于研钵中,加入少量80%乙醇和少量石英砂在研钵中研磨成均匀。将匀浆转入大试管,用乙醇洗涤研钵,洗涤液转入试管,乙醇总量10ml左右,摇匀,加塞,在沸水浴中浸提20min。
(2)脱色与去杂 向试管中加0.2g活性炭和0.5g人造沸石,剧烈振荡5-6min,过滤,滤液入25ml容量瓶。用乙醇洗涤试管、残渣,洗涤液一并转入容量瓶,加乙醇定容至刻度。
(3)显色反应 吸取2ml滤液于干燥的15ml刻度试管,加2ml冰醋酸、2ml酸性
- 3 - [5][4]
茚三酮,用玻璃球盖住试管口,置沸水浴中。同时,以80%乙醇代替滤液,做空白。反应15min,将空白及样品从沸水浴中取出,在冷水中冷却。为避免加热中各管溶液蒸发减少而影响测定结果,在加热后添加蒸馏水至原刻度处。
(4)比色 以80%乙醇为参比液,在分光光度计515nm波长下测定样品反应液的光密度,根据光密度值从标准曲线上查出样品液的脯氨酸浓度。
(5)标准曲线制作 用标准脯氨酸溶液配置成含脯氨酸0、2、4、6、8、12、16、20μg/mL的溶液。按上述相同方法取各浓度溶液、冰醋酸、酸性茚三酮显色、比色。以脯氨酸浓度为横坐标,光密度为纵坐标绘制标准曲线。
1.2.3.2.4丙二醛(MDA)含量的测定
(1)MDA的提取 取叶片数片剪碎后称取1g置研钵中,加2mL10%TCA和少许石英砂,研磨成匀浆,加入8mL10%TCA继续研磨均匀。匀浆在3000×g下离心10min,上清液即为提取液。
(2)显色测定 取10mL刻度试管2支,一支加入上清液3mL,另一支加入TCA 3mL(空白),各加0.5%的TBA溶液3mL,摇匀,在沸水浴中煮沸10min(溶液出现小气泡时开始计时),立即在冷水中冷却。如有沉淀,应离心。以空白做参比,在分光光度计430nm、532nm、600nm下测定样品反应液的吸光度值。 [6]
2.结果与分析
2.1 幼苗形态指标的测定
表2-1 烯效唑浸种处理对小麦形态指标的影响
处理浓度(mg/L) 株高(cm)
10
20
40
2.54 1.64 1.42 1.40 根长(cm) 3.91 4.08 3.95 5.20 根数(条) 根冠比(R/T) 13.6 11.0 9.4 9.7 0.085 0.492 0.567 0.560
- 4 -
图2-1
2.1.1 烯效唑对株高的影响 随着烯效唑浓度的升高,麦苗的株高依次降低,当烯效唑浓度为40mg/L时,株高最短为1.40cm,比对照降低了44.9%。说明烯效唑对麦苗地上部分的生长起抑制作用。
2.1.2 烯效唑对根长的影响 随着烯效唑浓度的升高,麦苗的根长都有所增长,当烯效唑浓度为40mg/L时,根最长为5.20cm,比对照增高了33.0%。说明烯效唑对麦苗地下部分的生长起促进作用。但烯效唑浓度与根长并不一定呈递增关系。
2.1.3 烯效唑对根数的影响 随着烯效唑浓度的升高,麦苗的根数都有所减少,当烯效唑浓度为20mg/L时,根数最少为9.4条,比对照减少了30.9%。说明烯效唑对麦苗的生根具有抑制作用。但烯效唑浓度与生根数并不一定呈递减关系。
2.1.4 烯效唑对根冠比(R/T)的影响 根冠比是植物地下部分干重与地上部分干重的比值,随着烯效唑的浓度升高,根冠比相对对照上升,当烯效唑浓度为20mg/L时,根冠比最大为0.567。说明了烯效唑有壮苗的作用,能为其创造更好的营养生长条件。但烯效唑浓度与根冠比并不一定呈递增关系。
2.2 幼苗生理指标的测定
2.2.1 根系活力的测定
表2-2 TPF标准曲线的原始数据
[7]
- 5 -

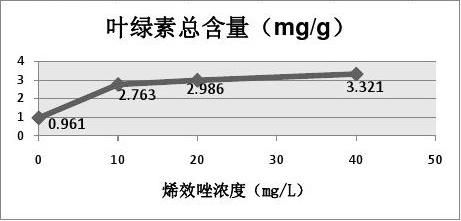
图2-2
计算公式:
根系活力(μgTPF/根·h)=(C·V/根数·t)×100
C:由标准曲线查得的浓度(mg/ml) V:提取液体积(ml) t:反应时间(h)
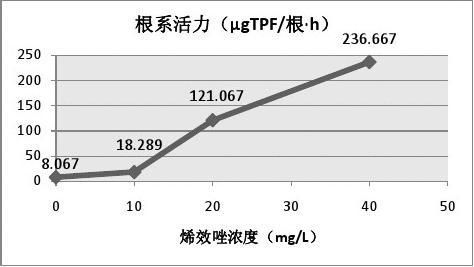
表2-3 烯效唑浸种处理对小麦根系活力的影响
处理浓度(mg/L)
0 10 20 40
吸光度值 0.015 0.034 0.225 0.440
TPF
浓度(C) 0.363 0.823 5.448 10.65
根系活力(μgTPF/根·h)
8.067 18.289 121.067 236.667
图2-3
烯效唑对根系活力的影响 根系活力是衡量根系活动能力强弱的重要指标,可以
- 6 -
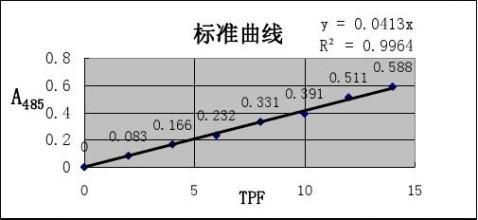
衡量根系吸收水分或矿质元素的大小,甚至可以反映地上部分的营养状况以及产量水平。据表2-2和图2-2可以看出:随着烯效唑浸种浓度的增加,TPF浓度依次增大,即根系还原的TTC增多,表明根系活力增强。并且高浓度(20mg/L及以上)的烯效唑浸种更是能显著增强根系的活力。
2.2.2 叶绿素含量的测定
表2-4 实验原始数据
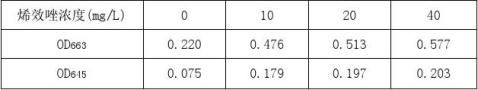
[8]
按下列Arnon公式计算材料中叶绿素a、b及叶绿素总含量。
Chla含量(mg/g)=(12.7OD663-2.69OD645)×V/1000W Chlb含量(mg/g)=(22.9OD663-4.68OD645)×V/1000W Chl总含量(mg/g)=(20.2OD663+8.02OD645)×V/1000W
OD:测定波长下的光密度值
V:叶绿素提取液总体积(ml)(若用的稀释液,则应乘稀释倍数) W:材料鲜重(g)
表2-5 烯效唑浸种处理对小麦叶绿素含量的影响
烯效唑浓度
(mg/L)
0 10 20 40
叶绿素a含量(mg/g)
0.648 1.391 1.496 1.695
叶绿素b含量(mg/g)
0.172 2.516 2.706 3.066
叶绿素总含量(mg/g)
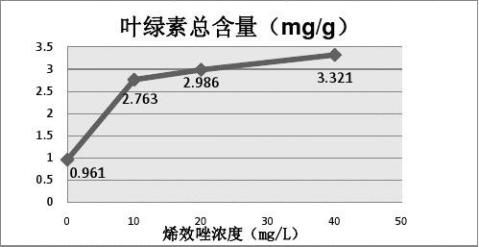
0.961 2.763 2.986 3.321
- 7 -
图2-4
烯效唑对叶绿素含量的影响 叶绿素是植物合成有机物的必需物质,它含量的高低直接反映着植物合成有机物能力的高低[9]。据表2-5和图2-4可知,烯效唑处理浓度的增加使小麦幼苗叶绿素的含量增加,且在40mg/L时达到最大值。植物体内叶绿素含量的增加,有利于植物体的光合作用,使其合成更多的有机物养料以供植物体利用。说明烯效唑能促使麦苗生成更多的叶绿素,加强其光合作用,使其合成更多的有机养料进而提高其营养状况。
2.2.3 脯氨酸的测定
表2-6 脯氨酸标准曲线的原始数据
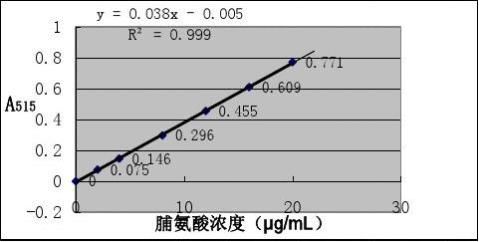
计算公式: 图2-5
样品中脯氨酸的含量(μg /g)=CX·V/dω
C:样品液的脯氨酸浓度(μg/ml)
- 8 -
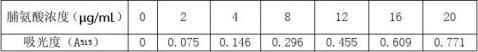
V: 提取液的总体积(ml) dω:样品干重(g)
表2-7烯效唑浸种处理对小麦脯氨酸含量的影响
烯效唑浓度(mg/L)
0 10 20 40
样品液的脯氨酸浓度
吸光度(A515)
0.036 0.044 0.017 0.022
(μg/mL) 1.068 1.275 0.574 0.704
样品中脯氨酸含量
(μg/g) 21.36 25.50 11.48 14.08
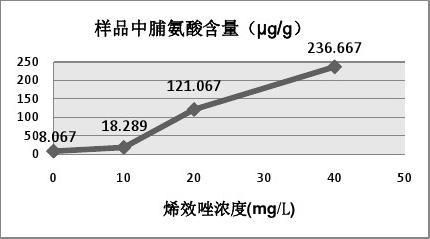
图2-6
烯效唑浓度对脯氨酸含量的影响 脯氨酸是植物体内最重要的渗透调节物质之一。当植物遭遇干旱、盐碱、高温、低温、大气污染等逆境时,体内游离脯氨酸的含量增高,抗性强的植物尤为显著。因此常以游离脯氨酸含量作为植物多种抗逆性的指标
[10]
。游离脯氨酸含量与植物的抗逆性呈负相关的关系,脯氨酸的含
量越高,植物收到的外界影响越大,其抗逆性也越差。由表2-7和图2-6可以得出结论:低浓度的烯效唑(10mg/L)会增加小麦幼苗中的游离脯氨酸含量,而较高浓度的烯效唑则会减少麦苗中的游离脯氨酸含量。说明低浓度的烯效唑会使麦苗的抗逆性减弱,而较高浓度的烯效唑则有助于增强麦苗的抗逆性(以20 mg/L的效果最好)。
2.2.4 丙二醛含量的测定
表2-8 实验原始数据
- 9 -
烯效唑浓度(mg/L)
0 10 20 40
计算公式:
OD430 1.211 1.722 0.853 0.953
OD532 0.795 0.836 0.407 0.480
OD600 0.610 0.527 0.249 0.302
C(μmol/L)=6.45(OD532-OD600)-0.56OD430 MDA的含量(μmol/g)=C×V×10/W
OD532、OD600、OD430:430nm、532nm、600nm波长下的光密度 C:提取液中MDA的浓度(μmol/L) V:提取液的总体积(ml) W:样品鲜重(g)
表2-9 烯效唑浸种处理对小麦丙二醛含量的影响
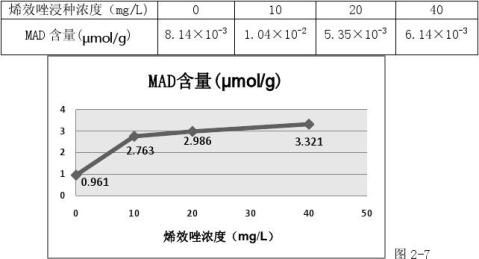
-3
烯效唑对丙二醛(MDA)含量的影响 植物遭遇逆境胁迫或衰老过程中,由于自由基、活性氧的积累引起膜脂过氧化,产生脂质自由基,进一步诱发膜脂连续过氧化并导致蛋白质交联变性,而引起细胞损伤或死亡。MDA是膜脂过氧化的最终产物,通过其含量的测定可了解膜脂过氧化伤害的程度,比较不同植物抗逆性的差
- 10 -
异[11]。丙二醛含量与植物的抗逆性呈负相关的关系,丙二醛含量越高,植物越易受到伤害,其抗逆性也越差。由表2-9和图2-7可以得出结论:低浓度的烯效唑(10mg/L)会增加小麦幼苗中的丙二醛含量,较高浓度的烯效唑则会减少麦苗中的丙二醛含量。说明低浓度的烯效唑会减弱麦苗的抗逆性,而较高浓度的烯效唑则有助于增强麦苗的抗逆性(以20mg/L的效果最好)。
3.结论与讨论
3.1 结论
综合上述所得数据分析:(1)烯效唑能显著增强小麦幼苗的根系活力,提高麦苗根系吸收水分和矿质元素的能力。由于试验中设计的烯效唑浓度差不大,因此不能确定随着烯效唑浓度的继续增加根系活力是否不断增强,这还有待于进一步研究;(2)烯效唑有利于小麦幼苗根的生长且高浓度的促进作用最好,但不利于小麦幼苗地上部分的生长,烯效唑浸种的小麦幼苗的株高降低且这种作用随浓度的增加而增强,故可知烯效唑对植物体有“控上促下”的作用[12]。因此,烯效唑增强了小麦幼苗的根冠比(R/T),表现出壮苗的效果,与周欣等的研究结果相一致[13]。同时烯效唑还会一定程度地抑制麦苗的生根;(3)烯效唑能促使麦苗生成更多的叶绿素,加强其光合作用,使其合成更多的有机养料进而提高其营养状况;(4)低浓度的烯效唑(10mg/L)会增加小麦幼苗游离脯氨酸和丙二醛的含量,减弱小麦幼苗的抗逆性,而高浓度的烯效唑则会降低其游离脯氨酸和丙二醛的含量,提高其抗逆性,使其更好地适应外界环境的变化,保护麦苗度过逆境(均以20mg/L的浓度效果最好)。
因此可以得出结论:在一定的浓度范围内,烯效唑对小麦幼苗具有壮苗的作用,施用一定浓度的烯效唑有利于促进小麦种子更好地成苗与生长,综合分析发现,20mg/L的烯效唑浸种最有利于小麦幼苗的生长,并建议在生产上使用。
3.2讨论
由于实验过程中存在随机误差以及人为操作的不当等,造成数据的不精确,可通过多次反复实验得出更精确的结论,通过测定烯效唑浓度对小麦(川育20)形态指标和生理指标的影响,确定出烯效唑的最适浓度,以便更广泛的应用到农
- 11 -
业生产以及观赏性植物中。
- 12 -
[参考文献]:
[1]栗丹,张静,鲁璐,等.高产优质抗病小麦新品种川育20的丰产性、稳定性及适应性分析[J].种子,2011,11:84-86
[2]张洪昌,李星林.植物生长调节剂使用手册[M].北京,中国农业出版社,2011,3
[3]熊庆娥.植物生理学实验教程[M].四川科学技术出版社.2003:30-31.
[4]熊庆娥.植物生理学实验教程[M].四川科学技术出版社.2003:55-56.
[5]熊庆娥.植物生理学实验教程[M].四川科学技术出版社.2003:123-124.
[6]熊庆娥.植物生理学实验教程[M].四川科学技术出版社.2003:126-127.
[7]李合生.现代植物生理学(第二版)[M].北京:高等教育出版社,2006.7.
[8]熊庆娥.植物生理学实验教程[M].四川科学技术出版社.2003:26.
[9]潘瑞炽.植物生理学[M].5版.北京:高等教育出版社,2004:57-94.
[10]熊庆娥.植物生理学实验教程[M].四川科学技术出版社.2003:123.
[11]熊庆娥.植物生理学实验教程[M].四川科学技术出版社.2003:126.
[12]罗锋,杨辉.烯效唑对小麦幼苗生长发育的影响[J].安徽农业科学,2011,39(36): 22267-22268,22434
[13]周欣,杨向平,潘珉.烯效唑对小麦幼苗生长的影响[J].云南大学学报,2001,23(S1): 96-98.
致谢:
该实验的所有材料均由四川农业大学提供。在实验的过程中离不开刘帆老师的悉心指导,在此对刘帆老师表示衷心的感谢!实验的完成更是离不开团队的合作,团队成员们分工明确,并且相互帮助,提供了大家所需的数据。可以说没有团队的合作,是无法完成本报告的,故在此对本团队所有成员表达由衷的谢意!
- 13 -
