初中易错实验题
1.有一种白色固体可能含有:BaCl2、NaCl、Na2CO3、Na2SO4和CuSO4中的一种或几种。对该固体进行如下实验。
①取样,加足量的水,充分搅拌,过滤。得到白色沉淀A和无色溶液B。
②在白色沉淀A中加入稀盐酸,沉淀全部溶解,放出能使石灰水变浑浊的无色气体。
③在无色溶液B中加入AgNO3溶液,得到白色沉淀,再加入稀盐酸,白色沉淀不溶解。请回答下列问题。
(1)原白色固体中一定不含有_________________;一定含有______________。
(2)实验①得到的无色溶液B中一定含有的溶质是_______________________。
(3)原白色固体中可能含有________________________________________
2.有一包白色固体A,可能含有 、
、 、
、 、
、 、
、 、
、 中的几种,取少量A做如下实验,主要现象如图所示。试用化学式填空:
中的几种,取少量A做如下实验,主要现象如图所示。试用化学式填空:

(1)白色沉淀B是________________,D是________________________;
(2)白色固体A中一定不存在的物质是_________________________________;
(3)若白色固体A中只含两种物质,它们是_________________________________;
(4)白色固体A还有哪些可能的组成:①______________________________
②______________________________ ③______________________________
3.有一包固体物质,可能是由H2SO4、CaCO3、Fe(NO3)3、Ba(OH)2、NaCl、MgCl2中的一种或几种组成。为确定其成分,进行如下实验:
①取样品放入小烧杯中,加水充分溶解,静置,有白色沉淀。
②再向小烧杯中逐滴加入稀硝酸,开始无现象,后沉淀逐渐溶解,最后沉淀不再减少。试推断:
(1)这包固体中一定不存在的物质是___________,可能存在的物质是___________。
(2)写出①中发生的反应方程式:
_______________________________________________________
_______________________________________________________
4.有四家相邻的小化工厂排放的废水中溶质的主要成分如下表:

为保持环境、防止污染,四厂决定联合处理废水,其处理方案如下:
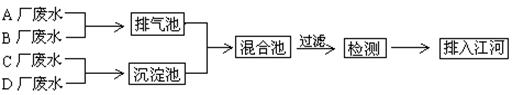
(1)排气池中发生反应的化学方程式为:____________________________
(2)沉淀池中出现的现象是______________,化学方程式为_______________
(3)若进入混合池中的物质恰好完全反应,经检测合格后排入江河的溶液中的溶质是____________________(填化学式);
(4)若排气池中B厂废水过量,则混合池中发生反应的化学方程式为:
_____________________________________________________________
5.A、B、C、D四个试剂瓶中分别盛碳酸钠、硝酸银、烧碱、稀硫酸四种稀溶液中的一种,取四种溶液各少量,依次滴入物质X的溶液和稀硝酸,发生的现象如下表所示:
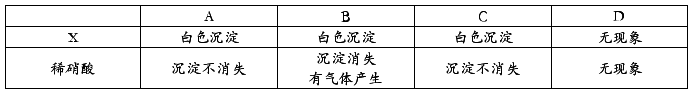
回答:
(1)物质X的化学式是_________。
(2)物质B是_______________,加入X后反应的化学方程式是__________________,加稀硝酸后,沉淀消失的反应化学方程式是___________________________。
(3)为进一步区别A和C,可根据置换反应的原理进行实验,写出其中一个反应的化学方程式___________________________。
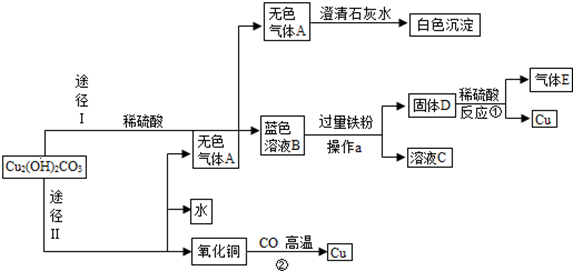
6.小红同学在实验室发现了一块绿色的孔雀石样品,他查阅资料知道其成分为Cu2(OH)2CO3。小红以孔雀石(不考虑其中的杂质参与反应)为原料设计了两种途径制取铜,其制备流程如下图所示(部分生成物略去),请回答下列问题:
⑴无色气体A是 (填化学式),固体D的成分为 (用符号表示)。
⑵写出下列反应的化学方程式:① ; ②: .
⑶操作a的名称是 ;
⑷小红同学设计的两种途径中 ,你认为途径 更合理(填“Ⅰ”或“Ⅱ”),
其理由是____ __。
7.有一包固体粉末,可能由CuSO4、CaCO3、Na2SO4中的一种或几种所组成.小文为了确定它的成分,进行了如下实验:

(1)操作a的名称是 (填“蒸发”或“过滤”),其中必须要用到的玻璃仪器有烧杯、玻璃棒和 .
(2)写出蓝色沉淀的化学式: .
(3)白色固体是 ,它与盐酸反应的化学方程式为 ,该反应所属基本反应类型为 .
(4)小文通过实验后认为,这包固体粉末中只有两种物质,他的判断是 (填“正确”或“错误”)的,理由是 .
8.有一包白色固体粉末,可能含有CuSO4、Na2SO4、(NH4)2CO3、BaCl2、NH4Cl 、KCl中的一种或几种。现做如下实验:

根据上述实验现象判断:
(1)白色固体中一定不含 ,一定含有 ,可能含有 。
(2)写出①中化学反应方程式 。
(3)写出②中化学反应方程式 。
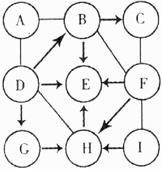 9.右图中的A~I表示几种初中化学常见的纯净物,且分别是由H、c、O、s、CI、Na、Ca中的两种或两种以上元素组成。其叶l,A、E、H是氧化物;A是大气的主要污染物之一,A中氧元素质量分数为50%;E是生产和生活中离不开的一种常见物质;I俗称小苏打,C、1分别与足量F反应的生成物相同。图中“一”表示两端的物质问能发生化学反应, “一”表示物质间存在转化关系。部分反应物或生成物已略去。
9.右图中的A~I表示几种初中化学常见的纯净物,且分别是由H、c、O、s、CI、Na、Ca中的两种或两种以上元素组成。其叶l,A、E、H是氧化物;A是大气的主要污染物之一,A中氧元素质量分数为50%;E是生产和生活中离不开的一种常见物质;I俗称小苏打,C、1分别与足量F反应的生成物相同。图中“一”表示两端的物质问能发生化学反应, “一”表示物质间存在转化关系。部分反应物或生成物已略去。
(1)写出:E的化学式为_______________,I的化学式为___________。
(2)在C物质的水溶液中滴加无色酚酞溶液,溶渡显_________色。
(3)写出A和B反应的化学方程式___________________________。
(4)写出G发生分解反应的化学方程式:__________________________。
10.有一包白色粉末,可能含有Ba(OH)2、KNO3、FeCl3、Na2CO3、Na2SO4中的一种或几种。为了确定其成分,进行如下实验:
① 取一定量的白色粉末加入足量的水,振荡,静置,得白色沉淀,上层清液为无色。
② 过滤,在白色沉淀中加入足量稀盐酸,白色沉淀全部溶解,且有气泡产生。
⑴ 据此推断,该白色粉末中一定含有 ;可能含有 ;
一定不含有 。
⑵ 写出步骤②中发生反应的的化学方程式: 。
初中易错实验题答案
1.(1)CuSO4、Na2SO4;BaC12、Na2CO3 (2)NaCl (3)NaCl
2.(1) (2)
(2) (3)
(3)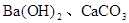
(4)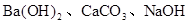

3.(1)CaCO3、Fe(NO3)3 NaCl
(2)
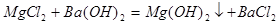
4.(1) (2)蓝色沉淀;
(2)蓝色沉淀;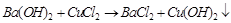 (3)
(3) (4)
(4)

5.(1) (2)碳酸钠(或
(2)碳酸钠(或 或纯碱)
或纯碱) (3)
(3) (或
(或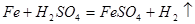
6. ⑴
 21世纪教育网
21世纪教育网
⑵反应①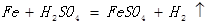
反应②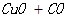 高 温
高 温 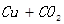 ⑶过滤
⑶过滤
⑷Ⅰ; 途径Ⅱ 需要加热,消耗较多的能量
7.(1) 过滤 , 漏斗 .(2) Cu(OH)2 .
(3) CaCO3 , CaCO3+2HCl═CaCl2+H2O+CO2↑ , 复分解反应 .
(4) 错误 , 无法判断是否存在Na2SO4 .
8.(1)CuSO4、(NH4)2CO3; Na2SO4、BaCl2、NH4Cl; KCl
(2)Na2SO4 + BaCl2=BaSO4↓+ 2NaCl

(3)NaOH + NH4Cl NaCl+ NH3↑+H2O
9. (1)H2O NaHCO3 (2)红
(3)SO2 +2NaOH = Na2SO3+ H2O
(4)CaCO3高温 CaO+CO2
10、⑴Ba(OH)2、Na2CO3 KNO3 FeCl3、Na2SO4 ⑵BaCO3+2HCl = BaCl2+H2O+CO2↑
第二篇:初中化学 实验探究题及答案
一、物质探究:
1.氯气(Cl2)是黄绿色气体,水溶液叫氯水。把品红试纸(染有品红的纸)伸入氯水中,品红褪色。
【发现问题】 氯水中的哪些成分能使品红褪色呢?
【查阅资料】 氯气溶于水,部分与水反应,方程式为Cl2 + H2O = HCl + HClO。其中,HClO的 名称叫次氯酸,是一种弱酸,具有强氧化性。
【猜 想】 猜想1:是氯水中的水使品红褪色的;
猜想2:是氯水中的 (填化学式)使品红褪色的;
猜想3:是氯水中的盐酸使品红褪色的;
猜想4:是氯水中的次氯酸使品红褪色的。
【实验探究】

结论:氯水中的 (填化学式)使品红褪色,具有漂白作用(能使品红等有色物质褪色)。
反思:(1)HClO中氯元素的化合价为 价。
(2)氯水中加入AgNO3溶液有白色沉淀生成,化学方程式为 。
(3)向氯水中滴加紫色石蕊试液,观察到的现象是 。
2.叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某兴趣小组对其进行下列研究.
(1)汽车经撞击后,30毫秒内引发NaN3,迅速分解为Na、N2,反应方程式为_______。
(2)将金属钠与液态氨反应得NaNH2,再将NaNH2与N2O反应可生成NaN3、NaOH和气体X,该反应的化学方程式为2NaNH3+N2O = NaN3+NaOH+X,实验室检验X气体使用的试纸是湿润________。
工业级NaN3中常含有少量的Na2CO3,为测定样品中Na2CO3的质量分数设计如图装置(已知H2SO4溶液与NaN3,反应不生成气体)。

(3)装置A的作用是_____。设计的实验步骤为:①精确称量样品,检查装置气密性;②打开弹簧夹,鼓入空气,称量装置C;③关闭弹簧夹,打开分液漏斗活塞;④再打开弹簧夹,_____;⑤再次称量装置C。
计算碳酸钠含量至少需要测定______(填数字)个数据。根据制备反应,分析工业级NaN3中含有Na2CO3的可能原因_______。

【NaN3纯度测定】
精确称量0.140 g NaN3样品,设计如图装置,测定其纯度。已知2NaN3 → 3N2 (NaN3中的N全部转化为N2,其他产物略),反应中放出大量的热。
(4)检查该装置气密性的方法是连接好装置,从水准瓶注水,量气管中液面与右边液面形成高度差,做好标记,一段时间后,两边高度差_____(填“变大”、“变小”或“不变”),说明气密性良好。
(5)使小试管中的NaN3样品与M溶液接触的操作是______。
(6)使用冷水冷凝的目的是______。反应前应将液面调节到量气管的“0”刻度,并使两边液面相平,反应后读数时,还需要进行的操作是_______。
(7)常温下测得量气管读数为67.2 mL(N2的密度为1.25 g/L),则实验中选用的量气管规格合适的是_____(填字母序号)。
A. 100 mL B. 1 L C. 2 L
(8)计算NaN3样品的纯度(写出计算过程)。
二、实验探究:
3.梧州市某中学化学兴趣小组按照课本实验方法(如图19甲),做木炭与氧化铜反应实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现。他们决定对这个实验进行探究和改进。


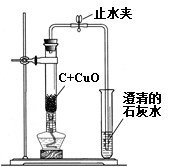


提出问题:暗红色的固体是什么?如何选择合适的条件,使木炭还原氧化铜的实验现象更明显?
查阅资料:铜有+1和+2两种化合价,通常情况下,氧的化合价为-2,碳的化合价为+4或-4。
猜想与假设:(1)同学们认为这种暗红色固体可能是一种化合物,并猜测它的化学式为 。
(2)同学们还认为,通过改变反应物的状态、质量比,以及反应装置,可以使该实验现象更加明显,减少出现暗红色固体的情况。
分析与交流:(1)小吴建议用超细炭粉与氧化铜粉末进行实验。你认为这样建议的原理是 。
(2)小周建议用图19的乙装置替代甲装置。与甲相比较,乙装置中将试管直立放置的作用是 。
(3)对下列三种氧化铜和碳的质量比例,小施建议选择 (填选项序号)的比例。
A. 32︰3 B. 40︰3 C. 48︰3
你认为小施这样选择的理由是 。
实验与结论:
同学们决定按改进后的方案进行实验,他们在检验了乙装置的 后,往试管中加入已干燥的药品并开始加热,当看到澄清的石灰水刚出现浑浊时, (填“可以”或“不能”)确定氧化铜和炭粉已经开始反应。不久,即可看到试管底部变红热,停止加热后,仍能看到红热现象,并沿试管底部自下而上蔓延,这个现象说明该反应是 (填“吸”或“放”)热反应。待反应结束,先将导气管从石灰水中取出,然后关闭止水夹,让产物自然冷却。若不关闭止水夹,可能出现的问题是 。待产物冷却后,同学们终于找到了期待已久的紫红色铜珠,实验获得了圆满成功。
三、现象探究:
4.20##年4月28日某媒体题为“排污工程施工,毒气放倒三人”的报道,引起某兴趣小组同学的思考。
提出问题:排污管道中的毒气有什么成分?
查阅资料:I.排污管道中的大部分有机物在一定条件下发酵会产生CO、CO2、H2S、CH4等。
Ⅱ.H2S气体能与CuSO4溶液反应生成黑色沉淀。
提出猜想:小组同学对排污管道气含有上述气体中最少3种成分的猜想如下:
猜想1:有CO、CO2、H2S; 猜想2:有CO、CO2、CH4; 猜想3:有CO、H2S、CH4;
猜想4:有CO2、H2S、 ; 猜想5:有CO、CO2、H2S、CH4。
实验方案:小组同学共同设计了下图所示的装置并进行探究(夹持仪器已省略)。
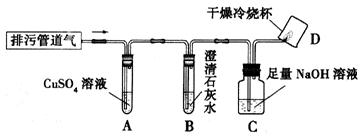
问题讨论:(1)若A装置没有明显变化,则猜想 成立;若B装置没有明显变化,则猜想 成立。
(2)在验证猜想l的实验中,装置C中NaOH溶液的作用是 ;若要进一步验证
气体燃烧后的产物,操作是:迅速把烧杯倒过来,向烧杯内注入 ,振荡。
(3)要确证猜想5中是否有CH4,某同学认为图示装置有不足之处,需要在装置C与D之间加一个 装置。改进后,若气体燃烧,且D装置内壁出现 ,证明气体中一定含有CH4。为了进一步确定气体中是否含有CO,可分别测定燃烧产物中H2O、CO2的质量。其方法是:将燃烧产物依次通过盛有 、 的装置,分别称量吸收燃烧产物前、吸收燃烧产物后装置的质量,通过计算、分析得出结论。
化学答案(实验探究题)
1.【猜 想】Cl2 【实验探究】③把品红试纸伸入到盐酸中 【结 论】HClO
【反 思】(1)+1 (2)AgNO3+HCl=AgCl↓+HNO3 (3)先变红色后褪色
2.(1)2NaN2=2Na+3N2↑ (2)红色石蕊试纸 (3)除去空气中的CO2 缓缓放入空气 3 生成NaN2的同时有NaOH生成,NaOH吸收空气中的CO2生成Na2CO3 (4)不变 (5)倾斜锥形瓶,使样品与M溶液接触 (6)降低气体温度(防止量气管中水喷出) 调节两边液面相平 (7)A (8)92.9%
3.【猜想与假设】Cu2O (Cu4C、Cu2C等)
【分析与交流】(1)这是固体反应物间的反应,使用颗粒更小的反应物,可以增加表面积,有利于反应的进行。 (2)有利于集中加热,获得持续高温。
(3) A 反应中炭粉会与试管内的氧气反应而部分消耗,故稍过量的炭粉有利于反应的进行。
【实验与结论】气密性 不能 放 空气会进入反应的试管中,使生成的依然灼热的铜重新被氧化。
4.【提出猜想】CH4 【问题讨论】(1) 2 3 (2) 吸收CO2 澄清石灰水 (3) 干燥 水雾 浓H2SO4(或CaCl2或无水CuSO4) NaOH溶液
