高一化学上学期期末复习
第一单元 丰富多彩的化学世界
一、离子反应及其发生的条件
⑴.电解质在水溶液中反应的实质
多种电解质在水溶液中发生电离,产生能够自由移动的离子,不同离子之间发生反应生成沉淀、气体、水等。
① 离子反应:有离子参加的化学反应。
②离子反应发生的条件(离子不能大量共存的规律)—— 物质之间能发生复分解反应
生成难溶物或微溶物:如Ba2+与CO32-、Ag+与Br-、Ca2+与OH-、Mg2+与CO32-、OH-等之间发生离子反应。
生成气体或挥发性物质:如NH4+与OH-,H+与CO32-、HCO3-、HSO3-、SO32-等之间发生离子反应。
生成弱电解质:如H+与CH3COO-、CO32-等生成弱酸;OH-与NH4+等生成弱碱;H+与OH-生成水(水也是种弱电解质)。
⑵.离子方程式
① 书写离子方程式的步骤
写:写出正确的化学方程式;
拆:将化学方程式中易溶解于水且能完全电离的物质拆写成阴、阳离子符号;而难溶于水的物质、气态物质和水仍用化学式表示;
删:删去方程式等号两边重复的离子;
查:检查是否满足元素原子守恒、反应前后电荷守恒等。
② 书写离子方程式的方法
化学式与离子符号使用要正确,其规律是:一般易溶于水的强酸(H2SO4、HNO3、HCl、HBr、HI)、强碱(NaOH、KOH、Ba(OH)2、Ca(OH)2)、大多数可溶性盐均写成离子符号(拆);而单质、氧化物、弱电解质、非电解质极难溶于水的物质均写成化学式(不拆)。
判断离子方程式书写是否正确,注意两守恒:方程式两边的原子数、电子数必须守恒。
5. 离子共存题易错点:(B)
⑴ 在题目中告知是无色溶液,应排除具有颜色的离子
Fe2+(浅绿色)、Fe3+(黄色)、Cu2+(蓝色)、MnO4—(紫色)等离子。
⑵ 多元弱酸的酸式酸根离子不能与H+、OH—大量共存 HCO3—、HSO3-、
6.元素化合价在化学反应中的变化(B)
⑴ 氧化还原反应:凡有元素化合价升降的化学反应就是氧化还原反应。
非氧化还原反应:凡没有元素化合价升降的化学反应,就是非氧化还原反应。
⑵ 氧化还原反应特征(判别方法):化合价发生变化。
8.氧化还原反应的实质 (B)
⑴ 元素化合价升降的实质:化合价升高,该元素原子在反应中失去电子;
化合价降低,该元素原子在反应中得到电子。
⑵ 氧化还原反应的本质:反应过程中有电子得失(或偏移)。
9. 氧化剂和还原剂(C)
⑴ 定义:
① 从化合价角度定义:在氧化还原反应中,所含元素的化合价降低的反应物,称为氧化剂;在氧化还原反应中,所含元素的化合价升高的反应物,称为还原剂。
② 从电子转移角度定义:在氧化还原反应中,得到电子(或电子偏近)的反应物,称为氧化剂;在氧化还原反应中,失去电子(或电子偏离)的反应物,称为还原剂。
⑵ 记住一些常见的氧化剂和还原剂
⑶ 价态与氧化剂、还原剂的关系:
① 元素为最低价态时,只具有还原性。I-,S2-等。
② 元素为最高价态时,只具有氧化性。Fe3+,H+等。
③ 元素处于中间价态时,既具有氧化性,又具有还原性。如S、SO2 ,Fe2+,I2,H2O2。
⑷ 一般来说,氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物。

二、物质的量(要非常注意掌握几个基本量的计算)
1、物质的量是一个物理量,符号为 n,单位为摩尔(mol)
2、1 mol粒子的数目是0.012 kg 12C中所含的碳原子数目,约为6.02×1023个。
3、1 mol粒子的数目又叫阿伏加德罗常数,符号为NA,单位mol-1。
4、使用摩尔时,必须指明粒子的种类,可以是分子、原子、离子、电子等。
5、N = n NA(NA表示阿伏加德罗常数)
三、摩尔质量
1、定义:1mol任何物质的质量,称为该物质的摩尔质量。
用符号:M表示,常用单位为g·mol-1

2、数学表达式:
四、物质的聚集状态
1、物质的聚集状态:气态、液态和固态
决定物质体积大小的因素:粒子数目、粒子大小和粒子间的距离
2、气体摩尔体积
单位物质的量的气体所占的体积。符号:Vm表达式:Vm=V/n ;单位:L·mol-1
在标准状况下,1 mol任何气体(包括混合气体)的体积都约是22.4 L。
五、物质的分散系
2.胶体:(1)概念:分散质微粒直径大小在10-9~10-7m之间的分散系。
(2)性质:①丁达尔现象(用聚光手电筒照射胶体时,可以看到在胶体中出现一条光
亮的“通路”,这是胶体的丁达尔现象。)
②凝聚作用(吸附水中的悬浮颗粒,如明矾净水)
3.溶液:电解质溶液、非电解质溶液
4.化合物
电解质:在水溶液中或熔融的状态下能导电的化合物
非电解质:在水溶液中或熔融的状态下都不能导电的化合物
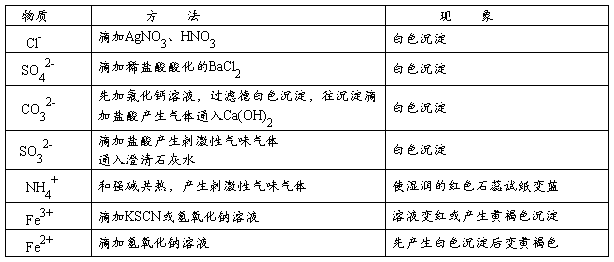
2、常见气体和离子的鉴别:
第三单元人类对原子结构的认识
一. 1. 核外电子排布规律:
(1) 核外电子总是尽先排布在能量较低的电子层,然后由里向外排布在能量较高电子层
(2) 原子核外各电子层最多容纳2n2个电子(表示电子层数)。
(3) 原子最外野电子数目不能超过8个(第一层不能超过2个)
(4) 次外层电子数目不能超过18个(第一层为次外层时不能超过2个),倒数第三层电子数目不能超过32个。
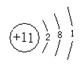
注意:请写出Cl、Na、Br、Mg、Al、Fe、S、N、C、O、H、Si等原子的结构示意图。
1.几个重要的关系式
质量数(A)=质子数(Z)+中子数(N)
(1) 原子:核电荷数(质子数)=核外电子数,
(2) 阳离子:核电荷数(质子数)>核外电子数,
(3) 阴离子:核电荷数(质子数)<核外电子数,
2.两个重要的概念
核素:具有一定质子数和一定中子数的一种原子。
同位素:质子数相同、质量数(中子数)不同的原子(核素)互为同位素
3.原子的最外层电子数决定该元素的化学性质。
 第三章 金属及其化合物
第三章 金属及其化合物
1.钠及其重要化合物的性(B)
⑴原子结构示意图:
⑵ 钠的物理性质:
银白色、有金属光泽的固体;密度小,ρ(Na)=0.97g/cm3,比水的密度小;熔点和沸点低,熔点97.81℃,沸点882.9℃;硬度小,可以用小刀切割。
⑶ 钠的化学性质:
① 钠与水的反应:2Na + 2H2O = 2NaOH + H2↑
② 钠与氧气的反应:
钠在空气中被氧化:4Na + O2 = 2Na2O(白色固体)
钠在空气中加热或点燃:2Na + O2  Na2O2(淡黄色固体)
Na2O2(淡黄色固体)
⑷ 钠的保存及用途
① 钠的保存:钠很容易跟空气中的氧气和水起反应,因此,在实验室中,通常将钠保存在煤油里,由于ρ(Na) >ρ(煤油),钠沉在煤油下面,将钠与氧气和水隔绝。
② 钠的用途:钠钾合金(室温下呈液态),用作原子反应堆的导热剂。
制备Na2O2 作为强还原剂制备某些稀有金属。
⑸ 氧化钠与过氧化钠的性质比较
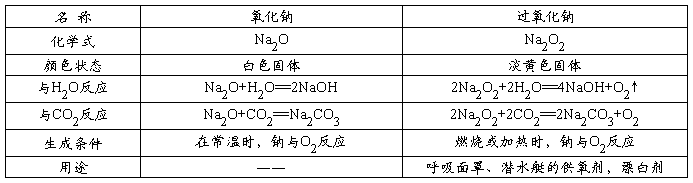
⑹ 钠盐

⑺ 碱金属元素(A)
①化学性质:
单质的化学性质相似,都具有强还原性,能跟卤素、氧气、硫等多数非金属直接化合。由Na 到Cs ,单质的还原性逐渐增强。单质能跟水反应,生成相应的碱和氢气。
② 焰色反应:是指金属或其化合物在灼烧时使火焰显现出特殊的颜色;属物理变化。
2. 从海水中提取镁
步骤:① 将海边的贝壳煅烧成石灰,再制成石灰乳,加到海水沉淀池,得到氢氧化镁沉淀;
② 将上制得的氢氧化镁沉淀与盐酸反应生成MgCl2·6H2O晶体,并使其在氯化氢气流中加热脱水得到氯化镁。
③ 电解熔融的氯化镁即可得到镁。
 化学方程式:
化学方程式:
3. 铝及其重要化合物的性质(B)
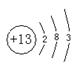
⑴原子结构示意图:
⑵ 物理性质:
密度小熔点较低,硬度较小,银白色金属;
⑶ 化学性质
① 跟O2及其它非金属反应
常温下,在空气中都因生成氧化膜,具有抗腐蚀能力。
4Al+3O2 2Al2O3
2Al2O3
②跟非氧化性酸的反应
2Al+6H+==2Al3++3H2↑(常温下,在浓H2SO4、浓HNO3中钝化)
③跟碱反应 2Al+2NaOH+2H2O == 2NaAlO2+3H2↑
⑷ 铝的化合物

4. Fe的性质(B)
⑴是一种变价元素,通常显示+2价、+3价,其化合物和其水溶液往往带有颜色。
 ⑵ Fe与O2反应,随着外界条件和两者量的相对多少不同,生成的产物不同。
⑵ Fe与O2反应,随着外界条件和两者量的相对多少不同,生成的产物不同。

 3Fe + 2O2 (纯) Fe3O4(黑色、有磁性)
3Fe + 2O2 (纯) Fe3O4(黑色、有磁性)
 4Fe + 3O2 2Fe2O3(红棕色)
4Fe + 3O2 2Fe2O3(红棕色)
生成Fe3O4的反应还有:3Fe+4H2O(g) Fe3O4+4H2
⑶铁与酸的反应:
铁与盐酸、稀硫酸的反应:Fe + 2H+ == Fe2+ + H2O(反应后溶液呈浅绿色)
⑷ 铁的氧化物

⑸ 铁的氢氧化物 (C)
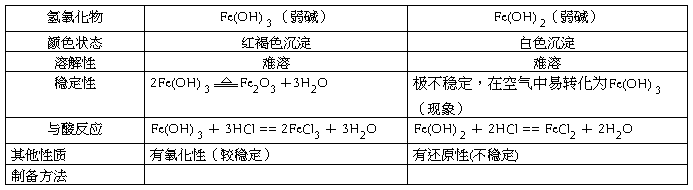
思考:用可溶性碱分别与Fe2+、Fe3+反应可制得Fe(OH)2和Fe(OH)3。通过哪些方法可避免生成Fe(OH)2中会有Fe(OH)3?
提示:关键在于无孔不入的O2及Fe3+存在。4Fe(OH)2 + O2 + 2H2O == 4Fe(OH)3
①驱氧法:如用同煮沸过的NaOH溶液和亚铁盐溶液。
②隔氧法:如用长滴管吸取NaOH溶液后插入亚铁盐溶液面下加入;又如在液面上加某些合适的有机溶剂液封。
③还原法:在FeSO4溶液中加入Fe钉,或者用Fe与稀H2SO4反应新制的FeSO4溶液,生成的H2又可驱赶O2。
⑹ 盐
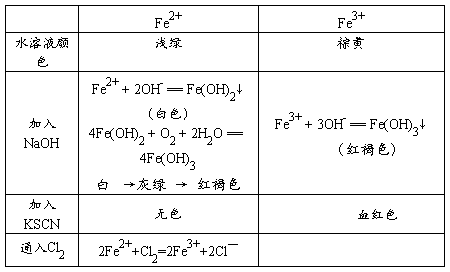
① Fe、Fe2+、Fe3+的相互转化
② Fe2+和Fe3+鉴别
第四章 非金属及其化合物
1. 硅及其化合物
⑴碳和硅的比较

第二篇:20xx年上学期高一化学实验教学总结
20##年上学期高一化学实验教学总结
桃源八中 彭宏云
20##年上学期在教务处、化学实验室的统一安排下,在高一全体化学教师的共同努力下,按照教学计划和新课标的要求,以素质教育的要求为出发点,全面提高学生的实验素质为目的,出色的完成了高一本期的化学实验教学任务。本期的化学实验教学工作,既取得了出色的成绩,也存在一些问题。现将本期实验教学工作总结如下:
一、加强了认识,落实了实验教学
化学是一门以实验为基础的学科,实验在化学教学中有着举足轻重的作用。对学生理解掌握化学基本概念、理论有着非常大的促进作用,同时也是现阶段素质教育的需要。因此,我们认真落实了实验的教学。
1、认真备好了课。学生分组实验先在课堂上认真地把将要做的实验的实验原理、注意事项告诉学生,让其理论上有充分的准备。
2学生在实验室进行实际操作的过程中,科任老师积极配合实验员,给予学生当场解决所发现的问题,使学生获益非浅
3、本期我们着重抓了对学生的化学实验重要性的教育,并且努力培养他们动手的积极性和动手能力,使一部分对化学实验不感兴趣的同学也参与到实验中来了。
二、本学期所开设完成的实验
按本学期的教学计划,高一年级共开设了四个学生分组实验和若干课堂演示实验,分组实验分别是:
实验一 同周期、同主族元素性质的递变规律
实验二 放热反应与吸热反应
实验三 化学反应速率与限度
实验四 乙酸乙酯的性质与制取
以上四个学生分组实验均在实验室由学生完成。另外,课本上的一些演示实验都随堂开设。通过实验教学,达到了实验教学的初步目的。
三、存在的问题
问题是存在的。主要还是体现在学生的基础素质差,高二全体化学教师通过一期的努力,不愿动手或害怕动手的学生减少,但依然大有人在。因此设法使学生认识化学实验的重要性以及培养他们动手的积极性,将是以后化学实验教学工作的重点,也是一个难点,这也是我在今后的实验教学中须长期注意的问题。
总之,实验课的开设是必须的、必要的。作为一所农村高中,我们要充分发挥学校现有的实验条件,积极地创造新的实验条件,通过化学实验的教学,充分调动学生的学习化学的兴趣和积极性,达到充分落实素质教育的目的。
20##-6-27
