电化学知识总结
一、原电池
1、二次电池(铅蓄电池)
负极:pb 正极: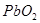 电解质溶液:
电解质溶液: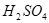
①放电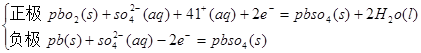
②充电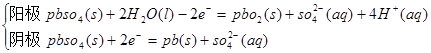
总反应 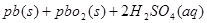

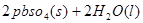
[练习]已知爱迪生蓄电池放电和充电时发生的总反应为:
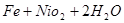

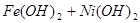
请分别写出该电池放电和充电时的电极反应式。
①放电
②充电
2、燃料电池
(1)氢氧燃料电池(负极: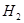 正极:
正极: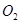 )
)
①酸性电解质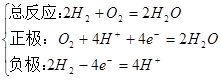
②碱性电解质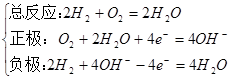
③中性电解质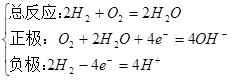
(2)甲烷燃料电池(负极: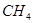 正极:
正极: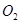 )
)
①酸性电解质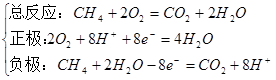
②碱性电解质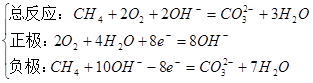
[练习]分别写出乙烷燃料电池在不同电解质溶液中的电极反应式。
①酸性电解质
②碱性电解质
③甲醇燃料电池(负极: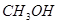 正极:
正极: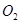 )
)
①酸性电解质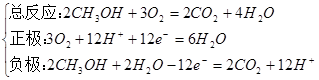
②碱性电解质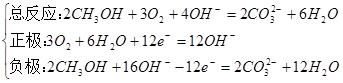
[练习]分别写出乙醇燃料电池在不同电解质溶液中的电极反应式。
①酸性电解质
②碱性电解质
4、熔融盐燃料电池(电解质:熔融的
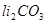 )(负极
)(负极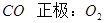 )
)
电池总反应: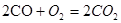
负极: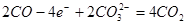
正极: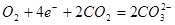
3、钢铁的腐蚀
(1)析氢腐蚀(酸性电解质)
负极: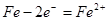 正极:
正极:
总反应:
(2)吸氧腐蚀
①中性电解质
负极: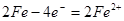
正极: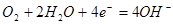
②碱性电解质(如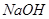 )
)
负极: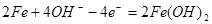
正极: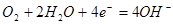
总反应: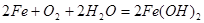
铁锈的形成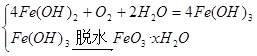
二、电解池(以下各电解均使用惰性电极)
1、电解水型
(1)含氧酸(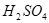 ) (2)可溶性强碱(
) (2)可溶性强碱(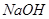 ) (3)活泼金属的含氧酸性(
) (3)活泼金属的含氧酸性(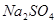 )
)
阳极: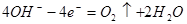
阴极:
总反应: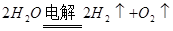
练习:1、电解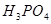
阳极
阴极
2、电解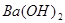 溶液
溶液
阳极
阴极
3、电解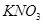 溶液
溶液
阳极
阴极
总反应
2、电解电解质型
(1)无氧酸(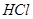 )
)
阳极: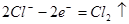
阴极: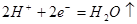
总反应: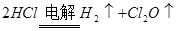
(2)不活泼金属的无氧酸盐(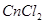 )
)
阳极: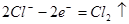
阴极: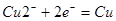
总反应: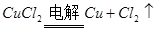
3、电解电解质和水型
(1)阴极放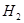 生碱型——活泼金属无氧酸盐(
生碱型——活泼金属无氧酸盐(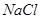 )
)
阳极: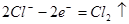
阴极: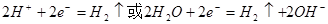
总反应: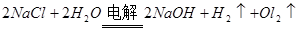
(2)阳极放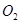 生酸型——不活泼金属含氧酸盐(
生酸型——不活泼金属含氧酸盐(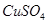 )
)
阳极: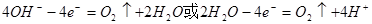
阴极: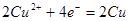
总反应: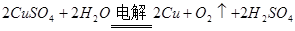
4、电解法制铝

阳极: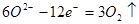
阴极:
5、电镀池(铁上镀铜)
阳极材料
电极反应式
阴极材料
电极反应式
6、铜的电解精炼(杂质、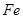 、
、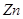 、
、 )
)
阳极材料
电极反应式
练习:
1、电解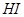 溶液 2、电解
溶液 2、电解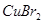
阳极 阳极
阴极 阴极
电解总反应 电解总反应
3、电解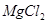 溶液 4、电解
溶液 4、电解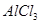 溶液
溶液
阳极 阳极
阴极 阴极
电解总反应 电解总反应
5、电解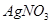 溶液
溶液
阳极
阴极
电解总反应
第二篇:电化学知识点总结
; 原 电
池 正极:用氧化性较强的物质正极,正极从外电路得到电子,发生还原反应。 原
理
失e-,沿导线传递,有电流产生 氧化反应 还原反应
Zn-2e-=Zn 2H++2e-=2H2↑
负极(锌筒)Zn-2e-=Zn2+
正极(石墨)2NH4++2e-=2NH3+H2↑
总反应:Zn+2NH4+=Zn2++2NH3+H2↑
电解质溶液:糊状的NH4Cl
;
。
PbO2) PbO2+SO42-+4H++2e-=PbSO4+2H2O
负极(Pb) Pb+SO42--2e-=PbSO4
PbO2+Pb+2H2SO4 2PbSO4+2H2O
电解液:1.25g/cm3~1.28g/cm3的H2SO4 溶液
蓄电池 特点:电压稳定。
Ni——Cd)可充电电池;
Cd+2NiO(OH)+2H2O Cd(OH)2+2Ni(OH)2
锂电池
不是把还原剂、氧化剂物质全部贮藏在电池内,而是工作时不断从外界输入,同时 燃料 电极反应产物不断排出电池。
电池 ②、原料:除氢气和氧气外,也可以是CH4、煤气、燃料、空气、氯气等氧化剂。
2H2+2OH--4e-=4H2O ;正极:O2+2H2O+4e-=4OH-
总反应:O2 +2H2 =2H2O
Hg2+)酸碱等物质;回收金属,防止污染。
放电` 化学电源简介
腐蚀危害:
腐蚀的本质:M-ne-→Mn+(氧化反应)
化学腐蚀(金属与接触到的物质直接发生化学反应而引起的腐蚀)、电化腐蚀
负极(Fe):Fe-2e-=Fe2+;正极(C):O2+2H2O+4e-=4OH- 金
属
的电化
总反应:2Fe+O2
+2H2O=Fe(OH)2
腐腐蚀 后继反应:4Fe(OH) +O +2HO =4Fe(OH) 2223蚀△与 2Fe(OH)3Fe2O3 +3H2O 防负极(Fe):Fe-2e-=Fe2+; 护
正极(C):2H++2e-=H2↑
总反应:Fe+2H+=Fe2++H2↑
定义:使电流通过电解质溶液而在阴阳两极引起氧化还原反应的过程。
装置特点:电能转化为化学能。
形成条件②、电解质溶液(或熔化的电解质)
阳极:与直流电源正极相连的叫阳极。
电概念 阴极:与直流电源负极相连的叫阴极。 解 池
原 理
离子放电顺序:阳极:阴离子还原性 S2->I->Br->Cl->OH->SO42-(含氧酸根)>F-
Ag+>Fe3+>Cu2+>Pb2+>Sn2+>Fe2+>Zn2+>H+>Al3+>Mg2+>Na+
氧化反应
--4e-=2H2O +O+2e-=Cu 电解结果:在两极上有新物质生成。
2CuSO4+2H2O 2Cu+2H2SO4+O2↑
CuSO4 (加一定量H2SO4)作电解液。
Cu2++2e
-
=Cu
阳极:Cu-2e-=Cu2+、Zn-2e-=Zn2+
Ni-2e-=Ni2+
阳极泥:含Ag、Au等贵重金属;
CuSO4浓度基本不变
③、原理:阳极 Cu-2e-=Cu2+ ;Cu2++2e-=Cu
④、装置:
(如图)
现象 KI变蓝;
原理: NaCl =Na++Cl- H2++OH-
Fe):Na+,H+移向阴极;2H++2e-=H2↑(还原反应)
C):Cl-、OH-移向阳极;2Cl--2e-=Cl2↑(氧化反应)
2NaCl +2H2O 2NaOH +Cl2↑+H2↑
氯碱
工业
;阴极:碳钢网(涂有Ni涂层) 电解 电解的应用
