选修三知识点
第一章 原子结构与性质
1能级与能层

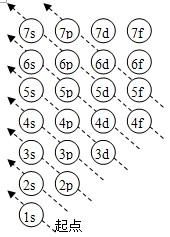
⑴构造原理:随着核电荷数递增,大多数元素的电中性基态原子的电子按右图顺序填入核外电子运动轨道(能级),叫做构造原理。
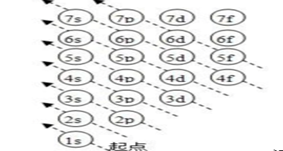
能级交错:由构造原理可知,电子先进入4s轨道,后进入3d轨道,这种现象叫能级交错。 说明:构造原理并不是说4s能级比3d能级能量低(实际上4s能级比3d能级能量高),而是指这样顺序填充电子可以使整个原子的能量最低。
(2)能量最低原理 现代物质结构理论证实,原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,简称能量最低原理。 构造原理和能量最低原理是从整体角度考虑原子的能量高低,而不局限于某个能级。
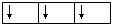
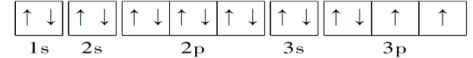
(3)泡利(不相容)原理:基态多电子原子中,一个轨道里最多只能容纳两个电子,且电旋方向相反(用“↑↓”表示),这个原理称为泡利(Pauli)原理。
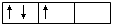
(4)洪特规则:当电子排布在同一能级的不同轨道(能量相同)时,总是优先单独占据一个轨道,而且自旋方向相同,这个规则叫洪特(Hund)规则
洪特规则特例:当p、d、f轨道填充的电子数为全空、半充满或全充满时,原子处于较稳定的状态。
4. 基态原子核外电子排布的表示方法
(1)电子排布式 ①用数字在能级符号的右上角表明该能级上排布的电子数,这就是电子排布式,例如K:1s22s22p63s23p64s1。
②为了避免电子排布式书写过于繁琐,把内层电子达到稀有气体元素原子结构的部分以相应稀有气体的元素符号外加方括号表示,例如K:[Ar]4s1。
③外围电子排布式(价电子排布式)
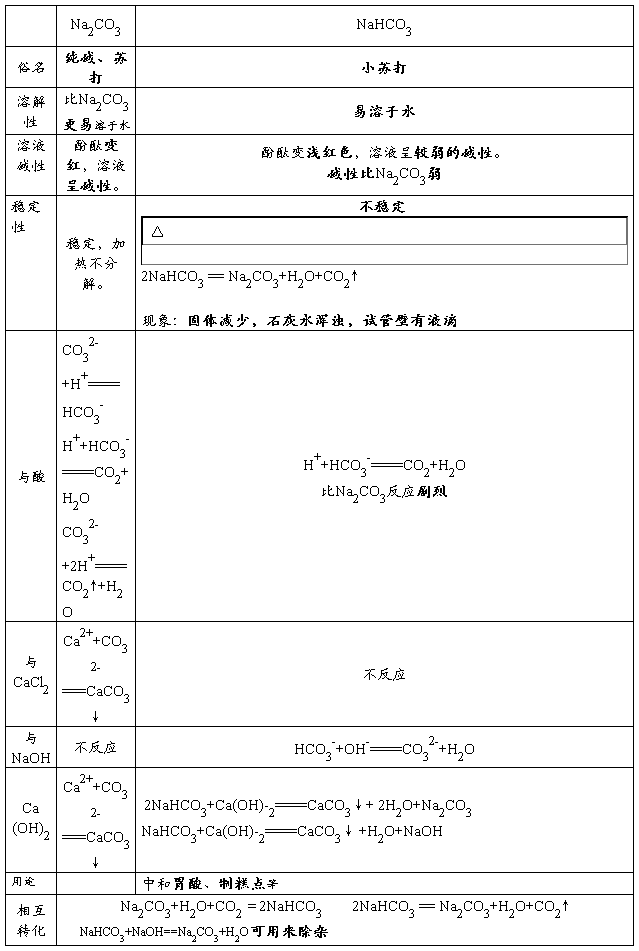
(2)电子排布图(轨道表示式)是指将过渡元素原子的电子排布式中符合上一周期稀有气体的原子的电子排布式的部分(原子实)或主族元素、0族元素的内层电子排布省略后剩下的式子。 每个方框或圆圈代表一个原子轨道,每个箭头代表一个电子。 如基态硫原子的轨道表示式为
…… …… 余下全文



 态原子的电子按右图顺序填入核外电子运动轨道(能级),叫做构造原理。
态原子的电子按右图顺序填入核外电子运动轨道(能级),叫做构造原理。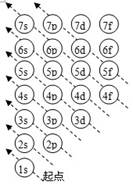
 也就是说,整个原子的能量不能机械地看做是各电子所处轨道的能量之和。
也就是说,整个原子的能量不能机械地看做是各电子所处轨道的能量之和。 低原理。
低原理。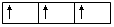
 或
或