高三化学期末考试分析
郭俊香
一、试卷评价
以教材为本,立足于《考试大纲》和考试说明,紧扣课本的基础知识,覆盖面广,突出学科的内部综合;注重考查学生对知识的运用能力、解题的规范性和思维的开放性;注重对化学实验的考查及实验操作的规范性,突出化学学科特点。特别重视从试题结构、难度、学生答题形式等方面紧密联系高考、模拟高考,体现高考对能力和素质的要求。
二、从学生答卷分析
1、选择题部分
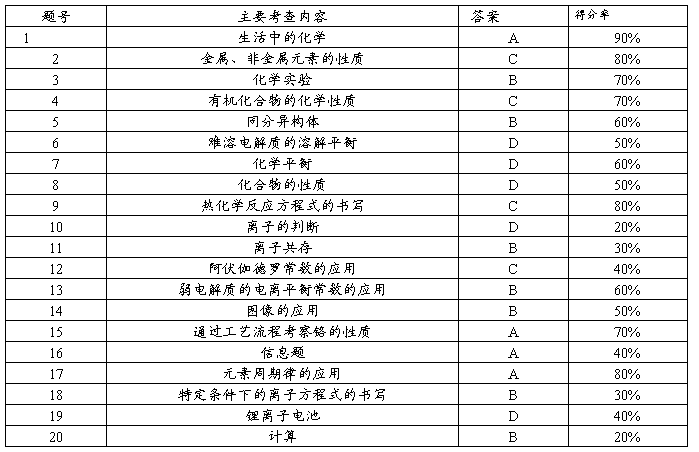
第Ⅰ卷选择题部分
2、非选择题部分
21、【考查目的】
检查学生外界条件对化学平衡的影响化学平衡图像、盖斯定理掌握情况。
【学生答题情况统计】

【学生答题中存在的问题】
1. △H计算结果不标单位。
2. 不能从图表中获取信息,从而得出正确的关系式。
3. 不能较好的应用化学用语进行简答或叙述。
【失分原因分析】
1. 盖斯定律的计算方法掌握不好,部分学生没有考虑“正”、“负”号,不标单位。
2. 对化学平衡图像的理解不到位,部分学生对其中点和线的意义不清楚,因而不能正确的关系式。
22、【考查目的】
检查学生对元素化合物性质、化学实验操作、离子方程式书写、Ksp应用、工艺流程图应用掌握情况。
【学生答题情况统计】

【学生答题中存在的问题】
1. 检验沉淀是否完全的叙述不完整或不准确,有些方法复杂。
2. 不能很好的根据图表数据、信息回答问题。
3. 不能很好的根据工艺流程图得出实验操作的步骤。
【失分原因分析】
(1)审题不清,思维定势。
(2)元素化合物性质不记忆用时想不起来。
(3)工艺流程图的有关训练少、流程图中的很多信息得不到理解的应用。
(4)不能较好的图表中获取有用的信息。
23、【考查目的】
检查学生有机化学实验的掌握情况。
【学生答题情况统计】

【学生答题中存在的问题】
1. 实验现象的原因的表述不清楚。
2. 实验操作的方法掌握不熟练。
【失分原因分析】
(1)此实验为课本实验的改造题,但错误率较高,充分暴露出实验复习的问题。
(2)此题失分较多的原因仍然体现在多数学生缺乏必要的化学实验知识。
(3)基本的实验操作能力较差,平时没做过或很少做实验。
(4)答题不规范失分较多。
(5)学生怕实验题、实验题得分较低。
24、【考查目的】
检查学生对元素化合物性质、氧化还原知识和应用、离子方程式书写掌握情况。
【学生答题情况统计】

【学生答题中存在的问题】
1. 利用平衡移动原理解释实验现象的能力差。
2. 不会根据元素化合价的变化书写氧化还原反应方程式,特别是生成物的判断存在很大问题,而此点刚好是高考的常考点。
3.计算能力差。
【失分原因分析】
1. 氧化还原反应计算方法掌握不好,失分较多,说明部分学生不能很好的从化合价的变化认识元素化合物性质,没有掌握此类计算的关键。
2. 已知条件、陌生氧化还原反应方程式的书写是高考重点考查的一个点,从学生的答题情况看,多数学生不会从题中所给的化合价变化确定产物,此空的得分率极低。
三、纵向比较
我校三个班级最高分69分,是一班的张晓鸽,一班60分以上5人,平均分 47.6;二班60分以上2人,平均分37.9;三班60分以上1人,平均分 33.2。和一练相比,虽然最高分没有一练的高,但是整体来看,化学成绩比一练有所提高。
四、今后的整改措施
1. 抓好基础,,落实知识点必记
基础仍然是学生获取高分数的前提,一方面要强调基础知识,熟悉课本内容;另一方面课堂与训练中要给学生强调解决问题的基本方法,尽可能地帮助学生建立化学经典的模型,让学生在考试中能准确联想到模型,以致考试时有依靠,充分发挥出学生的水平。
2. 认真查漏补缺
认真分析学生卷面情况和回顾一轮复习以来教学中存在的问题,力争下阶段的教学能更有实效性。
3. 重视解题后的反思与知识、方法的归纳整理,提高讲评实效
有的相似的题目已经做过了,但学生仍然不会,这种现象更要引起我们注意,高三学生所做的习题不可谓不多,但如何减少盲目做题,让学生多想题,多反思,多积淀,这样才能升华,思维能力才能提高。
教师在复习中要重视“讲与练、练与评、评与纠、纠与导”的结合。要清楚做题的关键不在于“多”,而在于“到位”,即做一题得一题,努力要求学生答的都达到“标准答案”的规格。在于及时“反思”,不能做题不少,想题不多,没有反思,没有积淀,没有升毕,这是高考失败的原因之一。因此,要重视解题后反思,即对解题活动的反思,主要包括:
(1)对试题涉及的知识点和题设陷阱的反思 (2)对所用解题方法的反思
(3)对解题规律的反思 (4)对解题失误的反思
4. 关注学生的学习状况,提升学生信心
我们发现学生在答题时遇到计算放弃的多,这种现象要通过平时的教学引导加以纠正,其实本次考试涉及的计算也不难,只要学生能有正常的心态对待得分也不是困难的事。
5. 重视解题规范,提高学生的应试能力
应试能力包括解题策略、规范性、速度、准确性、完整性。本次考试不少学生因解题不规范导致较多的无谓失分,这都是因为平时规范化训练不够造成。回答问题时更要注意关键词的描述到位。
6.加强化学实验教学,培养学生的动手能力
第二篇:北京市西城区20xx届高三第一学期期末考试(化学)
北京市西城区2010 — 2011学年度第一学期期末试卷
高三化学 2011.1
试卷满分100分,考试时间120分钟。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Fe 56
第Ⅰ卷(选择题 共42分)
每小题只有1个选项符合题意。
1.下列说法不正确的是 ...
A.维生素是参与生物生长发育和新陈代谢所必需的一类有机化合物
B.糖类、油脂、蛋白质、维生素、无机盐和水是人体所需的营养素
C.阿司匹林是一种人工合成药物,具有解热镇痛等作用
D.合成纤维和光导纤维都是新型的无机非金属材料
2.下列金属的冶炼方法与钠相同的是
A.银 B.铝 C.铁 D.铜
3.下列物质中,既含有离子键又含有极性共价键的是
A.Na2O2 B.MgCl2 C.HCl D.NH4Cl
4.下列顺序表述正确的是
A.酸性:H3PO4 > HNO3 > HClO4 B.稳定性:H2O > HF > H2S
C.原子半径:Na > Mg > O D.还原性:F> Cl> S2 ---
5.下列现象与电化学腐蚀无关的是 ..
A.生铁比纯铁易生锈 B.纯银饰品久置表面变暗 C.黄铜(铜锌合金)制品不易产生铜绿 D.与铜管连接的铁管易生锈
6.下列说法正确的是
A.少量金属Na应保存在水中 B.用萃取的方法可除去水中的Cl离子 C.Na2SiO3溶液应保存在带玻璃塞的试剂瓶中 D.用向沸水中滴加FeCl3饱和溶液的方法可制Fe(OH)3胶体 -
7.实验室常用NaNO2和NH4Cl反应制取N2。下列有关说法正确的是
A.NaNO2是还原剂 B.NH4Cl中N元素被还原
C.生成1 mol N2时转移6 mol 电子 D.氧化剂和还原剂的物质的量之比是1︰1
8.下列说法正确的是
A.若发生A2+ 2D=2A+ D2反应,则氧化性D2>A2
B.若X原子的质子数是a,中子数是b,则该核素可表示为 b
a--X
- 1 -

C.若相同温度和浓度的两种钠盐溶液的碱性NaA<NaB,则酸性HA>HB
D.若主族元素的简单离子R 2 和M+的电子层结构相同,则原子序数R>M -
9.下列实验操作正确的是
A.用饱和溴水除去甲苯中混有的苯酚 B.用氨水洗涤除去试管内壁上的银镜
C.实验室用加热NH4Cl固体使之分解的方法制NH3
D.用稀硫酸和Zn反应制H2时,加少量CuSO4溶液可加快反应速率
10.已知:乙醇可被强氧化剂氧化为乙酸。
2 2 COOH ,发生反应的类型依次是 2 可经三步反应制取 Br Br Cl
A.水解反应、加成反应、氧化反应 B.加成反应、水解反应、氧化反应
C.水解反应、氧化反应、加成反应 D.加成反应、氧化反应、水解反应
11.在下列溶液中,一定能大量共存的一组离子是
A.溶液的pH=13:ClO、HCO3、Na+、 Mg2+ B.溶液中含有大量NO3:NH4+、I、-??-
+?SO2
4、H
C.溶液中c(HCO3)=0.1 mol/L :Na+、K+、CO3、Br?2?-
--D.溶液中由水电离出的c(H+)=1×10
-13 mol/L :Na+、H+、Cl、Br
12.将AgCl分别加入盛有:①5 mL水;② 6 mL 0.5 mol/L NaCl溶液;
③10 mL 0.2 mol/L CaCl2溶液;④50 mL 0.1 mol/L 盐酸的烧杯中,均有固体剩余,各溶液中c(Ag+)从大到小的顺序排列正确的是
A.④③②① B.②③④① C.①④③② D.①③②④
13.NA表示阿伏加德罗常数。下列说法正确的是
A.7.8 g Na2O2中含有的阴离子数目为0.2 NA B.标准状况下,2.24 L CHCl3的分子数为0.1 NA
C.1 L 0.1 mol/L Al2(SO4)3溶液中,Al3+的数目为0.2 NA
D.9.2 g NO2和N2O4的混合气中含有的氮原子数为0.2 NA
14.某原电池装置如右图所示。下列有关叙述中,正确的是
+ -
D.工作一段时间后,NaCl溶液中c(Cl)增大
15.下列离子方程式书写正确的是
A.铝片放入NaOH溶液中:2Al + 2OH= 2AlO2 + H2↑ --?
B.碳酸钙溶于醋酸中:CaCO3 + 2H+= Ca2+ + CO2↑+ H2O
C.氯气通入NaOH稀溶液中:Cl2 + 2OH= Cl+ ClO+ H2O
2+ ?D.Ba(OH)2溶液与过量NaHSO4溶液混合:H+ + SO2+ OH= BaSO4↓+ H2O 4+ Ba----
16.已知Ca(OH)2的溶解度随温度升高而降低。将某温度下饱和澄清石灰水①加入少量生石灰
后恢复到原来温度;②降低温度。这两种情况下,前后均保持不变的是
A.溶液的质量 B.Ca(OH)2的溶解度
C.溶液中Ca2+离子的数目 D.溶液中溶质的质量分数
17.将4 mol A和2 mol B放入2 L密闭容器中发生反应2A(g) + B(g) 2C(g) ΔH<0。
4 s后反应达到平衡状态,此时测得C的浓度为0.6 mol/L。下列说法正确的是
A.4 s内,υ(B)=0.075 mol/(L ·s)
B.当c(A)︰c(B)︰c(C)=2︰1︰2 时,该反应即达到平衡状态
C.达到平衡状态后,若只升高温度,则C的物质的量浓度增大
D.达到平衡状态后,若温度不变,缩小容器的体积,则A的转化率降低
第Ⅱ卷(非选择题 共58分)
18.(4分)常温下,有浓度均为0.1 mol/L的4种溶液:①盐酸;②硫酸;③醋酸;
④氢氧化钡。(注:忽略溶液混合时体积的变化)
(1)将上述溶液两两等体积混合后,溶液pH=7的组合有(填序号) 。
(2)醋酸钡是易溶于水的强电解质。将③与④等体积混合,所得溶液中离子浓度由大到
小的顺序是 。
19.(6分)氢气是一种清洁能源。用甲烷制取氢气的两步反应的能量变化如下图所示:


- 3 -
(1)甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是 。
(2)第II步为可逆反应。在800℃时,若CO的起始浓度为2.0 mol/L,水蒸气的起始
浓度为3.0 mol/L,达到化学平衡状态后,测得CO2的浓度为1.2 mol/L,则此反 应的平衡常数为 ,CO的平衡转化率为 。
20.(6分)现有3种化合物A、B、C均含短周期元素R,其转化关系如下图所示。 A X B X C
(1)若A由第三周期2种元素组成。常温下,0.1 mol/L X溶液的pH=13,则R在周
期表中的位置是 ,X中阴离子的电子式是 ,B转化为 C的离子方程式是。
(2) 若常温下A、B、C、X均为气态物质,1 mol A中含有共价键的数目约为1.806×1024,
X为单质,A与X反应生成B的化学方程式是;在一定条件下,
A可与C反应消除C对大气的污染,该反应的化学方程式是。
21.(12分)以食盐为原料进行生产并综合利用的某些过程如下图所示。
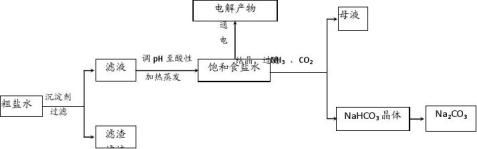
?(1)除去粗盐中的Ca2+、Mg2+和SO2 4离子,加入下列沉淀剂的顺序是(填序号) 。
a.Na2CO3 b.NaOH c.BaCl2
(2)将滤液的pH调至酸性除去的离子是 。
(3)电解饱和食盐水反应的离子方程式是 。
(4)若向分离出NaHCO3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的
物质,其化学式是 。
(5)纯碱在生产生活中有广泛的应用。
① 纯碱可用于除灶台油污。其原因是(结合离子方程式表述) 。 - 4 -
② 常温下,向某pH=11的Na2CO3溶液中加入过量石灰乳,过滤后所得溶液pH=13。
则反应前的溶液中与反应后的滤液中水电离出的c(OH)的比值是 —
③ 工业上,可以用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与Cl2反应制
取有效成分为NaClO的消毒液,其反应的离子方程式是 。(已知碳酸的酸性强于次氯酸)。
22.(8分)兴趣小组通过实验探究溶解铜的方法和本质。
(1)在热水浴中进行3个实验,部分实验报告如下表所示。
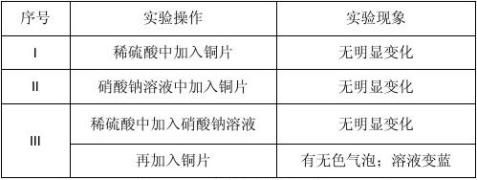
① 实验I、II的目的是 。
② 实验III中反应的本质是(用离子方程式表示) 。
(2)利用电化学原理实现铜溶于稀硫酸并生成氢气。
① Cu作 极。 ② 总反应的离子方程式是 。
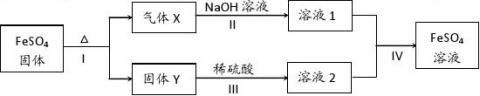
23.(8分)有关FeSO4的转化关系如下图所示(无关物质已略去)。
已知:① X由两种化合物组成,将X通入品红溶液,溶液褪色;通入BaCl2溶液,
产生白色沉淀。
② Y是红棕色的化合物。
(1)气体X的成分是(填化学式) 。
(2)反应I的反应类型属于(填序号) 。
a.分解反应 b.复分解反应 c.置换反应 d.化合反应
e.氧化还原反应
(3)溶液2中金属阳离子的检验方法是 。
(4)若经反应I得到16 g固体Y,产生的气体X恰好被0.4 L 1 mol/L NaOH溶液完全吸收, - 5 -
则反应IV中生成FeSO4的离子方程式是 。
24.(14分)某研究小组设计用含氯的有机物A合成棉织物免烫抗皱整理剂M的路线如下(部分反应试剂和条件未注明):

已知:
① E的分子式为C5H8O4,能发生水解反应,核磁共振氢谱显示E分子内有2种不同环
境的氢原子,其个数比为3︰1。
② ROOCCH2COOR′ + CH2=CHCOOR″ 乙醇钠 ROOC——COOR′
2CH2COOR″ (R、R′、R″代表相同或不相同的烃基)
(1)A分子中的含氧官能团的名称是 。
(2)D→E反应的化学方程式是 。
(3)A→B反应所需的试剂是 。
(4)G→H反应的化学方程式是
(5)已知1 mol E 与2 mol J 反应生成1 mol M,则M的结构简式是 (6)E的同分异构体有下列性质:①能与NaHCO3反应生成CO2;②能发生水解反应,且水
解产物之一能发生银镜反应,则该同分异构体共有 种,其中任意1种的结构简式是 。
(7)J 可合成高分子化合物,该高分子化合物结构简式是 。
- 6 -
北京市西城区2010 — 2011学年度第一学期期末试卷
高三化学参考答案及评分标准
第Ⅰ卷(选择题 共42分)
1~9小题,每小题2分;10~17小题,每小题3分。
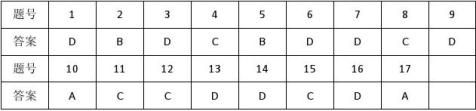
第Ⅱ卷(非选择题 共58分)
说明:其他合理答案均可给分。 18.(4分) (1)(2分)②和④
——
(2)(2分)c(OH)>c(Ba2+)>c(CH3COO)>c(H+) 19.(6分) (1)(2分)CH4(g) + 2H2O(g) = 4H2(g) + CO2(g) ΔH=—136.5 kJ/mol (2)(2分) 1 (2分)60 % 20.(6分) (1)(1分)第三周期IIIA族 (1分)
--
(1分)Al(OH)3 + OH = AlO2 + 2H2O (2)(1分)4NH3 + 5O2 4NO + 6H2O
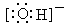
一定条件
(2分)8NH3 + 6NO2 7N2 + 12H2O
21.(12分) (1)(1分)c a b 或者 c b a或者b c a (2)(1分)CO3和OH (3)(2分)2Cl+ 2H2O (4)(2分)NH3
2?-
2?—
电解
2OH+ H2↑ + Cl2↑
2?
-
(5)①(2分)CO3水解显碱性CO3+ H2O下水解,达到去污目的。 ②(2分)1×1010
HCO3+ OH,油污在碱性条件
?—
③(2分)2CO3+ Cl2 + H2O = Cl + ClO + 2HCO3
2?
—
—
?
22.(8分)
(1)①(2分)证明Cu不与H+、NO3单独反应
?
- 7 -
②(2分)3Cu + 8H++ 2NO3=3Cu2+ + 2NO↑+ 4H2O ?
(2)①(2分)阳 ②(2分)Cu + 2H+
23.(8分)
(1)(2分)SO2、SO3
(2)(2分)a、e 电解 Cu2+ + H2↑
(3)(2分)取少量溶液2于试管中,滴加几滴KSCN溶液,溶液变红,则证明原溶液中含
有Fe3+。
(4)(2分)2Fe3+ + SO3+ H2O =2Fe2++SO4+ 2H+ 2?2?
24.(14分)
(1)(1分)羟基 浓硫酸 (2)(2分)HOOCCH2COOH + 2CH3OH CH3OOCCH2COOCH3 + 2H2O △ (3)(1分)NaOH水溶液 醇(4)(2分)ClCH2CH2COOH +2NaOH 2=CHCOONa + NaCl+ 2H2O △2CH2COOCH3 (5)(2分)
CH3OOCC COOCH3
2CH2COOCH3 (6)(2分)5
(2分)写出以下任意1种即可:
3
或 HCOOCH2 COOH HCOOCH2CH2CH2COOH
3 3
或 2 CH3 或 2 COOH
(7)(2分) CH
3 或 COOH 3
- 8 -
