硫酸亚铁铵制备实验的改进
摘要
对硫酸亚铁铵的制备实验进行了改进。减少空气含氧量、加酸抑制Fe2+氧化,改进减压过滤装置进行趁热过滤,并以硫酸量计算反应的铁量,硫酸亚铁铵产率可达76.82%,产率较高。
关键词:硫酸亚铁铵的制备
引言
为了更好的了解复盐的特性和产率的计算,在无机化学实验中设置了硫酸亚铁铵的制备实验。通常,有Fe2+参与的反应要考虑防止Fe2+的氧化,一般加过量铁粉起还原作用,但此实验有滤掉铁粉、加热的过程,导致Fe2+易被氧化,使产品纯度偏低。实验室实验装置不能满足趁热过滤,使产品产量偏低。由于空气的快速氧化,利用铁粉剩余质量计算反应质量造成数据误差。
通过对制备实验的分析,我们对制备硫酸亚铁铵的步骤进行了改进,从防氧化、防结晶、更准确处理数据的方面进行条件优化,较高产率的制备出硫酸亚铁铵。
1实验部分
1.1实验试剂
铁屑,碳酸钠溶液,硫酸,硫酸铵,乙醇,硫氰酸钾。
1.2实验仪器
电子天平,烧杯,玻璃棒,电磁炉,布氏漏斗,抽滤瓶,量筒,滴管,蒸发皿,玻璃皿。
1.3实验方法
称取5.6g铁屑,加40mlNa2CO3洗涤。通风处内向净化后的铁屑加10mL 3mol/L的H2SO4,水浴加热,添蒸馏水保持体积,加1mLH2SO4,反应结束后趁热过滤,滤液转移至蒸发皿。称取4.6g(NH4)2SO4加入滤液溶解完全,水浴加热至有结晶膜,冷却,减压过滤,用乙醇洗涤,晾干,称重,计算产率。反应原理如下:
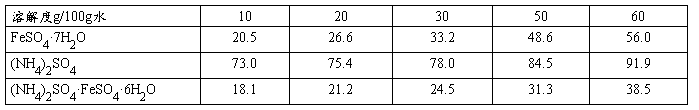

0到60oC, (NH4)2SO4·FeSO4·6H2O在水中的溶解度比组成它的每一组分的溶解度都小。
FeSO4+(NH4)2SO4+6H2O═(NH4)2SO4·FeSO4·6H2O
2讨论

 2.1提高亚铁盐纯度
2.1提高亚铁盐纯度
未经改进的实验,对亚铁盐进行直接加热,防止Fe2+被氧化的措施是加入过量的铁粉。
但直接加热温度过高,高温下Fe2容易迅速被氧化,因此将原实验中直接加热改为水域加热,保持温度在60oC-70oC。加热过/程中,取铁粉和H2SO4于4个小烧杯,放置在反应烧杯周围,以产生的H2减少02浓度。
并且,原实验未考虑Fe2的水解,因为酸性条件抑制Fe2水解,且根据铁的E-pH图Fe2在酸性条件下更稳定不易被氧化,所以改进实验中,Fe与H2SO4接近完全反应时再加1mLH2SO4。
2.2趁热过滤的处理
由于没有热滤漏斗,实验室采用快速减压过滤。
但是,烤箱烘烤过的布氏漏斗和滤瓶降温迅速,FeSO4容易在滤液中析出,不能与滤液一起被转移。
改进实验增加步骤,烘烤后,用热毛巾捂住滤瓶,过滤后取少量温水于滤瓶,使FeSO4重新溶解,倒入滤液。
2.3铁粉用量的计算方法对实验数据的影响
未经改进的实验,在铁屑净化、趁热过滤后对铁粉进行两次称重,计算Δm作为参加反应的铁粉的量。
但考虑到趁热过滤时,未反应的铁粉在高温下与空气、水充分接触很容易被氧化成Fe2O3(参考实验现象:布氏漏斗重铁粉约60%变成红褐色,取变色铁粉溶于酸未产生气泡,加KSCN变血红色)从而影响称量结果。并且,将剩余铁粉移出布氏漏斗很容易造成损失,造成数据误差。
改进实验,使铁粉与H2SO4充分反映,依据H2SO4用量求参与反映的铁粉质量,从而避免
 误差。
误差。
2.4数据分析
理论产量 m0=(10+1)*10-3*3*392=12.94g
实际产量 m=9.94g
产率 m/m0=9.94/12.94*100%=76.82%
3.结论
本实验围绕防止亚铁盐被氧化、防止趁热过滤晶体析出进行一系列小的操作上的改进措施,并以H2SO4用量计算反应铁粉量,计算得(NH4)2SO4·FeSO4·6H2O产率为76.82%。此实验摩尔盐一般产率为50%-80%,本次实际的产率较高,表明改进步骤效果良好。
第二篇:硫酸亚铁铵制备实验的两点改进

