实验 钡盐中钡含量的测定及中间过程残留离子鉴定
沉淀重量法:加入适量的沉淀剂使被测组分沉淀出来,后转化为称量形式,求得被测组分的含量。
要求:①沉淀的溶解度要小;②沉淀易于过滤和洗涤;③沉淀要纯净,没沉淀剂和杂质,易转变为称量形式;;④称量形式要具有确定的化学组成;⑤足够的稳定性;⑥比较大的摩尔质量
一 实验原理
Ba2+能生成BaCO3,BaCrO4,BaSO4,BaC2O4等一系列难容化合物,其中BaSO4的溶解度最小(Ksp=1.1x10-10),其组成与化学式符合,摩尔质量较大,性质稳定,符合重量分析对沉淀的要求。因此通常与BaSO4沉淀形式和称量形式测定Ba2+。为获得颗粒较大和纯净的BaSO4晶体沉淀,试样溶于水后;加HCl酸化,SO42+ + H+=HSO4-,以降低溶液的相对过饱和度,同时可防止其他的弱酸盐生成。加热近沸,在不断搅动下缓慢地加适当过量的沉淀剂稀H2SO4形成的BaSO4沉淀颈陈化,过滤,洗涤,灼烧后,以BaSO4形式称量,即可求得试样中Ba的含量。
二 仪器和试剂
瓷坩埚,漏斗,马弗炉,定量滤纸,BaCl2●2H2O,HCl溶液2mol/L,H2SO4溶液1mol/L,AgNO3溶液0.1mol/L。
三
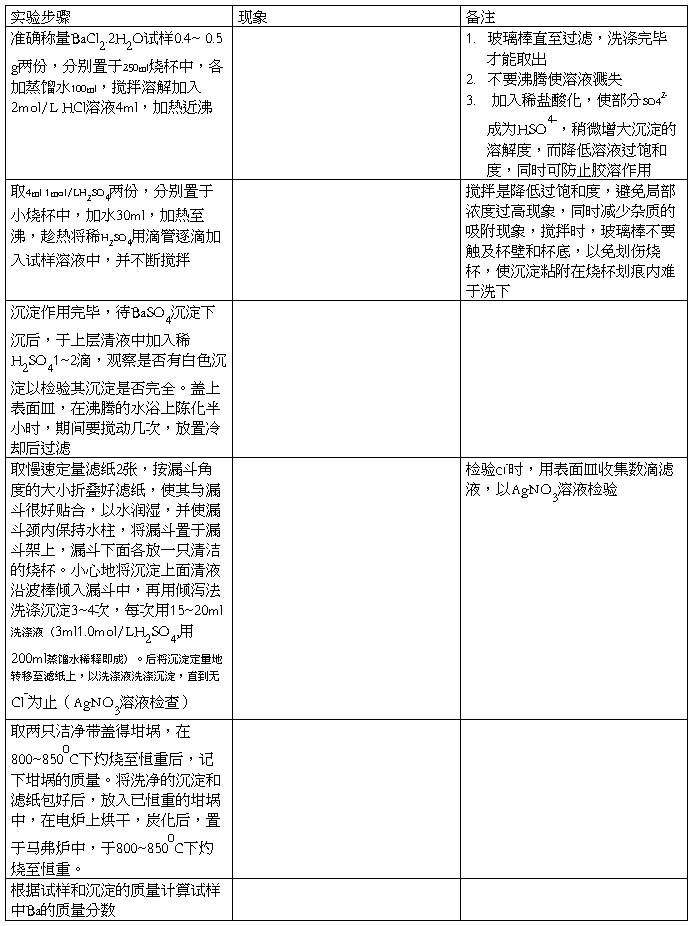
四 注意事项
测定误差主要来源沉淀的溶解损失,粘污和称量。玻璃棒不断搅拌的目的是防止沉淀附在玻璃棒上,洗涤沉淀时,少量多次,是减少沉淀量的损失。
五 数据记录
第二篇:钡盐中钡含量的测定
钡盐中钡含量的测定
(沉淀重量法)
一、实验目的
1. 熟悉晶形沉淀条件及方法;
2.掌握沉淀的过滤、洗涤和灼烧等基本操作;
3. 测定氯化钡中钡含量。
二、仪器与试剂
分析天平;长颈漏斗;玻璃棒;烧杯;滴管;电炉;瓷坩埚;马福炉;干燥器;定量滤纸等。
BaCl2·2H2O试样;HCl(2mol·L-1);
H2SO4(1mol·L-1);AgNO3(1mol·L-1)。
三、实验原理
1.Ba2+能生成一系列难溶化合物,如BaCO3、BaC2O4、BaCrO4和BaSO4等,其中以BaSO4的溶解度最小(Ksp=1.1×10-10),且很稳定,其组成与化学式相符,符合重量分析对沉淀的要求。
2.BaSO4是典型的晶形沉淀,因此应完全按照晶形沉淀的处理方法,将所得沉淀经陈化后,过滤、洗涤、干燥和灼烧,最后以硫酸钡沉淀形式称量,求得试样中Ba2+的含量。
3.可溶性硫酸盐试样溶于水中,用稀盐酸酸化,加热近沸并在不断搅拌的情况下,缓慢地加入热的沉淀剂—稀H2SO4溶液,使生成难溶性硫酸钡沉淀。
4.反应式:Ba2+ + SO42- = BaSO4↓(白)
四、实验步骤
1.称样及沉淀的制备
准确称取 BaCl2. 2H2O 试样 0.4~0.5 g,置于250mL烧杯中,加100 mL水搅拌溶解。加入 4mL
2 mol·L-1HCl,加热近沸。
取4mL l mol·L-1 H2SO4于100mL烧杯中,加水30mL,加热至近沸。趁热将稀 H2SO4用滴管逐滴
加入至试样溶液中。沉淀作用完毕,待BaSO4沉淀下沉后,于上层清夜中加入稀H2SO41~2滴检验沉淀是否完全。沉淀完全后,盖上表面皿,放在沸水浴上,经常搅拌并保温陈化30min,冷却后过滤。
2.沉淀的过滤和洗涤
用慢速定量滤纸进行倾泻法过滤,用稀 H2SO4溶 液(3mL 1 mol·L 的H2SO4,用200mL水稀释既成)在烧杯中洗涤沉淀3~4次,然后,小心将沉淀定量转移到滤纸上,用洗涤液洗涤漏斗中的沉淀及滤纸直到无Cl-1为止。
3. 空坩埚的恒重
将两个洁净带盖的瓷坩埚放在 800~850 ℃的高温炉中灼烧至恒重。第一次灼烧恒温时间40min,第 二次及以后每次只需灼烧20min。前后两次称量的差值<0.4mg,即为恒重。
4.沉淀的灼烧和恒重
将包叠好沉淀的滤纸包置于已恒重的瓷坩埚中,经烘干、炭化、灰化后,放入800℃的马弗炉中灼烧至恒重。
根据试样和沉淀的质量计算试样重Ba的质量分数。
五、数据记录与处理
