唾液淀粉酶最适pH值的测定实验
摘要:目的:掌握测量pH对酶活力影响的基本原理和方法,熟悉缓冲溶液的配置,722分光光度计的使用。方法:温度、酶浓度相同的条件下,酶的活力在最适pH处达到最大,远离则变小。测定碘液与淀粉的不同程度水解的产物反应后的吸光度。取处于升高与降低趋势之间的较小吸光度范围对应的pH值即为唾液淀粉酶的最适pH。结果:pH=6.8左右,吸光值最低。结论:测出唾液淀粉酶的最适PH值,约为6.8。 关键词:淀粉酶 pH 吸光度
前言:酶量与酶活性的改变都会引起代谢的异常乃至生命活动的停止。由于酶的独特的催化功能,使它在工、农业和医疗卫生等领域具有重大实用意义。酶的高效性和专一性,及其不需要在高温、强酸、强碱条件下作用的特点是普遍化学催化反应所无法比拟的。其研究成果给催化理论、催化剂的设计、药物的设计和作用原理的了解、疾病的诊断和治疗以及遗传和变异等方面提供了理论的依据和新的概念。
实验目的:
1.掌握设计性实验的基本思路,并完成设计报告。
2.掌握唾液淀粉酶最适PH的测定原理和方法。
3.熟悉影响酶促反应速度的因素。
实验原理:
1.酶促反应速度受到许多因素的影响,如温度、PH、激动剂和抑制剂等。上述诸因素对唾液淀粉酶催化淀粉水解反应速度的影响,可用定性或定量的反应来观察。利用碘与淀粉机器不同程度纾解产物反应的颜色,来衡量酶促反应的速度的快慢。蓝色—紫红色—黄色,颜色由蓝变黄,表示酶促反应速度由慢到快。此为定性观察。
2.进一步利用郎伯—比尔定律来判定溶液的吸光度与溶液的浓度符合一定的比例关系。由于在被水解的程度也不一样。当唾液淀粉酶不能将完全水解时,淀粉遇碘呈蓝色,吸收波长位于660nm处。不同PH环境中唾液淀粉酶与淀粉的反应程度不同,吸光度值也不同。因此,通过测量660nm处的吸光度值,可以了解PH对酶促反应的影响,吸光度最小的溶液其PH即为唾液淀粉酶的最适PH。
仪器材料和试剂药品:
仪器材料:中试管,毛刷,吸耳球,玻璃笔,小烧杯,坐标纸,漱口杯。0.1ml、0.5ml、1.0ml、2.0ml、5.0ml、10.0ml刻度吸管,胶头滴管,37 C恒温水浴箱,分光光度计,。
试剂药品: 淀粉溶液. 0.2mol/L磷酸二氢钠溶液、0.2mol/L磷酸氢二钠溶液 、 碘液,唾液。
实验步骤:
1、 缓冲液的配置:根据下表1,取10支试管进行编号1-10,配置各个pH值的缓冲溶液各10ml,PH
表1 用量(ml) 编号 1 2 3 4 5 PH 6.0 6.2 6.4 6.6 6.8 0.2mol/L
0.62 0.93 1.33 1.88 2.45
NaHPO4 0.2mol/L NaH2PO4 蒸馏水
编号 PH
0.2mol/L NaHPO4 0.2mol/L NaH2PO4
4.38
4.07
3.67
3.12
2.55
5.00 5.00 5.00 5.00 5.00
6 7.0 3.05 7 7.2 3.60 8 7.4 4.05 9 7.6 4.35 10 7.8
4.58
1.95 1.40 0.95 0.65
0.42
蒸馏水 5.00 5.00 5.00 5.00 5.00
2、唾液的获取:[2]
a.吐取法:蒸馏水漱口,然后用舌尖抵住上额或下额齿根后,微低头.轻启双唇,将下嘴唇搁在烧杯边缘,让唾液自然流入试管中.
b.实验者先把痰咳尽,用蒸馏水漱口,清除口腔内的食物残渣,再在口腔内含蒸馏水,并作漱口运动,3分钟后吐入垫有两层经润湿过处理的脱脂纱布漏斗里,过滤于小烧杯备用。
c.酸刺激法将。滴于舌前部,每次4滴,尝试者将舌头后卷,分泌的唾液用吐取法收集,一般测试5分钟。
3、唾液的稀释:
取8支试管,分别编上号1~8
管号 1 2 3 4 5 6 唾液 1.00 1.00 1.00 1.00 1.00 1.00 蒸馏水 2.00 4.00 6.00 8.00 10.00 12.00
4、唾液稀释倍数的选取
另取8支试管,分别编上1~8号,各取上述稀释的唾液各1ml,分别加入相应编号的试管里,向8支试管内同时加入1ml的0.02%的淀粉溶液,振荡混匀后放入37 C恒温水浴5分钟后取出,滴加1~2碘液,振荡混匀,观察颜色,选取颜色变化适中的一支,记录稀释倍数。
根据颜色适中判断,可以得出最适的唾液稀释倍数为4号试管。
5、底物用量的确定 用量(ml)
试剂 PH7.0缓冲液 淀粉(2.5g/L) E(最适稀释倍数)
碘液(滴) 蒸馏水 颜色
1 0.9 0.1 0.1 混匀,37°C
1 5 蓝色+
2 0.8 0.2 0.1 水浴,7.5min
1 5 蓝色+
3 0.7 0.3 0.1 1 5 蓝色++
1 5 蓝色+++
1 5 蓝色+
4 0.6 0.4 0.1
空白 0.5 0.1
用量(ml) 7 8 1.00 1.00 14.00 16.00
根据颜色适中判断,可以得出最适的淀粉底物用量为0.3ml。 6、测量pH: 取10支试管,分别标上号1~10,按下表操作
经“5、底物用量的确定 ”可以确定底物的用量为0.3ml,经“4、唾液稀释倍数的选取” 可以得出最适的唾液稀释倍数为4号试管。
用量(ml) 管 号 1 2 3 4 5 0.02%淀粉溶液 0.3 0.3 0.3 0.3 0.3 2ml缓冲溶液pH 6 6.2 6.4 6.6 6.8 (保温10min) 37 摄氏度
稀释唾液 1 1 1 1 1
0.02%淀粉溶液 0.3 0.3 2ml缓冲溶液pH 7 7.2
(保温10min) 37 摄氏度
稀释唾液 1 1
0.3 7.4 0.3 7.6
0.3 7.8
1 1 1

以pH值为横坐标,吸光度A为纵坐标,在坐标纸上作出平滑曲线,取曲线最低点对应的pH值,即为唾液淀粉酶的最适pH值。
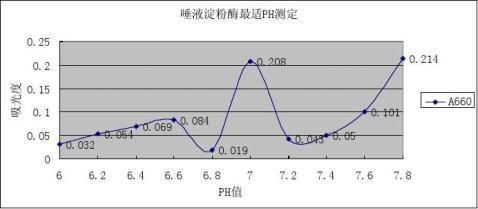
实验结论:根据实验数据做出的平滑曲线图可知,结果测得pH值在6.0~7.8范围内
并且随着pH的增大先减小后增大,pH=6.8左右,吸光度值最低。最低点对应的pH=6.8即为唾液淀粉酶的最适pH值。
分析讨论:
(1)此次实验是根据唾液淀粉酶催化底物水解量来测最适pH值,因此在唾液淀粉酶活性最高时要保证底物过量,淀粉分解的越多,A值就小;
(2)滴加碘液测定唾液稀释倍数时,用吸量管吸取少量碘液沿管壁加入一滴即可,本次实验过程中,由于经验不足,加入碘液过多无法辨认颜色最适中的试管,导致重做。
(3)由实验可知:过酸过碱都会抑制酶的活性,使之淀粉的分解减少,A值增大;
(4)最适PH不是酶的特征性常数,它受底物浓度、缓冲液种类与浓度以及酶纯度等因素的影响。溶液PH高于或低于最适PH时,酶活性降低,远离最适PH时还会导致酶变性。在测定酶活性时,应选用适宜的缓冲液以保持酶活性的相对恒定。
(5)本实验中可能导致结果误差的原因:在配制不同PH缓冲液和测定唾液淀粉酶 最适PH中加入试剂时若未混匀,将对实验结果造成一定影响;本实验中配制的碘液浓度相对而言比较高,碘液的颜色将实际反应的颜色遮蔽,导致实验结果不能准确观察
参考文献:
[1]吴耀生 医学生物化学与分子生物学实验指南 人民卫生出版社
[2]查锡良、周春燕 . 生物化学 . -第7版-北京:人民卫生出版社2008.1:75
第二篇:唾液淀粉酶活力的测定
唾液淀粉酶活力的测定
一、实验目的
了解并掌握唾液淀粉酶活力的测定方法
二、实验原理
唾液淀粉酶能催化水解淀粉,生成分子较小的糊精和麦芽糖。本实验利用碘的呈色反应来测定唾液淀粉酶水解淀粉作用的速度,从而测定唾液淀粉酶活力的大小。
三、实验仪器和试剂
1. 仪器
(1)多孔白瓷板 (2)50mL三角瓶 (3)恒温水浴锅
(4)烧杯 (5)500mL容量瓶 (6)100mL容量瓶
(7)漏斗 (8)吸管
2. 试剂
(1)原碘液:称取碘11g、碘化钾22g,加少量蒸馏水完全溶解后,定容至500mL,于棕色瓶中保存。
(2)稀碘液:吸取原碘液2mL,加碘化钾20g,用蒸馏水溶解,定容至500mL,于棕色瓶保存。
(3)标准“终点色”溶液
①准确称取氯化钴40.2439g、重铬酸钾0.4878g,加蒸馏水溶解并定容至500mL。
②准确称取铬黑T 40mg,加蒸馏水溶解并定容至100mL。
取①液80mL与②液10mL混合,即为终点色。冰箱保存。
Page 1 of 3
(4)2%可溶性淀粉溶液:称取烘干可溶性淀粉2.00g,先以少许蒸馏水混匀,倾入80mL沸水中,继续煮沸至透明,冷却后用蒸馏水定容至100mL。(需新鲜配制)
(5)稀释100倍的唾液
用蒸馏水漱口,以清除食物残渣,然后让唾液流入量筒并稀释100倍,混合备用。
(6)0.02mol/L、pH6.8磷酸氢二钠-柠檬酸缓冲溶液:称取磷酸氢二钠45.23g和柠檬酸8.07g,用蒸馏水溶解后定容至1000mL,配好后用酸度计或精密试纸校正pH。
四、操作步骤
(1)将“标准色”溶液滴于白瓷板的左上角空穴内,作为比较终点色的标准。
(2)在50mL的三角瓶中,加入2%可溶性淀粉溶液20mL,加缓冲液5mL在37℃水浴中平衡约10min,加入0.5mL稀释唾液,立即记录时间,充分摇匀。定时用滴管取出反应液约0.25mL,滴于预先充满此稀碘液(约0.75mL)的调色板空穴内,当空穴颜色由紫色变为棕红色,与标准色相同时,即为反应终点,记录时间T(min)。
五、计算
1mL唾液淀粉酶于37℃、pH 6.8的条件下,1h液化可溶性淀粉的克数,称为唾液淀粉酶的活力单位。
酶活力单位=(60/T×20×2%×n)/0.5
n ——唾液淀粉酶稀释倍数
Page 2 of 3
60 ——1h(60min)
0.5 ——吸取待测唾液淀粉酶的量(mL)
2%——淀粉浓度
20 ——2%可溶性淀粉溶液的量(mL)
T ——反应时间(min)
六、注意事项
1. 全部时间应该控制在2~2.5min,否则应改变稀释倍数,重新测定。
2. 实验中,吸取2%可溶性淀粉及稀释唾液淀粉酶的量必须准确,否则误差较大。
Page 3 of 3
