碘钟反应
2012301040010 杨平
一、实验目的
1.掌握“碘钟”反应的原理。学会运用“碘钟”反应设计动力学实验的方法。
2.测定过硫酸根与碘离子的反应速率常数.反应级数和反应活化能.
二、实验原理
在水溶液中,过二硫酸铵与碘化钾发生如下反应:
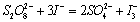 (1)
(1)
为了能够测定一定时间(Δt)内S2O82- 浓度的变化量,在混合过二硫酸铵、碘化钾溶液的同时加入一定体积已知浓度并含有淀粉(指示剂)的Na2S2O3 溶液,在式(1)进行的同时,有下列反应进行:
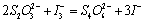 (2)
(2)
反应(2)进行得非常快,而反应(1)却缓慢得多,故反应(1)生成的I3 -立即与S2O32- 作用生成无色的S4O62- 和I? ,因此反应开始一段时间内溶液无颜色变化,但当Na2S2O3耗尽,反应(1)生成的微量碘很快与淀粉作用,而使溶液呈现特征性的蓝色。由于此时(即Δt) S2O32- 全部耗尽,所以S2O82- 的浓度变化相当于全部用于消耗Na2S2O3。由上可知,控制在每个反应中硫代硫酸钠的物质的量均相同,这样从反应开始到出现蓝色的这段时间可作为反应初速的计量。由于这一反应能显示自身反应进程,故称为“碘钟”反应。
1、反应级数和速率常数的确定
当反应温度和离子强度相同时,(1)式的反应速率方程可写为:
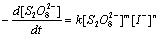 (3)
(3)
在测定反应级数的方法中,反应初速法能避免反应产物的干扰求的反应物的真实级数。
如果选择一系列初始条件,测得对应于析出碘量为Δ[I2]的蓝色出现的时间Δt,则反应的初始速率为:
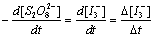 (4)
(4)
根据(2)式的反应计量关系结合硫代硫酸钠的等量假设,可知
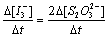 (5)
(5)
根据(3)(4)(5)可知,
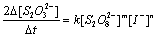 (6)
(6)
移项,两边取对数可得
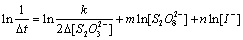 (7)
(7)
因而固定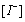 ,以
,以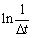 对ln
对ln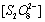 作图,根据直线的斜率即可求出
作图,根据直线的斜率即可求出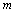 ;固定
;固定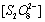 ,同理可以求出
,同理可以求出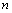 。然后根据求出的
。然后根据求出的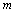 和
和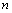 ,计算出在室温下“碘钟反应”的反应速率常数
,计算出在室温下“碘钟反应”的反应速率常数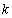 。
。
2、反应活化能的确定
根据Arrhenius公式
六.数据处理与分析
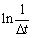 与ln
与ln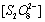 的关系见表3。
的关系见表3。
表3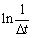 与
与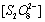 的关系数据表
的关系数据表
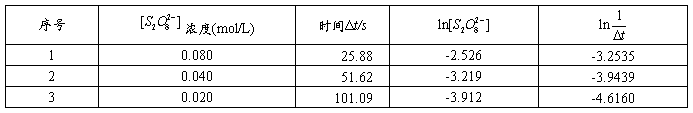
根据表3的数据作图,见图1。
图1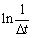 与ln
与ln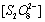 关系图
关系图
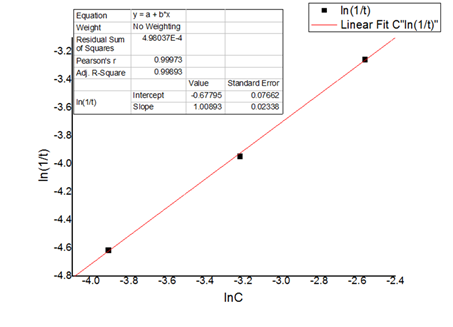
由图1可知m=1.009
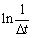 与
与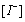 的关系见表4。
的关系见表4。
表4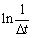 与
与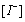 的关系数据表
的关系数据表
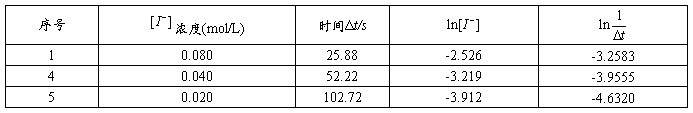
根据表4的数据作图2。
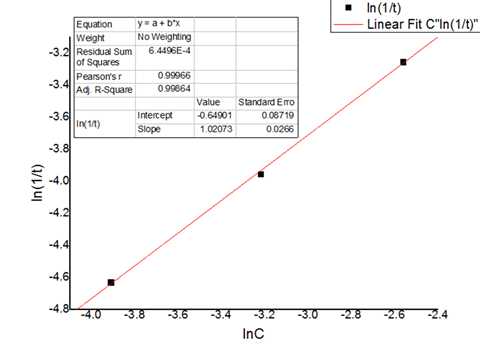
图2.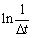 与
与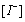 的关系图
的关系图
由图2知n=1.021
5.2反应速率常数的测定
我们根据(6)式可知,知道m,n,这样就可以计算出反应速率常数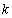 的值了。
的值了。
表5 反应速率常数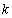 的测定(21.0℃条件下)
的测定(21.0℃条件下)

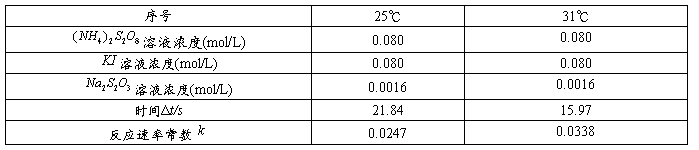
同理可以计算25℃和31℃时反应速率常数k。
表6 25℃和31℃时反应速率常数k
5.3反应活化能的测定
计算得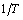 与
与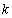 的关系如表7所示:
的关系如表7所示:
表7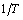 与
与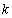 的关系表
的关系表
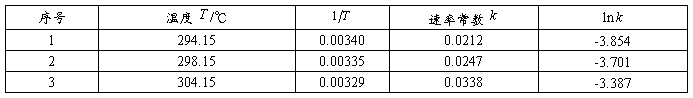
作lnk和1/T的关系图
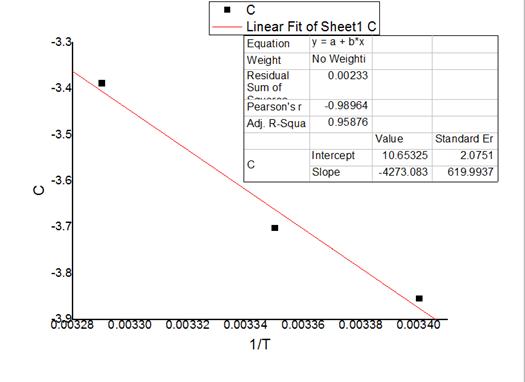
图3 lnk和1/T的关系图
由(8)式可知Ea=8.314*4273=35.53 KJ/mol
5.4 反应结果的表达:
a).反应级数:测得[S2O82-]的反应级数m=1.009,[I-]的反应级数n=1.021,总的反应级数m+n=2.030
b).反应速率常数:在21ºC条件下,该反应的速率常数为0.0212L/(mol?s);
在25ºC条件下,该反应的速率常数为0.0247L/(mol?s);
在31ºC条件下,该反应的速率常数为0.0338L/(mol?s)。
c).反应活化能:Ea=35.53KJ/mol
第二篇:碘钟反应的动力学和热力学参数的测定完整实验报告
碘钟反应”的反应级数、速率常数和活化能的测定实验报告
化学学院 材化班
一、 实验目的
1、用初速法测定过硫酸根与碘离子的反应速率常数和反应级数。
2、掌握碘钟反应过程及其原理。
二、简要实验原理
在水溶液中,过二硫酸铵与碘化钾发生如下反应[1]:
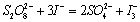 (1)
(1)
我们事先同时加入少量的硫代硫酸钠溶液和淀粉指示剂,则(1)式中产生的少量的 会优先和
会优先和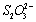 反应而被还原成
反应而被还原成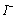 :
:
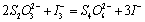 (2)
(2)
这样,当溶液中的硫代硫酸钠全部反应掉后,(1)式生成的碘才会和淀粉指示剂反应,使溶液呈蓝色。由上可知,控制在每个反应中硫代硫酸钠的物质的量均相同,这样从反应开始到出现蓝色的这段时间即可用来度量本反应的初速。
当反应温度和离子强度相同时,(1)式的反应速率方程可写为:
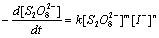 (3)
(3)
根据(1)式中的反应计量关系,可以认为:
 (4)
(4)
根据(2)式的反应计量关系结合硫代硫酸钠的等量假设,可知
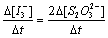 (5)
(5)
根据(3)(4)(5)可知,
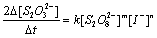 (6)
(6)
移项,两边取对数可得
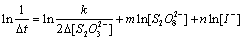 (7)
(7)
因而固定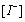 ,以
,以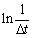 对
对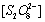 作图,根据直线的斜率即可求出
作图,根据直线的斜率即可求出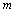 ;固定
;固定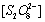 ,同理可以求出
,同理可以求出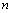 。然后根据求出的
。然后根据求出的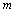 和
和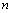 ,计算出在室温下“碘钟反应”的反应速率常数
,计算出在室温下“碘钟反应”的反应速率常数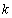 。
。
最后改变温度,测出不同温度下从反应开始到出现蓝色所需的时间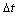 ,计算出不同温度下的反应速率常数,由Arrhenius公式,以
,计算出不同温度下的反应速率常数,由Arrhenius公式,以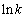 对
对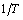 作图,根据直线的斜率即可求出活化能。
作图,根据直线的斜率即可求出活化能。
三、主要的实验仪器及试剂
恒温水浴槽一套;
50mL烧杯两个;
玻璃棒一支;
秒表一只;
0.20M 溶液;
溶液;
0.20M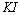 溶液;
溶液;
0.01M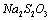 溶液;
溶液;
4%淀粉溶液;
0.20M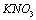 溶液;
溶液;
0.20M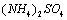 溶液。
溶液。
四、实验内容
1、反应级数和速率常数的测定
按照表1所列数据将每组的 溶液、
溶液、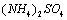 溶液和淀粉溶液放入烧杯A中混合均匀,
溶液和淀粉溶液放入烧杯A中混合均匀,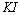 溶液、
溶液、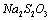 溶液和
溶液和 溶液放入B烧杯中混合均匀。然后将两份溶液混合,当混合至一半时开始计时,并不断搅拌,当溶液出现蓝色时即停止计时。
溶液放入B烧杯中混合均匀。然后将两份溶液混合,当混合至一半时开始计时,并不断搅拌,当溶液出现蓝色时即停止计时。
表1 “碘钟反应”动力学数据测量的溶液配制表
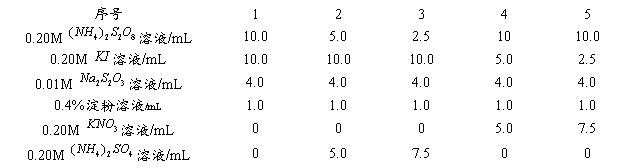
2、反应活化能的测定
按照表1中第1组反应的溶液配制方案配制溶液,分别在10.0、30.0和40.0℃下按照3.1中的操作步骤测量溶液出现蓝色所需的时间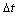 并记录,要注意必须先将溶液在相应的水浴槽中恒温一段时间,待溶液温度与恒温槽温度相同后再将溶液进行混合。
并记录,要注意必须先将溶液在相应的水浴槽中恒温一段时间,待溶液温度与恒温槽温度相同后再将溶液进行混合。
五、实验数据的记录
1、反应级数和速率常数测定的数据记录
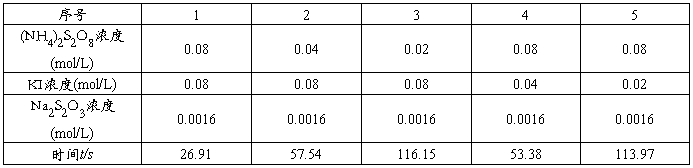
2、不同温度下反应1时间记录

六、实验数据的处理
1、反应级数和速率常数的计算
由5、1数据表格,我们可以依次求出反应级数及数率常数K。
(S2O2-8)反应级数的测定
Ln1/△t与ln(S2O2-8)关系数据表

有计算机做出Ln1/△t与ln(S2O2-8)关系图得:
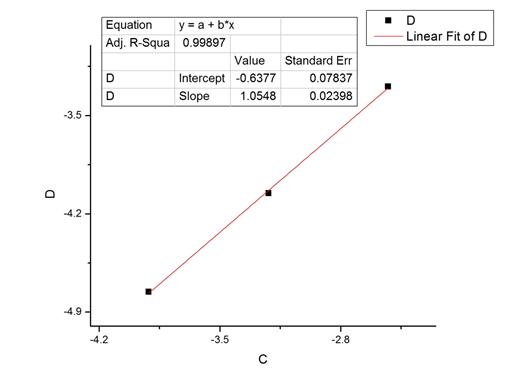
由图可知:Ln1/△t=1.0548ln(S2O2-8)-0.6377,其中相关系数r=0.99897.对比可知1.0548即为
(S2O2-8)的反应级数。
(I-)反应级数的测定
Ln1/△t与ln(I-)关系数据表

由计算机做出Ln1/△t与ln(I-)关系图得:
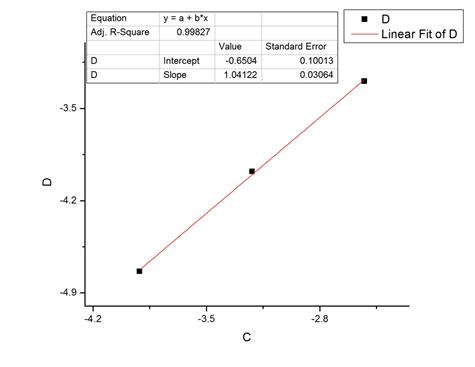
由图可知:Ln1/△t=1.04122 ln(I-)-0.6504.其中相关系数r=0.99827.对比公式可知n=1.04122,这就是I2的反应级数。
2、反应数率常数的测定
根据公式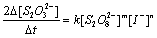
将m、n的值代入,即可算出k的值。
实验数据的处理见下表
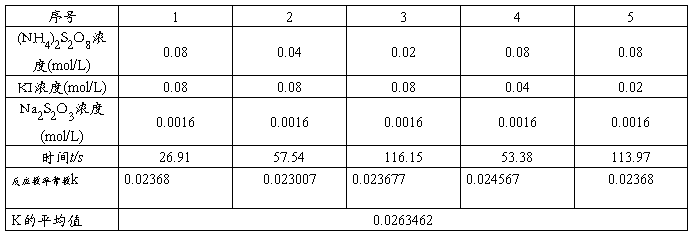
由上可知,此反应数率常数为k=0.0263462
3、反应活化能的测定
Lnk对1/T的数据关系见下表:

Lnk对1/T由计算机作图得:
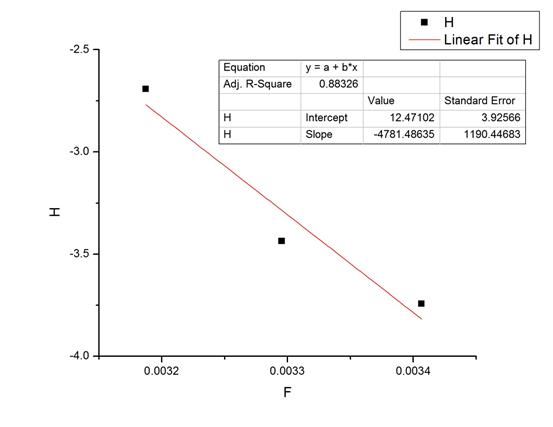
由阿伦尼乌斯公式两边取对数得:lnk=lnA-Ea/RT.
线性拟合的结果为lnk=12.471-4781.48/T, 则由此计算出的活化能为Ea=4781.48*8.314=39.752kJ/mol.
七、实验结果讨论
1、温度对实验的影响
显然,温度越高,反应速率越大。且观察发现,随着温度的升高,碘最终与淀粉的显色越深,可能是由于高温下淀粉糊化,支链结构发生改变,影响碘与淀粉的络合。
2、其他因素对实验的影响
反应计时起始时间,搅拌的程度,溶液体积的变化均会对实验结果产生影响。
