验证总计划
一、简介
二、验证的目的及合格标准
三、组织机构及职责
四、验证的原则要求
五、相关文件
六、验证进度计划及内容
七、附录:平面布置图、工艺流程图、系统图以及其他各种图表
一、简介:
本次验证规划项目制剂生产车间,计划项目建设总投资 万元,建筑面积 10000平方米左右,生产头孢粉针剂、冻干粉针剂与固体制剂、头孢胶囊。项目包括以下内容:
1、空气净化系统
2、工艺用水(纯化水、注射用水)系统
3、生产工艺
4、压缩空气
5、生产设备(包括灭菌设备)
6、药液过滤及灌封工艺
二、验证的目标
确认本项目的所有系统运转正常,始终如一地生产出符合法定标准的产品,确保产品不受污染。整过过程符合GMP及其附录要求。
三、组织机构及其职责
根据本项目及生产品种的特点,结合公司实际情况,特设立验证小组,并明确职责如下:
组长: 唐小波负责验证的总体策划与协调,验证文件的审核批准,并为验
证提供足够的资源。
副组长:杨自英 负责供应商审计、计量器具校正、检验方法的确认;负责日常验证活动的协调,掌握日常验证进度,安排验证文件的制订和审核;承担验证项目的具体实施工作。
组员: 谢文娟、王建文、朱燕、洪燕、徐玉红、俞峰、许道威、王落雁等
谢文娟、朱燕、王落雁 三人负责空气净化系统验证方案、纯化水系统、压缩空气系统验证方案。 谢文娟、洪燕、俞峰、许道威四人负责生产设备确认及清洗效果验证方案、环境消毒方法及效果的验证方案、生产工艺验证方案的起草、小结、评价及报告;参与验证实施工作。
四、验证的原则要求
1、验证方案遵循“谁用谁起草”的原则
2、验证方案必须经审核批准后方可执行
3、验证方案起草内容应遵循GMP文件相关项目的规定
4、验证过程中发生的问题、偏差,应如实记录并详细的说明并附在验证报告中。
五、相关文件:
1、中国药典20xx年版一部、二部
2、公司验证GMP文件
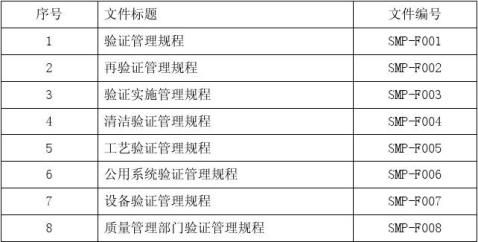
六、验证进度计划与内容
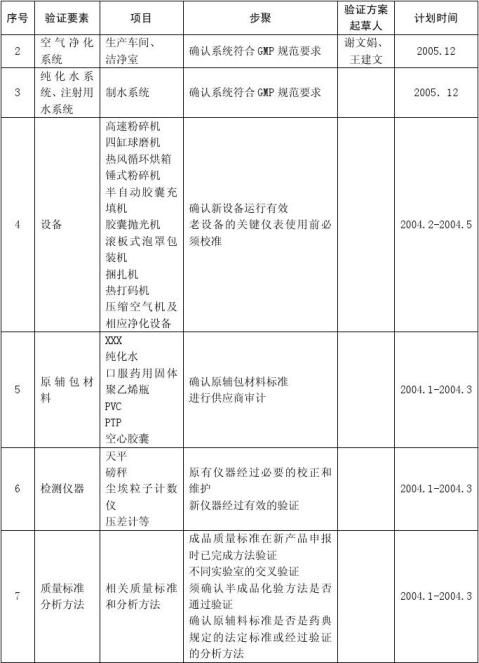
续上表:
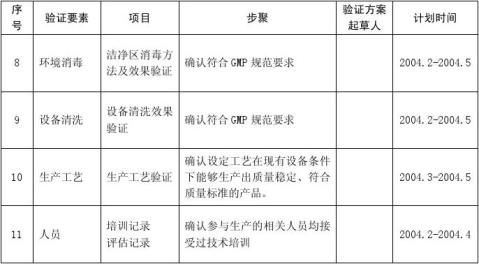
XXXXXXXXXXXXXXXXXXX
二○○四年一月十日
第二篇:比对和验证试验计划
比对和验证试验计划
编 号: 年 月 日

比对和验证试验分析总结报告
编 号: 年 月 日

图A.1 比对和验证试验计划格式
